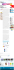471-476 Rebonato - Recenti Progressi in Medicina
Transcript
471-476 Rebonato - Recenti Progressi in Medicina
471 Recenti Prog Med 2012; 103: 471-476 Carcinoma renale di piccole dimensioni (≤4 cm): pattern di enhancement con TC spirale multistrato trifasica Alberto Rebonato1, Luisa Pierotti2, Francesco Barberini3, Giovanni Rosi1, Luca Macarini4, Michele Scialpi1 Riassunto. Gli autori definiscono i criteri semeiologici quali-quantitativi per il carcinoma renale di piccole dimensioni (CR) mediante TC trifasica. In 24 pazienti affetti da CR, in fase cortico-midollare (FCM) sono state identificate 12 lesioni ipervascolari e 12 lesioni ipovascolari. I CR ipervascolari hanno mostrato un incremento densitometrico in FCM (170,7±46,3 UH) ed un graduale wash-out in fase nefrografica (152,5±41 UH) e in fase pielografica (99,2±38 UH). I CR ipovascolari hanno evidenziato un incremento densitometrico in FCM (52,9±24,7 UH) ed un graduale wash-out in fase nefrografica (64,5±16,9 UH) e in fase pielografica (di 55,0±17,3 UH). Small renal cell carcinoma (≤4 cm): enhancement patterns on triphasic spiral CT. Parole chiave. Carcinoma renale, TC trifasica. Key words. Renal cell carcinoma, triphasic CT. Introduzione Materiali e metodi L’impiego routinario nella pratica clinica dell’ecografia (US) e della tomografia computerizzata (TC) ha sensibilmente modificato l’approccio nei pazienti in urgenza ed oncologici1-4 ed ha reso più frequente l’identificazione incidentale di piccoli (≤4 cm) tumori renali. Si tratta, nell’80-85%, di carcinomi renali (CR) che rappresentano il 3% delle neoplasie maligne nell’adulto5. L’approccio diagnostico a tali lesioni, come per lesioni a carico di altri organi, mediante citologia agoaspirativa rimane controverso6-8. Allo stato attuale, nonostante i riconosciuti risultati della risonanza magnetica (RM) nella differenziazione tra lesioni “benigne” e “maligne” e dei vari istotipi9-11, la tomografia computerizzata (TC) trifasica è considerata la metodica di elezione; in alcuni casi particolari, l’associazione con la SPECT può essere di ausilio nella diagnosi di neoplasie renali rare12. Una valida metodologia di studio per tali lesioni al fine di un’accurata valutazione è rappresentata dall’associazione di un’analisi qualitativa ad un’analisi quantitativa mediante la determinazione di curve tempo-densità. Scopo del nostro studio è stato determinare aspetti semeiologici quali-quantitativi per la diagnosi di CR di piccole dimensioni (≤4 cm) mediante TC spirale trifasica. Sono stati analizzati retrospettivamente gli esami TC trifasici di 24 pazienti (11 femmine, 13 maschi; età media 61 anni) con diagnosi istologica ed immunoistochimica di CR (≤4 cm), da ottobre 2008 a giugno 2011. Lo studio è stato condotto in conformità con la dichiarazione di Helsinki e con le norme vigenti in Italia secondo la GCP (Good Clinical Practice). È stato richiesto il consenso informato del paziente. Summary. The aim of this study was to define enhancement patterns of small renal cell carcinoma (RCC) (≤4 cm) by triphasic spiral CT. In 24 patients with RCC, hypervascularity and hypovascularity were identified in 12 and 12 RO, respectively, in the cortico-medullary phase (CMP). Hypervascular RCC showed increased density in the CMP (170,7±46,3 UH) and a gradual wash-out in the nephrographic phase (NP) (152,5±41 UH) and pielographic phase (PF) (99,2±38 UH). Hypovascular RCC showed increased density in the CMP (52,9±24,7 UH) and a gradual wash-out in NP (64,5±16,9 UH) and PP phases (55,0±17,3 UH). TECNICA Gli esami TC sono stati eseguiti con apparecchiatura TC 16 strati (Light Speed Pro 16, GE, Milwaukee, USA) e 64 strati/rotazione (Philips Brilliance, Best). Il protocollo TC trifasico ha previsto, successivamente ad un’acquisizione volumetrica diretta dell’addome superiore, un’acquisizione in fase cortico-midollare (FCM), nefrografica (FN) e pielografica (FP). Il tempo di ritardo dall’inizio dell’iniezione del mezzo di contrasto (mdc) per vena è stato registrato a 35-40 sec per la FCM, a 70-80 sec per la FN e a 5 min per la FP. È stata utilizzata una quantità media di 150 ml di mdc organo-iodato per paziente alla concentrazione di 300-370 mgI/ml (iopromide; Ultravist Schering, Berlino, Germania), 320 mgI/ml (iodixanolo; Visipaque; GE Healthcare, Milwaukee, USA), somministrato mediante un iniettore (Endovision CT injector, Medrad, Italia) con velocità di flusso di 4,0 ml/sec da una vena antecubitale usando un ago di calibro 18gauge seguito da 20 ml di soluzione salina a 4 ml/sec. 1 Diagnostica per Immagini e Radioterapia, Università di Perugia; 2Unità Operativa di Radiologia, Ospedale di Budrio, AUSL di Bologna; 3Dipartimento di Scienze Chirurgiche, Radiologiche ed Odontostomatologiche, Struttura Complessa di Chirurgia Oncologica, Università di Perugia; 4Dipartimento di Scienze Chirurgiche, Università di Foggia. Pervenuto il 26 settembre 2012. 472 Recenti Progressi in Medicina, 103 (11), novembre 2012 Spessore della fetta era di 2,5 mm, velocità di rotazione del gantry di 0,75 sec, indice di ricostruzione 1,25; passo: 0,935:1, 120 kVp e controllo automatico della corrente al tubo (mA) mediante modulazione sull’asse z (Auto mA o Z-DOM). Gli esami TC sono stati completati con ricostruzioni multiplanari sagittali e coronali. Il bolus test non è stato effettuato in nessuno dei pazienti; tuttavia, nessuno dei pazienti presentava ridotta gittata cardiaca o significative alterazioni della funzionalità renale. ANALISI DELLE IMMAGINI Le immagini TC sono state analizzate in due fasi: analisi qualitativa e analisi quantitativa dei tumori. Entrambe le analisi sono state effettuate su una stazione di lavoro per la segnalazione ed elaborazione delle immagini (Advantage Workstation 4,2 GE Healthcare e MagicView, Philips Medical Systems, Best, Olanda). Per l’analisi qualitativa del tumore, tutte le immagini sono state retrospettivamente valutate in consenso da due radiologi (MS e AR, con 16 e 6 anni rispettivamente di esperienza in TC addominale) e le conclusioni sono state effettuate in consenso. L’analisi qualitativa ha consentito il rilievo di due pattern di enhancement delle lesioni durante la FCM: – lesioni iperdense o ipervascolari (figura 1): densità simile o superiore a quella della corticale durante la FCM; – lesioni ipodense o ipovascolari (figura 2): densità inferiore a quella della corticale in FCM. Inoltre, sono stati definiti l’omogeneità/eterogeneità della lesione (presenza o assenza di aree emorragiche ne- Figura 1. TC multistrato in fase cortico-midollare: piccolo carcinoma ipervascolare disomogeneo mesorenale del labbro posteriore del rene destro. crotiche nel contesto che definiscono la disomogeneità), i contorni e la presenza di una possibile capsula/pseudocapsula. L’analisi quantitativa dei valori medi di attenuazione (UH) in ciascuna fase di acquisizione ha consentito la determinazione di curve tempo-densità per ogni lesione. I valori di attenuazione sono stati misurati sulle immagini ottenute in ciascuna delle tre fasi mediante una regione di interesse (ROI) per ogni lesione. La ROI ha coperto la metà dei due terzi della lesione evitando calcificazioni, aree di necrosi ed emorragia. I valori ottenuti sono stati utilizzati per generare curve di attenuazione per ogni lesione in tutte le fasi CT. Per ogni lesione è stata calcolata la percentuale assoluta e relativa del wash-out in FN e FP con la seguente formula: wash-out % assoluto in FN o FP = (attenuazione in FCM – attenuazione FN o FP)/ attenuazione in FCM – attenuazione basale x 100 wash-out % relativo in FN o FP = (attenuazione in FCM – attenuazione FN o FP)/ attenuazione in FCM x 100 ANALISI STATISTICA Per l’analisi comparativa dei valori medi di attenuazione (in HU + SD) delle lesioni e della corticale renale è stato utilizzato il test t di Student. Un valore di p inferiore a 0,05 è stato considerato statisticamente significativo. Per l’analisi statistica è stata utilizzata una versione di software SPSS per Windows (release13.0, SPSS Inc., Chicago). Figura 2. TC multistrato in fase cortico-midollare: piccolo carcinoma ipovascolare al 1/3 medio-superiore del rene sinistro. A. Rebonato et al.: Carcinoma renale di piccole dimensioni (≤4 cm): pattern di enhancement con TC spirale multistrato trifasica Risultati ANALISI QUANTITATIVA I valori di medi di attenuazione dei carcinomi ipervascolari, ipovascolari e della corticale renale nelle diverse fasi post-contrastografiche (FCM, FN e FP) sono I pattern di enhancement in FCM e le caratteristimostrati nelle tabelle 2 e 3 e nella figura 5. che delle lesioni all’analisi qualitativa sono riportati in I CR ipervascolari all’esame basale hanno evidentabella 1. I CR (n=24) sono risultati parimenti ipervaziato un valore medio di attenuazione di 34,4±7,4 UH, scolari (n=12) e ipovascolari (n=12). Le lesioni sono ricon un incremento densitometrico in FCM (valore mesultate disomogenee in tutti i casi iper- e ipovascolari (fidio di attenuazione di 170,7±46,3 UH) ed un graduale gure 3 e 4); una pseudocapsula era presente in due CR wash-out in FN (valore medio di attenuazione di ipervascolari e in due CR ipovascolari. 152,5±41 UH) e in FP (valore medio di attenuazione di 99,2±38 UH). Rispetto alla corticale renale, i CR ipervascolari hanno mostrato una differenza statisticamente non siTabella 1. Pattern di enhancement in FCM e parametri caratteristici di 24 carcinomi renali (CR). gnificativa in tutte le fasi postcontrastografiche (p>0,05). CR n=24 Omogeneo Disomogeneo Pseudocapsula I CR ipovascolari all’esame basale hanno evidenziato un vaIpervascolari (n=12) 0 12 2 lore medio di attenuazione di 32,7±11,7 UH con un incremenIpovascolari (n=12) 0 12 2 to densitometrico in FCM (valore medio di attenuazione di ANALISI QUALITATIVA a b c Figura 3. TC multistrato trifasica: piccolo carcinoma renale ipervascolare disomogeneo al 1/3 medio del rene destro. La lesione esibisce massimo enhancement in FCM (a) e graduale wash-out in FN (b) e FP (c). a b Figura 3. TC multistrato trifasica: piccolo carcinoma renale ipovascolare disomogeneo al 1/3 medio del rene destro. La lesione disomogeneamente ipodensa in FCM (a) esibisce graduale enhancement in FN (b) e FP (c). c 473 474 Recenti Progressi in Medicina, 103 (11), novembre 2012 Tabella 2. Valori medi di attenuazione dei carcinomi ipervascolari e della corticale renale. Basale FCM FN FP Carcinomi (media ± DS) 34,4 ± 7,4 170,7±46,3 152,5±41 99,2± 38 Corticale (media ± DS) 38,1±2 195,1 ±24,8 206,6±37,6 142,3±27,8 Tabella 3. Valori medi ± DS di attenuazione dei carcinomi ipovascolari e della corticale renale. Basale FCM FN FP Carcinomi (media ± DS) 32,7±11,7 52,9±24,7 64,5±16,9 55,0±17,3 Corticale (media ± DS) 36,9±2,9 178,8±46,1 190,6±32,4 130,5±22,3 Figura 5. Valori di attenuazione medi dei carcinomi ipervascolari, ipovascolari e della corticale renale. 52,9±24,7 UH) ed un graduale wash-out in FN (valore medio di attenuazione di 64,5±16,9 UH) e in FP (valore medio di attenuazione di 55,0±17,3 UH). Rispetto alla corticale renale, i CR ipovascolari hanno mostrato una differenza statisticamente significativa (p<0,01) in tutte le fasi post-contrastografiche. Nella figura 6 è riportata la percentuale di wash-out assoluto e relativo degli CR ipovascolari ed ipervascolari suddivisi negli istotipi RCC e CR papillari. I CR papillari ipovascolari hanno presentato una percentuale di wash-out assoluto e relativo rispettivamente di –214,7 e –23,5. I CR papillari ipervascolari hanno presentato una percentuale di wash-out assoluto e relativo rispettivamente di 51 e 42,1. I RCC ipovascolari hanno presentato una percentuale di wash-out assoluto e relativo rispettivamente 21,9 e –7,1. I RCC ipervascolari hanno presentato una percentuale di wash-out assoluto e relativo rispettivamente di 51,1 e 43,4. Discussione Figura 6. Percentuale di wash-out assoluto e relativo dei carcinomi (RCC e CR papillari). Il CR rappresenta la variante istologica più frequente (approssimativamente 70%) dei CR13 seguito dal carcinoma papillare (1015%) e dal carcinoma a cellule cromofobe (5%). La TC spirale multifasica con apparecchiature sia a singolo che a multidetettore, mediante acquisizioni volumetriche dei reni in A. Rebonato et al.: Carcinoma renale di piccole dimensioni (≤4 cm): pattern di enhancement con TC spirale multistrato trifasica FCM, FN e FP consente una valutazione morfofunzionale nonché del grado di vascolarizzazione dei reni e di lesioni focali14-16. Sebbene tali studi dimostrino una maggiore accuratezza della FN e della FP tardiva rispetto alla FCM nella diagnosi dei tumori renali, numerose lesioni rimangono indeterminate. La tecnica trifasica17 presenta il limite della dose eccessiva di radiazioni al paziente, limite recentemente superato con l’introduzione della UroTC, con la tecnica dello split-bolus che consente risultati analoghi alla tecnica trifasica nella identificazione e determinazione dell’enhancement di piccole masse renali con il vantaggio di ridurre la dose di radiazioni al paziente18. Nello studio di una massa renale, i dati clinicoanamnestici e la semeiotica TC e RM rappresentano gli elementi essenziali: criterio di riferimento è la determinazione dell’enhancement. In linea generale, una lesione solida che esibisce enhancement dopo mdc per vena in TC o in RM è da considerare neoplastica. Sia la TC sia la RM devono specificare il grado di vascolarizzazione di una lesione, essenziale in previsione di una di tumorectomia, in quanto vasi intratumorali possono formare comunicazioni con la normale vascolarizzazione renale, specie in sede capsulare, con maggiore possibilità di metastasi per via ematica. Un’attenta valutazione di esami TC di qualità diagnostica, insieme al contesto clinico, consente la determinazione della natura delle lesioni praticamente nella maggior parte dei casi e pertanto la biopsia non è necessaria. Il nostro studio ha previsto un protocollo di studio multifasico senza e dopo somministrazione di mdc per vena in FCM, FN e FP. L’analisi qualitativa ha consentito la determinazione dell’aspetto e del grado di vascolarizzazione delle lesioni, distinguibili in ipervascolari in 12/24 casi (50%) e ipovascolari in 12/12 casi (50%). L’analisi quantitativa dell’enhancement ha reso possibile la determinare di curve tempo/densità e della percentuale relativa ed assoluta di wash-out. I CR ipervascolari all’esame basale hanno evidenziato un valore medio di attenuazione di 34,4±7,4 UH, con un incremento densitometrico in FCM (valore medio di attenuazione di 170,7±46,3 UH) ed un graduale wash-out in FN (valore medio di attenuazione di 152,5±41 UH) e in FP (valore medio di attenuazione di 99,2±38 UH). I CR ipovascolari all’esame basale hanno evidenziato un valore medio di attenuazione di 32,7±11,7 UH con un incremento densitometrico in FCM (valore medio di attenuazione di 52,9±24,7 UH) ed un graduale wash-out in FN (valore medio di attenuazione di 64,5±16,9 UH) e in FP (valore medio di attenuazione di 55,0±17,3 UH). I CR ipovascolari hanno presentato una percentuale di wash-out assoluto e relativo rispettivamente di –21,9 e –7,1I, differentemente dai CR papillari ipovascolari che hanno presentato una percentuale di wash-out assoluto e relativo rispettivamente di –214,7 e –23,5. I CR ipervascolari hanno presentato una percentuale di wash-out assoluto e relativo rispettivamente di 51,1 e 43 sostanzialmente analoga ai CR papillari ipervascolari, che hanno presentato una percentuale di wash-out assoluto e relativo rispettivamente 51 e 42,1. Rispetto alla tecnica bifasica19, la tecnica trifasica20, pur non consentendo una diagnosi differenziale certa tra neoplasia benigna e maligna, permette una valutazione del wash-in in fase arteriosa ed anche il wash-out del mdc in FP tardiva, contribuendo validamente nell’orientamento diagnostico. Il limite principale del nostro studio è rappresentato dal fatto che lo studio è retrospettivo e presenta una casistica limitata relativamente ai vari istotipi. Nello studio infatti non sono inclusi carcinomi a cellule cromofobe. Conclusioni In conclusione, la TC multifasica (in FCM, FN e FP) mediante l’analisi quali-quantitativa dell’enhancement ha un importante impatto clinico nei pazienti con massa renale di piccole dimensioni, riducendo il numero dei falsi positivi con impatto notevole sulla scelta della terapia più adeguata (nefrectomia totale o parziale). Una lesione ipervascolarizzata disomogenea va considerata in prima istanza carcinoma, mentre una lesione ipovascolarizzata va differenziata da una cisti, che invece risulta avascolare. Fortemente discusso allo stato attuale è il ruolo della biopsia renale e della citoaspirazione per ago sottile, in relazione alle possibilità di “seeding” della neoplasia lungo il tragitto dell’ago o del dispositivo di accesso alla lesione21,22. Bibliografia 1. Cagini L, Vannucci J, Scialpi M, Puma F. Diagnosis and endovascular treatment of an internal mammary artery injury. J Emerg Med May 10 [Epub ahead of print]. 2. Scialpi M, Pierotti L, Piscioli I, et al. Detection of small (≤20 mm) pancreatic adenocarcinoma: histologic grading and CT enhancement features. Radiology 2012; 262: 1044-5. 3. Gilbert SM, Russo P, Benson MC, Olsson CA, Mckiernan JM. The evolving role of partial nephrectomy in the management of renal cell carcinoma. Curr Oncol Rep 2003; 5: 239-44. 4. Pusiol T, Zorzi MG, Morichetti G, Piscioli I, Scialpi M. Synchronous non functional duodenal carcinoid and high risk gastrointestinal stromal tumour (gist) of the stomach. Eur Rev Med Pharmacol Sci 2011; 15: 583-5. 5. Jemal A, Thomas A, Murray T, Thun M. Cancer Statistics, 2002. Cancer J Clin 2002; 52: 23-47. 6. Pusiol T, Zorzi MG, Morichetti D, Piscioli I, Scialpi M. Uselessness of percutaneous core needle renal biopsy in the management of small renal masses. Urol Int 2011; 87: 125-6. 7. Brancato B, Scialpi M, Pusiol T, Zorzi MG, Morichetti D, Piscioli F. Needle core biopsy should replace fine needle aspiration cytology in ultrasound-guided sampling of breast lesions. Pathologica 2011; 103: 52. 475 476 Recenti Progressi in Medicina, 103 (11), novembre 2012 8. Brancato B, Crocetti E, Bianchi S, et al. Accuracy of needle biopsy of breast lesions visible on ultrasound: audit of fine needle versus core needle biopsy in 3233 consecutive samplings with ascertained outcomes. Breast 2012; 21: 449-54. 9. Scialpi M, Cardone G, Barberini F, Piscioli I, Rotondo A. Renal oncocytoma: misleading diagnosis of benignancy by using angular interface sign at MR imaging. Radiology 2010; 257: 587-8. 10. Pusiol T, Zorzi MG, Morichetti D, Piscioli I, Scialpi M. Uselessness of radiological differentiation of oncocytoma and renal cell carcinoma in management of small renal masses. World J Urol May 21 [Epub ahead of print]. 11. Scialpi M, Brunese L, Piscioli I, Rotondo A. Dynamic contrast-enhanced MR imaging for differentiation of renal cell carcinoma subtypes: myth or reality? Radiology 2009; 252. 12. Tranfaglia C, Cardinali L, Gattucci M, et al. 111Inpentetreotide SPET/CT in carcinoid tumours: is the role of hybrid systems advantageous in abdominal or thoracic lesions? Hell J Nucl Med 2011; 14: 274-7. 13. Murphy WM, Beckwith JB, Farrow GM. Tumor of the kidney, bladder, and related urinary structures. In: Atlas of tumor pathology, 3rd ed. Fascicle 11. Washington, DC: Armed Forces Institute of Pathology, 1993. 14. Bertolini L, Vaglio A, Bignardi L, et al. Subclinical interstitial lung abnormalities in stable renal allograft recipients in the era of modern immunosuppression. Transplant Proc 2011; 43: 2617-23. 15. Birnbaum BA, Jacobs JE, Ramchandani P. Multiphasic renal CT: comparison of renal mass enhance- Indirizzo per la corrispondenza: Prof. Michele Scialpi Università Dipartimento di Scienze Chirurgiche, Radiologiche ed Odontostomatologiche Struttura Complessa di Radiologia 2 Ospedale S. Maria della Misericordia Loc. Sant’Andrea delle Fratte 06134 Perugia E-mail: [email protected] 16. 17. 18. 19. 20. 21. 22. ment during the corticomedullary and nephrographic phases. Radiology 1996; 200: 753-8. Szolar DH, Kammerhuber F, Altziebler S, et al. Multiphasic helical ct of the kidney: increased conspicuity for detection and characterization of small (<3 cm) renal masses. Radiology 1997; 202: 211-7. Kopka L, Fischer U, Zoeller G, Schmidt C, Ringert Rh, Grabbe E. Dual-phase helical CT of the kidney: value of the corticomedullary and nephrographic phase for evaluation of renal lesions and preoperative staging of renal cell carcinoma. AJR Am J Roentgenol 1997; 169: 1573-8. Maheshwari E, O’Malley ME, Ghai S, Staunton M, Massey C. Split-bolus mdct urography: upper tract opacification and performance for upper tract tumors in patients with hematuria. AJR Am J Roentgenol 2010; 194: 453-8. Jinzaki M, Tanimoto A, Mukai M, et al. Doublephase helical ct of small renal parenchymal neoplasms: correlation with pathologic findings and tumor angiogenesis. J Comput Assist Tomogr 2000; 24: 835-42. Shebel HM, Elsayes KM, Sheir KZ, et al. Quantitative enhancement washout analysis of solid cortical renal masses using multidetector computed tomography. J Comput Assist Tomogr 2011; 35: 337-42. De Filippo M, Corsi A, Evaristi L, et al. Critical issues in radiology: requests and reports. Radiol Med 2011; 116: 152-62. De Filippo M, Gira F, Corradi D, Sverzellati N, Zompatori M, Rossi C. Benefits of 3D technique in guiding percutaneous retroperitoneal biopsies. Radiol Med 2011; 116: 407-16.