621-633 Rass1-Testino - Recenti Progressi in Medicina
Transcript
621-633 Rass1-Testino - Recenti Progressi in Medicina
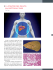
Rassegne Vol. 96, N. 12, Dicembre 2005 Pagg. 621-633 Steatosi ed epatopatia HCV correlata Gianni Testino Riassunto. Steatosi ed epatopatia HCV correlata sono due condizioni comuni e pertanto l’aspettativa di trovarle associate è legittima: la prevalenza della coesistenza è circa due-tre volte maggiore rispetto a quella che dovremmo aspettarci nel caso i due processi fossero indipendenti. In corso di epatopatia HCV sono state definite due condizioni: un quadro di “metabolic fat” caratterizzato da una correlazione fra steatosi ed alterazioni metaboliche ed un quadro di “viral fat” caratterizzato da un’azione diretta dell’HCV. In realtà ci si trova spesso in presenza di “forme miste”. Ad oggi, la maggior parte degli autori ritiene che la presenza di steatosi acceleri la progressione della fibrosi e quindi la progressione in cirrosi, incrementi il rischio di sviluppare epatocarcinoma e riduca la percentuale di risposta alla terapia antivirale sia nei soggetti immunocompetenti che in corso di recidiva post-trapianto. Il trattamento deve associare alla comune terapia antivirale tutte quelle misure atte ad affrontare le problematiche metaboliche, con particolare riferimento alla terapia antiossidante. Parole chiave. Cirrosi, epatite HCV, epatocarcinoma, fibrosi, sindrome metabolica, steatosi. Summary. Steatosis and hepatitis C. Steatosis and hepatitis C are two common liver diseases. Epidemiological and experimental data indicate that hepatitis C predisposes to non alcoholic fatty liver disease and the prevalence of coexistent hepatitis C and steatosis is two-three times higher than it would be expected if these were completely independent processes. Two conditions have been defined in course of hepatitis C: the “metabolic fat”, characterized by a correlation between steatosis and metabolic alterations and the “viral fat”, characterized by a direct action of HCV. Actually, “mixed forms” are often present. Up to today, most of the authors belive that the presence of steatosis accelerates the progression of fibrosis, and therefore the progression to cirrhosis, increases the risk of developing hepatocellular carcinoma, and decreases the antiviral therapy response percentage. The treatment must associate the common antiviral therapy with all the measures fit for facing the metabolic problems, with particular reference to the antioxidant therapy. Key words. Cirrhosis, fibrosis, hepatitis C virus, hepatocellular carcinoma, metabolic syndrome, steatosis. Sebbene, infatti, sull’associazione steatosi/ epatite HCV correlata siano state riportate in letteratura numerose esperienze, ad oggi in realtà, non vi sono ancora dati certi e definiti (figura 1). Le due condizioni sono patologie comuni e, quindi, l’aspettativa di trovarle associate è legittima: la prevalenza, infatti, della coesistenza di steatosi con epatite C è circa due-tre volte più elevata di quella che dovremmo aspettarci nel caso i due processi fossero completamente indipendenti: è evidente, quindi, come il rapporto possa essere diretto o comunque come la steatosi possa agire con l’HCV per alcuni aspetti in modo sinergico, per altri in modo additivo1-3. Le percentuali di associazione sono largamente variabili da uno studio all’altro anche in rapporto ai diversi tipi di valutazione: soprattutto i criteri istologici ed in particolare il grading e gli indici della steatosi utilizzati dai vari Autori so- Figura 1. Quadro di epatite HCV correlata con flogosi portale a disposizione nodulare, piecemeal necrosis e steatosi micro e macrovescicolare (gentilmente concessa dal prof. GL Ravetti e dalla prof R Gentile, UOC Istopatologia, Ospedale San Martino, Genova). Unità Operativa Dipartimentale Epato-Gastroenterologia, Dipartimento Trapianti di Organo, Azienda Ospedaliera Ospedale San Martino e Cliniche Universitarie Convenzionate, Genova. Pervenuto il 15 settembre 2005. 622 Recenti Progressi in Medicina, 96, 12, 2005 no spesso differenti 1. Inoltre, dato che l’incremento della steatosi nella maggior parte degli studi correla con quello dell’indice di massa corporea (BMI)4, la sua prevalenza in pazienti con epatite C dipende largamente dalla popolazione studiata con percentuali che possono superare l’80% (tabella 1). Certamente tale prevalenza è superiore rispetto a quella che possiamo rilevare in corso di epatite HBV correlata (27-51%) od in corso di epatite autoimmune (16-19%)3. Non vi è dubbio che la steatosi sia più frequente in corso di epatite HCV rispetto alla popolazione generale, dove tale fenomeno è presente in percentuali che, pur variando nei vari studi, si attestano mediamente intorno al 15-25%5. L’assunzione alcolica non viene sempre correlata in modo adeguato all’insorgenza di steatosi: ciò è da imputare al fatto che nella maggior parte degli studi non sono stati inclusi i forti bevitori, ma soprattutto al fatto che tale parametro risulta particolarmente difficile da quantificare. Relativamente al meccanismo “metabolic fat”, in numerose esperienze è evidente come nei casi HCV associati a steatosi vi siano, in modo statisticamentente significativo, maggiori problemati- Tabella 2. - Caratteristiche associate con la presenza di steatosi in corso di epatopatia HCV correlata. Casistica Steatosi metabolica e steatosi virale È noto ormai come in pazienti con epatite C si possa parlare di un quadro di “metabolic fat”, soprattutto in quelli con genotipo 1 ed un quadro di “viral fat”, in quelli con genotipo 3 6-8 (tabella 2). La comprensione di tale associazione e soprattutto la capacità di affrontarla attraverso una azione interdisciplinare può comportare indubitabili vantaggi nella pratica clinica: vi sono ripetute osservazioni, infatti, che indicano come nei soggetti portatori dei due quadri morbosi vi sia un incrementato rischio di progressione in cirrosi, un incrementato rischio di sviluppare epatocarcinoma ed, inoltre, una minore frequenza di risposta alla terapia antivirale. Questo, peraltro, anche in corso di recidiva HCV correlata nella fase post-trapianto. Caratteristiche Mihm et al. (1997) 85 Czaja et al. (1998) 60 Hourigan et al. (1999) 148 Rubbia et al. (2000) 70 Genotipo 3 BMI, Dislipidemia BMI Genotipo 3 (HCV-RNA intraepatico) Adinolfi et al. (2001) 180 BMI, Genotipo 3 Serfaty et al. (2002) 100 BMI, Genotipo 3 Monto et al. (2002) 297 BMI, Genotipo 3 Westin et al. (2002) 98 BMI, Alcool, Genotipo 3 Poynard et al. (2003) 1428 BMI, Genotipo 3 Castera et al. (2003) 96 BMI, Dislipidemia, Genotipo 3 Asselah et al. (2003) 290 BMI, Genotipo 3 Rubbia et al. (2003) 755 BMI, Alcool, Genotipo 3 Sanyal et al. (2003) 110 BMI, Diabete, Dislipidemia, S. Metabolica Cholet et al. (2004) 214 BMI, Genotipo 3 Testino et al. (2004) 88 BMI, Iperglicemia, Dislipidemia, S. Metabolica, Genotipo 3 Clouston et al. (2005) 148 BMI, S. Metabolica Tabella 1. - Frequenza e distribuzione della steatosi in corso di epatite HCV correlata. Mihm et al. (1997) Czaja et al. (1998) Rubbia et al. (2000) Adinolfi et al. (2001) Monto et al. (2002) Poynard et al. (2003) Castera et al. (2003) Asselah et al. (2003) Rubbia et al. (2003) Poynard et al. (2004) Cholet et al. (2004) Testino et al. (2004) Clouston et al.(2005) Casistica Steatosi (%) Genotipo 3 Altri genotipi Lieve (%) Moderata/Severa (%) 85 60 70 180 297 1428 96 290 755 574 314 88 148 73(86) 31(52) 28(40) 86(48) 171(58) 935(65) 51(54) 135(46) 315(42) 277(48) 182(58) 34(39) 91(61) – – 16/24(67) 20/26(77) – 175/210(83) 15/20(75) 36/58(63) 109/178(61) 61/84(72) 33/34(97) 8/11(73) 14/17(78) – – 12/46(67) 20/26(77) – 760/1218(62) 36/76(47) 97/232(42) 206/577(36) 216/490(44) 39/84(46) 26/77(34) 14/23(61) 60(82) 31(100) 16(65) 44(51) 146(85) 832(89) 42(82) 91(68) 206(65) 169(61) 90(49) 21(62) 61(67) 13(18) 0 7(25) 42(49) 25(15) 103(11) 9(18) 44(32) 109(35) 108(39) 92(182) 13(38) 30(33) 623 G. Testino: Steatosi correlata ad epatite C che metaboliche rispetto agli HCV isolati9,10. Ciò duce pertanto come l’IR non sia da riferire solo agli è emerso anche nella esperienza personale (88 castadi avanzati della patologia epatica. Gli elevati si con epatopatia HCV correlata, di cui 34 con livelli di insulina di per sè contribuiscono al pegsteatosi): sovrappeso (BMI >25) nel 76,4% dei cagioramento della patologia, favorendo direttamensi con steatosi e nel 33% di quelli senza, ipertente la fibrogenesi od i meccanismi di cancerogenesi sione nel 35% dei casi con steatosi e nell’11% di (figura 2). quelli senza, iperglicemia nel 32% dei casi con Per quanto riguarda la condizione di “viral fat”, steatosi e nel 9% di quelli senza, dislipidemia nel non solo evidenze epidemiologiche, ma anche tera53% dei casi con steatosi e nel 18,5% di quelli senpeutiche, hanno rilevato l’associazione steatosi/ geza, e sindrome metabolica (due o più criteri ATP notipo 3 (3a in particolare). III) nell’ 88% nei casi con steatosi e nel 31,5% di Numerose esperienze, infatti, hanno documenquelli senza. tato una correlazione, in corso di epatite da genoRelativamente al sovrappeso, di particolare imtipo 3, fra la risposta alla terapia antivirale e la riportanza è il deposito lipidico intra-addominale: duzione della steatosi16-18. Ciò non è stato rilevato in corso di infezione con altri genotipi. esso provvede ad un immediata risorsa di acidi Sebbene numerosi studi abbiano sottolineato un grassi liberi che direttamente confluiscono nella importante ruolo del genotipo 3 nella genesi della vena porta. Inoltre, i soggetti con obesità viscerale steatosi, il meccanismo rimane da definire. sono in possesso di bassi livelli di adiponectina e È noto come un ruolo della core protein, attrarelativi alti livelli di TNF-alpha. È noto come il verso numerosi meccanismi, sia stato ampiamenruolo dell’adiponectina sia quello di antagonizzare te suggerito e come sia stata dimostrata la sua insia la produzione che l’attività del TNF-alpha. La terferenza sul metabolismo lipidico19 (tabella 3 a combinazione di bassi livelli di adiponectina ed alpagina seguente). ti livelli di TNF-alpha in un contesto di una increIn particolare, Perlemuter et al. hanno ipotizzamentata esposizione epatica di acidi grassi liberi si to un elegante modello che prevede come la core protraduce in steatosi e severa insulino-resistenza tein inibisca l’attività della proteina microsomiale epatica11,12. Per quanto concerne l’insulino resistenza (IR), di trasferimento dei trigliceridi (MTP), inibendo coè bene segnalare come vi sia una stretta correlaziosì l’assemblaggio delle lipoproteine a bassisima denne con la infezione da HCV (indipendentemente sità (VLDL) e, quindi, la secrezione20,21. dal genotipo)13,14. È stato dimostrato come nei È bene sottolineare però il contrasto fra gli stutransgenic mouse per l’HCV core gene vi siano di sull’uomo (sia di ordine epidemiologico che teramaggiori livelli di insulina ed una minore tolleranpeutico), che hanno dimostrasto l’associazione geza al glucosio. Essendo la core protein incorporata, notipo 3/ steatosi ed i modelli sperimentali. si comprende come sia questa sequenza ad essere la causa della IR. La somministrazione di insulina in animali HOST HCV normali comporta la fo(Core protein/NS5A) sforilazione della tiroxina BMI – Visceral obesity Genotype 3 Genotype non 3 nell’ambito del substrato Hyperlipidemia (intra- hepatic replication) (Nitrosative stress) Type 2 Diabetes per il recettore dell’insuliInsulin Resistence na (IRS-1); ciò non accade STEATOSIS Metabolic syndrome nei transgenic mouse. Si Necro – Inflammatory Activity evince, pertanto, come il Peroxisome Mitochondria ER Alcohol (CYP 2E1, (AOX) (MRC) meccanismo alla base delCYP 4A10, “Endogenous Ethanol” la IR possa essere riconCYP 4R14) dotto ad un disturbo della Inflammatory –Cytochines OXIDATIVE STRESS (> TNF , > IL8, TGF 1, fosforilazione di tiroxi(Cell Death) PDGF,….) REACTIVE OXYGEN SPECIES na13,14. Aytug et al.15 hanATP and NAD depletion (O•, O •, OH•,H O ) IMPAIRMENT OF DNA and protein damage no confermato tale meccaRESPIRATORY Glutathione depletion nismo su preparati di CHIAN LIPID PEROXIDATION Y-Glu-Cys-Gly biopsia epatica. Sebbene questi dati indichino forSH temente un ruolo della inEndotoxin STELLATE CELLS KC activation fezione da HCV nel determinare IR, non possono Insulin MYOFIBROBLAST LIKE PHENOTYPE essere tuttavia esclusi i Leptin Others ECMProducing Cells Resistin meccanismi indotti da alPIA I- 1 FIBROSIS tri fattori. È stato dimostrato come la IR sia già presente Figura 2. Steatosi ed epatite HCV: vie metaboliche di danno epatico (Testino G, 2005 65). in corso di epatite C con fibrosi in stadio 0 o 1: si de2 (HNE - MDA) 2 2 624 Recenti Progressi in Medicina, 96, 12, 2005 Tabella 3. - Possibili meccanismi di steatosi HCV indotta. Ruolo diretto dell’HCV – core-protein induce un accumulo intracitoplasmatico di trigliceridi – alterazioni mitocondriali – inibizione attività Microsomal Triglyceride Transfer Protein (MTP) Promozione della insulino resistenza – alterazione della fosforilazione della tiroxina – riduzione della secrezione insulinica – riduzione adiponectina/ incremento TNF-alpha Alterazioni metaboliche – incremento della lipogenesi/ incremento lipolisi – decremento della formazione Apo B100 – interazione con la Apo A1 In tali modelli, infatti, la HCV core protein effettivamente produce steatosi diffusa, tuttavia tale steatosi appare microvescicolare piuttosto che prevalentemente macrovescicolare come nella maggior parte dei casi di studi sull’uomo. Inoltre, sono state utilizzate sequenze di prototipi del genotipo 1 e, peraltro, i livelli di espressione di tale sequenza nucleocapsidica sono in generale maggiori rispetto a quelli che possiamo osservare in vivo 22. È stato allora ipotizzato che la proteina virale responsabile per l’accumulo di grasso nelle infezioni umane non sia il nucleocapside e che i dati pubblicati siano circoscritti in modelli sperimentali. In alternativa, è stato ipotizzato come la core protein possa essere necessaria, ma non sufficiente, relativamente all’accumulo lipidico. La natura dei cofattori, però, ad oggi non è conosciuta, anche se il polimorfismo di uno o più fattori dell’ospite potrebbe condurre ad un meccanismo patogenetico maggiormente efficace. Numerosi fattori, infatti, sono stati descritti in vari modelli sperimentali: peroxisome proliferators-activated receptor alpha, fatty acyl-CoA oxidase, glycerol-3-phosphatase acyltransferase, tumor necrosis factor23. A suffragare comunque l’ipotesi “viral fat”1-3 sono dimostrazioni di una stretta correlazione fra steatosi e livelli sierici di HCV-RNA, ma soprattutto intraepatici: nella esperienza di Rubbia-Brandt et al. è bene evidente la correlazione con i livelli intraepatici ed in particolare per quanto riguarda il minus-strand: tutto ciò soprattutto in corso di infezione con genotipo 3a. Tale fenomeno viene descritto anche in soggetti sottoposti a trapianto di fegato, ove la correlazione si evidenzia solo in corso di infezione con genotipo 3a 19. Se eliminiamo dallo scenario le alterazioni metaboliche (o perlomeno la maggior parte di queste), meglio si evidenzia l’azione diretta del genotipo 3, che correla significativamente con la severità della steatosi, confermando la suddivisione fra “steatosi virale” da quella “metabolica”19. La steatosi metabolica può coesistere con quella da virus indotta in pazienti infetti da genotipo 3, ma con problematiche metaboliche. Queste “forme miste” migliorano solo parzialmente dopo la terapia antivirale se non si associano opportuni provvedimenti tesi a ridurre i fattori di alterazione metabolica. Steatosi: influenza sulla storia naturale dell’epatite C Certamente uno dei quesiti più importanti ai quali rispondere è quanto la presenza di steatosi possa influire sulla storia naturale delle epatopatie HCV correlate23,24. La steatosi di per sè ha un andamento sostanzialmente benigno (tabella 4), mentre la storia naturale della epatopatia HCV ad essa correlata ha un andamento, ormai, sufficientemente definito e così caratterizzato: evoluzione a cirrosi compensata dal 20 al 33% in circa 20 anni, successiva evoluzione ad epatocarcinoma (HCC) in percentuali che variano dall’1,4 al 3,3% anno, a scompenso in circa 3,6-6% anno, e morte in percentuali variabili dal 2,6 al 4% anno25,26. Tabella 4. - Steatosi non alcolica (NAFLD) e steatoepatite non alcolica (NASH): caratteristiche isto-patologiche. Tipo 1 Semplice steatosi Tipo 2 Steatosi con infiammazione lobulare (probabilmente benigna) Tipo 3 Steatosi, infiammazione lobulare, degenerazione balloniforme (NASH senza fibrosi – potenziale progressione a cirrosi) Tipo 4 Steatosi, degenerazione balloniforme, corpi di Mallory, fibrosi (NASH con fibrosi – possibile progressione a cirrosi/HCC) La considerazione che solo circa il 30% dei soggetti con epatite C in circa 20 anni progredisce a cirrosi, che una percentuale elevata progredirà nel suo percorso molto più lentamente ed addirittura una quota parte consistente di pazienti per numerosi decenni non svilupperà nemmeno fibrosi, suggerisce che altri fattori, in particolare nel nostro caso la steatosi (tabella 5), in aggiunta al virus favoriscano quello che è il momento di maggiore importanza e cioè la comparsa e successivamente l’accelerata progressione della fibrosi, evento che peraltro non sempre trova una precisa correlazione con i fenomeni infiammatori27,28. I dati pubblicati sulla correlazione steatosi-fibrosi e, quindi, sulla sua influenza sulla storia naturale della epatite C, hanno numerose limitazioni che possono far comprendere le discrepanze fra gli studi (tabella 6 a pagina seguente): – la maggior parte delle esperienze sono fondate su cross-sectional studies o sono retrospettive, – sono stati utilizzati differenti criteri istologici, – alcune casistiche sono costituite da un numero non adeguato di casi, – le popolazioni studiate sono differenti in relazione ai fattori di rischio, – la distribuzione dei vari genotipi varia nelle varie regioni sedi degli studi, – non sempre tutti i fattori favorenti la steatosi sono stati valutati (uno di questi è l’uso di alcol), – l’analisi multivariata non è sempre utilizzata. 625 G. Testino: Steatosi correlata ad epatite C Tabella 5. - Fattori che possono determinare progressione della patologia epatica in corso di epatite HCV correlata. Fattori virali Genotipo (?) Quasispecie (?) Mutazione T cell epitopes (?) Fattori dell’ospite Età al momento dell’infezione (+) Durata dell’infezione (++) Sesso (+) Razza (+) Patologie epatiche associate (per es. emocromatosi) (+) Diabete (++) Sovrappeso/ Obesità (+++) Steatosi (+++) Sindrome metabolica (+++) Altri fattori (HLA, polimorfismo citochine …) (+) Fattori esterni Alcool (+++) Stile alimentare (++) Fumo (+) Coinfezioni (HIV, HBV …) (+++) STEATOSI-FIBROSI Nonostante tutte queste limitazioni, è bene ricordare come fra i fattori favorenti la fibrosi, la steatosi sia considerata da molti un fattore di rischio indipendente29. Molti studi retrospettivi hanno dimostrato un link fra la severità della steatosi e lo stage della fibrosi valutata su un singolo prelievo bioptico. Questo link normalmente persiste attraverso l’analisi multivariata. In particolare, in pazienti non trattati per epatite HCV e studiati attraverso materiale bioptico rivalutato dopo 4 anni di intervallo, è stato dimostrato come la steatosi di per sè aggravi la fibrosi, ma soprattutto come l’aggravamento della steatosi comporti l’aggravamento della fibrosi. Altri studi invece hanno dimostrato una associazione steatosi/ progressione della fibrosi soprattutto nel genotipo 3a, ma nonostante in corso di infezione da genotipo 3 la steatosi possa essere maggiormente severa, non sempre in questa condizione è stata trovata una stretta correlazione con la fibrosi. Gli Autori sostengono che tale fenomeno possa dipendere da un errore di tipo beta, da differenti criteri di arruolamento o da altri non bene identificati fattori, quali la dieta od un particolare substrato genetico30. È opportuno, quindi, sottolineare come nessun studio distingua chiaramente i pazienti con pura steatosi virale da quelli con pura steatosi metabolica. È possibile, dunque, che le due forme di steatosi siano sinergiche e che la differente proporzione di pazienti con forme virali e metaboliche possa spiegare le discrepanze fra i vari studi. Nello studio di Cholet et al.31 emerge come la presenza di steatosi sia associata in modo statisticamente significativo ad una componente fibrotica maggiormente severa e come l’analisi multivariata evidenzi la steatosi (in associazione alla durata della patologia ed al genotipo 3) quale parametro indipendente associato alla fibrosi severa. Comunque, la migliore evidenza che la steatosi svolge un ruolo nella insorgenza e successivamente nella progressione della fibrosi HCV correlata è fondata sul fatto che la riduzione di peso in corso di epatite HCV conduce non solo ad un decremento della steatosi e ad un miglioramento dei parametri laboratoristici, ma anche ad un miglioramento della fibrosi, nonostante la persistenza del virus e soprattutto indipendentemente dal genotipo32,33. Alcuni Autori dimostrano, infatti, come il grado di steatosi influenzi in modo significativo il grado di fibrosi indipendentemente dal genotipo; altresì, dimostrano come anche la BMI correli con la steatosi sempre indipendentemente dal genotipo34. Più recentemente, la valutazione dei fattori istologici in corso di HCV che possono essere utilizzati per effettuare una predizione di progressione della fibrosi ha dimostrato alcuni parametri con valenza statisticamente significativa. Tabella 6. - Correlazione fra la presenza di steatosi con il grado e lo stage della epatite HCV correlata. Mihm et al. (1997) Czaja et al. (1998) Rubbia et al. (1999) Adinolfi et al. (2001) Serfaty et al. (2001) Monto et al. (2002) Westin et al. (2002) Poynard et al. (2003) Castera et al. (2003) Asselah et al. (2003) Rubbia et al. (2003) Cholet et al. (2004) Clouston et al. (2005) Casistica Valutazione Istologica Analisi Infiammazione Fibrosi 85 60 70 180 100 297 98 1428 96 290 755 314 148 Knodell Knodell/Scheuer Knodell Knodell/Scheuer Knodell Ludwig Ishak Metavir Metavir Metavir Metavir Metavir Scheuer Univariata Univariata Multivariata Multivariata Multivariata Multivariata Multivariata Multivariata Multivariata Multivariata Multivariata Multivariata Multivariata Sì No Sì (p<0001) Sì (p<0.007) No No Si No No Sì (p<0.001) No No Sì Sì No Sì (p<0.02) Sì (p<0.001) Sì (p<0.008) No Si Sì (p<0.007) Sì (p<0.03) No Sì (p<0.001) Sì (p<0.049) Sì 626 Recenti Progressi in Medicina, 96, 12, 2005 Essi sono: l’infiammazione lobulare, la steatosi, ma soprattutto il grado di fibrosi basale35: quindi, se il marker più consistente di progressione è questo, bassi valori di tale marker in pazienti con una lunga storia di infezione probabilmente indicheranno un percorso benigno: ciò fa comprendere come il decorso clinico della patologia possa essere determinato in una fase iniziale e come i fattori genetici possano svolgere un ruolo chiave nel regolare i complessi meccanismi patogenetici che compaiono per il rapporto steatosi/ HCV36. Relativamente al quadro di fibrosi in corso di associazione epatite C/steatosi è stato rilevato come sia simile a quello osservato in corso di steatosi non alcolica isolata36. Si può evidenziare, infatti, come37 nei casi di steatosi correlati ad HCV la steatosi si associ a fibrosi subsinusoidale in modo statisticamente significativo e ad incremento della BMI. È bene precisare come permanga una associazione fra la fibrosi subsinusoidale (figura 3) e la steatosi attraverso l’ analisi multivariata. Non emerge alcuna associazione fra il grado della steatosi e la BMI con lo spessore della fibrosi perivenulare, mentre la fibrosi subsinusoidale, ma soprattutto quella perivenulare, si correlano in modo significativo a fibrosi portale (figura 4). In corso di associazione steatosi/ HCV si assiste ad un arresto replicativo degli epatociti determinato dai due fattori anche indipendentemente. Ciò comporta l’attivazione di cellule epatiche progenitrici (cellule ovali) con conseguente reazione duttulare periportale. L’epitelio duttulare può esprimere TGF-beta, MCP-1, PDGF, con conseguente attivazione delle cellule stellate e promozione della fibrogenesi portale38. Nonostante l’associazione fra la steatosi e la fibrosi perisinusoidale, non è stata trovata alcuna associazione significativa fra il grado di steatosi e la espressione dell’ alpha-SMA staining; tale colorazione invece correla con la fibrosi e la infiammazione portale37. Questo dato conferma come il meccanismo di fibrosi in HCV-associated steatosis necessiti di un primo hit che riconosciamo nella steatosi ed un secondo hit per la progressione ad infiammazione/fibrosi od in modo predominante a fibrosi2. Il secondo hit può essere riconosciuto in una anormalità intraepatica che si sviluppa come risposta al primo hit oppure si presenta indipendentemente come nei casi associati ad HCV. In tali condizioni il secondo insulto può essere riconosciuto nella risposta infiammatoria antivirale o in una azione diretta del virus nel creare stress ossidativi (l’HCV core protein, infatti, può indurre stress ossidativi direttamente attraverso alterazioni in corrispondenza del trasporto di elettroni in sede mitocondriale con conseguente liberazione di ROS, citochine pro-infiammatorie e pro-fibrotiche, figura 2). Tutto favorito dal fatto che nel fegato steatosico è certamente presente un maggiore pool di substrato per fenomeni legati allo stress ossidativo e conseguente lipoperossidazione lipidica38-43. Figura 3. Fibrosi subsinusoidale – steatosi (colorazione tricromica). [Gentilmente concessa dal prof. GL Ravetti e dalla prof. R Gentile – UOC Istopatologia, Ospedale San Martino, Genova]. Figura 4. Fibrosi portale: spazio portale allargato in corso di epatite HCV correlata (colorazione tricromica). [Gentilmente concessa dal prof. GL Ravetti e dalla prof. R Gentile - UOC Istopatologia, Ospedale San Martino, Genova]. Da questi meccanismi si evince come non sempre vi sia una associazione steatosi/ infiammazione: viene evidenziata la possibilità di meccanismi non mediati dalla infiammazione per la insorgenza di fibrosi secondaria. G. Testino: Steatosi correlata ad epatite C È ben noto come una di queste possibilità possa essere legata alla lipoperossidazione lipidica che comporta una diretta stimolazione delle cellule stellate con successiva modificazione del fenotipo44-48; altresì è noto un ruolo della HCV core protein nel creare direttamente “stress ossidativo”, favorendo direttamente la fibrogenesi ed alterazioni al materiale genetico senza infiammazione (v. schema in figura 2). Nell’affrontare il ruolo della steatosi nel favorire la progressione della fibrosi non si può trascurare l’ importante esperienza di Adinolfi49: in tale lavoro, infatti, è dimostrato come la steatosi, ed in particolare quella con gradi elevati, abbia – in corso di epatite HCV – un ruolo clinico rilevante nell’accelerare la progressione della epatopatia, aiutando, quindi, ad identificare il gruppo con l’associazione fegato grasso/epatite C come un “gruppo maggiormente a rischio” nell’evolvere verso la cirrosi. Emerge come pazienti con grado 3-4 di steatosi abbiano un indice annuale di progressione della fibrosi significativamente maggiore rispetto a quello osservata per pazienti con steatosi di grado 1-2 o quelli senza steatosi49. Infine, è da ricordare il rapporto peggioramento della steatosi/progressione della fibrosi. In particolare, il peggioramento della steatosi appare nello studio di Castera et al. come unico fattore indipendente di progressione (utilizzando l’analisi multivariata50). Steatosi, HCV, epatocarcinoma Un altro dato da considerare è l’aumentato rischio per l’insorgenza di HCC in corso di associazione steatosi/ HCV. Innanzitutto è nota la capacità dell’HCV di modulare, attraverso la core protein in particolare, la transcrizione genica, la proliferazione cellulare e la morte cellulare e come tutto ciò possa favorire la cancerogenesi epatica51-53. È altresì noto come iperplasia epatocitaria sia stata descritta in ob/ob mice con steatosi epatica e come la IR sia un altro meccanismo in grado di influenzare la cancerogenesi13. L’ iperproduzione di stress ossidativi e di ROS svolge un ruolo centrale nella progressione sia della epatite che della NASH: in un modello animale di infezione da HCV, i ROS sono iperprodotti in sede epatica indipendentemente dalla infiammazione, contribuendo almeno in parte ai meccanismi di cancerogenesi16. È stato dimostrato come l’incremento dei ROS derivi da un disordine funzionale della catena respiratoria indotto soprattutto dalla core protein54 (figura 2). Ohata et al.55 hanno ben dimostrato come in corso di epatite HCV correlata, l’incidenza cumulativa di HCC in pazienti con steatosi sia significativamente maggiore rispetto a quelli senza. Tale rilievo suggerisce come in questi pazienti sia necessaria una più attenta sorveglianza, per mezzo di controlli laboratoristico-strumentali maggiormente ravvicinati. 627 Steatosi, HCV, terapia antivirale La steatosi induce un meccanismo di resistenza al trattamento con interferone – interferoni peghilati in associazione o meno alla ribavirina – riducendo la possibilità di ottenere una risposta virologica sostenuta21,56: si ipotizza che il meccanismo per mezzo del quale la steatosi induce resistenza alla terapia possa essere di tipo indiretto attraverso l’incremento della severità della fibrosi, e di tipo diretto attraverso alterazioni del metabolismo epatico relativamente ai farmaci antivirali57. Già nell’analisi di Poynard58 veniva confermato come in caso di genotipo 3 la terapia antivirale determinasse parallelamente la riduzione di steatosi in associazione a buone risposte alla terapia, mentre negli altri genotipi ed in particolare nel genotipo 1 vi fosse una ridotta risposta alla terapia. Il “meccanismo di resistenza” è, quindi, maggiormente specifico per la steatosi metabolica, pur essendo presente, anche se in misura minore, in corso di steatosi virale. Peraltro, tali risultati negativi permangono anche quando la terapia viene prescritta attraverso un adeguato dosaggio in relazione al peso corporeo (indipendentemente dalla carica virale). È stato dimostrato, inoltre, come insieme al genotipo 1 ed all’età, la steatosi rappresenti un predittore significativo di risposta virologica precoce. In particolare, l’incremento di steatosi dell’1% comporta un declino nella “probabilità predetta” di una risposta precoce17. Considerando che l’epatopatia HCV correlata rappresenta una delle cause maggiori di trapianto di fegato e che è riconosciuto universalmente come la reinfezione si presenti nella totalità dei casi [con la comparsa di cirrosi colestatica nel 5% dei casi a 6 mesi e di epatopatia avanzata nel 30-40% a 5 anni] e considerando, inoltre, che il picco di forme HCV correlate verrà raggiunto fra il 2010 ed il 2015 con un incremento della necessità di trapianto del 500% circa, si comprende come sia sempre più necessario salvaguardare gli organi allocati in pazienti affetti da HCV (sono i casi in cui alcune scuole cominciano a mettere in discussione il ritrapianto). Per queste ragioni la tematica steatosi/ HCV acquisisce grande importanza anche nella gestione nel post-trapianto. Ad oggi ci sono pochi dati per definire la storia naturale ed i fattori di rischio associati per l’insorgenza di steatosi nel graft in pazienti HCV59,60. Altresì non vi sono dati per meglio definire la eventuale correlazione fra la steatosi del graft e la gravità della recidiva. È stato rilevato da alcuni Autori come la gravità di recidiva di HCV non sia associata alla presenza ed al grado di steatosi, perlomeno in pazienti con genotipo non-3, entro il primo anno dal trapianto di fegato. 628 Recenti Progressi in Medicina, 96, 12, 2005 Una elevata incidenza di steatosi nel graft la si può rilevare dopo circa 4 mesi61: è opportuno però evidenziare una incidenza simile anche in graft di soggetti sottoposti a trapianto per problematiche non C correlate. Tale riscontro suggerisce come la presenza di steatosi sia un evento comune nel post-trapianto, legato a numerosi fattori, indipendentemente da una possibile concomitante infezione da HCV (genotipo non-3)62, 63. La steatosi a 12 mesi ha trovato una sua correlazione con la BMI, ma, a differenza di quanto accade nei casi non correlati al trapianto, nessuna correlazione è emersa con la carica virale, il quadro necro-infiammatorio e fibrotico61. Il capitolo sulla possibile influenza della steatosi sul decorso e sulla risposta alla terapia antivirale post-trapianto è aperto e la letteratura è abbastanza povera al riguardo. È noto come numerosi fattori, ed a vari livelli, possano influenzare sia la storia naturale che la risposta al trattamento59,60. I risultati preliminari della esperienza personale (28 pazienti con recidiva da genotipo 1 trattati con PEG-interferone e ribavirina fra i 4 ed i 12 mesi dal trapianto) evidenziano alcune considerazioni: – una correlazione fra steatosi/ BMI/ incremento dei trigliceridi (nessuna correlazione con i livelli del colesterolo), – la percentuale di steatosi influisce negativamente sulla risposta virologica sostenuta, ma anche sulla risposta biochimica sostenuta, – il parametro che in misura maggiore influenza negativamente la risposta alla terapia antivirale rimane la BMI (figura 5). Emerge, pertanto, come per ottenere il massimo di probabilità di successo nel trattamento delle epatopatie HCV correlate, sia mandataria una migliore interazione dell’epatologo con l’istopatologo nella valutazione di parametri – quali la steatosi – sino a poco tempo fa sottovalutati. Steatosi/HCV: gestione terapeutica Alla luce dei dati esposti, che dimostrano come la steatosi acceleri la progressione della infezione HCV correlata e riduca la risposta alla terapia antivirale standard, la gestione clinica della sottostante steatosi non alcolica/steatoepatite non alcolica (NAFLD/NASH) è essenziale per addivenire ad un trattamento ottimale della epatopatia HCV correlata anche in termini di prevenzione del carcinoma epatocellulare66 (tabella 7). Tabella 7. - Opzioni terapeutiche. Trattamento della insulino resistenza Attività fisica Riduzione del peso Incremento della sensitività insulinica – Metformina – Thiazolidinedione Trattamento della dislipidemia Trattamento del sovraccarico di ferro Trattamento con acido ursodesossicolico Trattamento dello stress ossidativo Vitamina E Betaina SAMe N-Acetylcysteina Silimarina RIDUZIONE DEL PESO Sebbene su tale argomento vi siano risultanze contradditorie, vi sono evidenze che affermano come l’insulino resistenza sia migliorata dalla riduzione del peso. Si assiste, infatti, ad una riduzione della ossidazione lipidica con consensuale incremento dell’utilizzazione del glucosio. Inoltre, un moderato miglioramento ottenuto a lungo termine in soggetti in sovrappeso, ma soprattutto obesi, favorisce una migliore sensitività all’insulina ed una migliore tolleranza glucidica, che si traduce in un miglioramento o normalizzazione della funzionalità epatica67. MIGLIORAMENTO DELLA SENSITIVITÀ INSULINICA Metformina Figura 5. Correlazione fra BMI, percentuale di steatosi e livelli di trigliceridi con la la risposta alla terapia antivirale (SBR: risposta biochimica sostenuta, SVR: risposta virologica sostenuta) (Testino G, Sumberaz A, 2005) Alcune evidenze – anche recenti – hanno rilevato un miglioramento di alcuni parametri istologici in corso di epatopatie, tuttavia ad oggi non vi sono ancora elementi certi e definitivi68. Nair et al.69 hanno documentato un miglioramento soltanto transitorio della funzionalità epatica senza nessuna significativa riduzione della IR. G. Testino: Steatosi correlata ad epatite C Inoltre, sono stati evidenziati casi di epatotossicità e rischio di acidosi lattica in soggetti con patologia epatica avanzata e Nammour et al.70 hanno segnalato casi di epatite colestatica. Ad oggi, quindi, la metformina non può ancora essere raccomandata nei casi di NAFLD/NASH autonomi o associati a patologia virale sino a che non siano presentati risultati di studi randomizzati e controllati. Thiazolidinedione Tali molecole (troglitazone, rosiglitazone, pioglitazone) attivano il PPAR-gamma, un recettore nucleare espresso nel tessuto adiposo, e favoriscono il mantenimento di una normale sensitività insulinica. L’attivazione del PPAR-gamma riduce il rilascio di FFAs e di TNF-alfa dagli adipociti68. Tuttavia, il troglitazione, il rosiglitazione e il pioglitazione possono provocare grave epatotossicità71-74, così da non renderne praticabile l’impiego. TRATTAMENTO DELLA IPERLIPIDEMIA L’uso di clofibrato per 12 mesi non ha comportato un significativo risultato né dal punto di vista istologico, né dal punto di vista biochimico75. Invece, l’uso di gemfibrozil ad un dosaggio di 600 mg/die ha indotto un importante miglioramento non solo dei livelli di trigliceridi, ma anche degli enzimi epatici76. È acquisito che il gemfibrozil inibisce la mobilizzazione di acidi grassi dal tessuto adiposo ed incrementa la clearance delle VLDL. In letteratura non sono presenti studi ben definiti sull’utilizzo delle statine in corso di NAFLD/ NASH. Recentemente è stato segnalato come in soggetti con steatosi epatica non alcolica vi sia stata una riduzione delle transaminasi; un miglioramento ultrasonografico in soggetti con ipertrigliceridemia utilizzando omega-3; in soggetti con ipercolesterolomia utilizzando atorvastatina ed in soggetti in sovrappeso utilizzando orlistat77. Acido ursodesossicolico Laurin et al. hanno rilevato come l’impiego di acido ursodessosicolico (UDCA) (13-15 mg/kg/die) per 12 mesi in soggetti con NASH abbia comportato un significativo miglioramento sia dal punto di vista istologico che laboratoristico75. In altri due studi, l’associazione terapia nutrizionale con UDCA ha comportato risultati ancora migliori. Attualmente comunque sono in corso studi a lungo termine per quanto riguarda l’uso dell’UDCA sia in monoterapia sia in associazione con la vitamina E. TRATTAMENTO DELLO STRESS OSSIDATIVO Il tentativo di agire a questo livello in corso di NAFLD/ NASH può rappresentare un importante ausilio e ciò anche in corso di epatite HCV correlata. 629 Alcune componenti del virus ed in particolare la core-protein agiscono direttamente a tale livello in modo sinegico (figura 2). Alpha-tocoferolo La vitamina E rappresenta un potente scavenger di radicali liberi nell’ambito delle membrane biologiche. Dosaggi di tale vitamina da 400 a 1200 IU/die hanno migliorato gli enzimi epatici in 11 bambini con diagnosi clinica di NASH. Tuttavia, non sono stati rilevati miglioramenti ecografici e alla sospensione del trattamento si è assistito ad un nuovo incremento delle transaminasi78. Hasegawa et al.79 hanno dimostrato una riduzione delle transaminasi in associazione ad una riduzione del TGFB1. Questa osservazione conferma il link fra i radicali liberi dell’ossigeno, l’attivazione di citochine e la fibrogenesi. È bene precisare comunque come l’effetto benefico della vitamina E debba essere ricercato nell’associazione con altre molecole anti-ossidanti80. Betaine Sono trimetil- amino acidi che derivano sia dalla colina che dalla dieta. Tali molecole sono importanti donatrici di metili ed inoltre la fosfatidilcolina è un importante componente delle VLDL. Da parte di tali sostanze è stata dimostrata una riduzione della fibrosi indotta su modelli animali per attivazione della collagenasi68. Attualmente lo studio di tale molecola è stato effettuato su casistiche ridotte, per cui ad oggi dal punto di vista clinico non possono essere formulati giudizi definitivi. Silibina L’associazione della silibina con vitamina E e fosfolipidi per potenziarne l’assorbimento intestinale e l’effetto anti-ossidante sembra essere particolarmente promettente. In realtà, è noto come tale molecola possa agire non solo attraverso proprietà antiossidanti, ma anche attraverso altri meccanismi 81-84 (tabella 8 a pagina seguente). Alcuni Autori hanno rilevato come la silibina sia un importante scavenger di radicali liberi e stimolante la produzione di SOD e GSH e conseguente riduzione della lipoperossidazione lipidica. Inoltre, è stata dimostrata una sua notevole azione nel ridurre in modo significativo l’ IR82-84. A livello sperimentale è stato di recente provato come la silibina possa avere una azione anti-fibrotica ed anti-infiammatoria attraverso l’espressione del TNF-beta 1 e la stabilizzazione delle mast cells85,86. È stata suggerita un’azione anti-fibrotica anche in pazienti con epatite cronica HCV correlata. 630 Recenti Progressi in Medicina, 96, 12, 2005 Bibliografia Tabella 8. - Effetti ad oggi conosciuti della silibina. – – – – – – – – – – – – – Azione antiossidante e inibizione della lipoperossidazione lipidica Inibizione della fibrogenesi Inibizione dei meccanismi infiammatori Miglioramento della insulino-resistenza Inibizione dell’attivazione NF- kB e IKK beta Regolazione della sintesi di RNA, DNA, proteine Regolazione della permeabilità cellulare Inibizione dei danni mitocondriali Immunomodulazione Inibizione dell’attività della P450 Inibizione della produzione di TNF alpha da parte delle cellule di Kupffer Aumento del contenuto intracellulare in linfociti attivati Induzione di apoptosi Inoltre, Katiyar et al.87 hanno dimostrato un azione di anti-cancerogenesi attraverso l’induzione di apoptosi. Tale meccanismo sarebbe p53 dipendente e mediato attraverso l’attivazione della capsasi-386. Da questi dati può essere ipotizzato, in caso di steatosi/ HCV, un importante ruolo di questa molecola anche in corso di terapia antivirale, ovviamente in associazione alle misure necessarie nel contenere i vari aspetti della sindrome metabolica. Per suffragare tale indicazione è opportuno sottolineare ciò che affermano Mahmood et al.88 e cioè che la terapia anti-ossidante in combinazione con quella antivirale può ridurre il danno epatico e prevenire il possibile sviluppo di epatocarcinoma. Conclusioni e prospettive 1. L’associazione epatite C e steatosi riveste un ruolo clinico rilevante. 2. È mandatario affrontare la complessa problematica degli eventuali squilibri metabolici, associando alla terapia antivirale presidî terapeutici vs la patogenesi dei vari meccanismi di stress ossidativo (che possono essere indipendenti da quelli infiammatori). 3. In tal modo si potrà pervenire ad un approccio terapeutico integrato e personalizzato, idoneo a produrre vantaggi di ordine istopatologico ed un controllo clinico più adeguato. 1. Brunt EM, Tiniakos DG. Steatosis, steatohepatitis: review of effects on chronic hepatitis C. Current Hepatitis Reports 2002; 1: 38-44. 2. Lonardo A, Adinolfi LE, Loria P, Carulli N, Ruggiero G, Day CP. Steatosis and hepatitis C virus: mechanisms and significance for hepatic and extrahepatic disease. Gastroenterology 2004; 126: 586-97. 3. Castera L, Chouteau P, Hezode C, Zafrani ES, Dhumeaux D, Pawlotsky JM. Hepatitis C virus-induced hepatocellular steatosis. Am J Gastroenterol 2005; 100: 711-15. 4. Loguercio C, De Girolamo V, De Sio I, Tucillo C, Ascione A, Baldi F. Non-alcoholic fatty liver disease in an area of Southern Italy: main clinical, histological and pathophysiological aspects. J Hepatol 2001; 35: 568-74. 5. Rubbia-Brandt L, Fabris P, Paganin S, Leandro G, Male PJ, Giostra E, Parlotto A, Bozzola L, Smedile A, Negro F. Steatosis affects chronic hepatitis C progression in a genotype specific way. Gut 2004; 53: 406-12. 6. Solis-Herruzo JA, Perez-Carreras M, Rivas E, Fernandez-Vazquez I, Garfia C, Bernardos E, Castellano G, Colina F. Factors associated with the presence of nonalcoholic steatohepatitis in patients with chronic hepatitis C. Am J Gastroenterol 2005; 100: 1091-98. 7. Liu CJ, Jeng YM, Chen PJ, Lai MY, Yang HC, Huang WL, Kao JH, Chen DS. Influence of metabolic syndrome, viral genotype and antiviral therapy on superimposed fatty liver disease in chronic hepatitis C. Antiviral Therapy 2005; 10: 405-15. 8. Hezode C, Roudot-Thoraval F, Zafrani ES, Dhumeaux D, Pawlotsky JM. Different mechanisms of steatosis in hepatitis C virus genotypes 1 and 3 infections. J of Viral Hepatitis 2004; 11: 455-58. 9. Asselah T, Boyer N, Marcellin P. Steatosis in hepatitis C : what does it mean ? Current Hepatitis Reports 2003; 2: 137-44. 10. Sanyal AJ, Contos MJ, Sterling RK, Luketic VA, Shiffman ML, Stravitz T, Mills S. Nonalcoholic fatty liver disease in patients with hepatitis C is associated of the metabolic syndrome. Am J Gastroenterol 2003; 98: 2064-71. 11. Diehl AM, Li ZP, Lin HZ, Yang SQ. Cytokines and the pathogenesis of non-alcoholic steatohepatitis. Gut 2005; 54: 303-06. 12. Kaser S, Moschen A, Cayon A, Kaser A, Crespo J, Pons-Romero F, Ebenbichler CF, Patsch JR, Tilg H. Adiponectin and its receptors in non-alcoholic steatohepatitis. Gut 2005; 54: 117-21. 13. Koike K, Moriya K. Metabolic aspects of hepatitis C viral infection: steatohepatitis resembling but distinct from NASH. J Gastroenterol 2005; 40: 329-36. 14. Fartoux L, Poujol-Robert A, Guechot J, Wendum D, Poupon R, Serfaty L. Insulin resistance is a cause of steatosis and fibrosis progression in chronic hepatitis C. Gut 2005; 54: 1003-08. 15. Aytug S, Reich D, Sapiro LE, Bernstein D, Begum N. Impaired IRS-1/P13-kinase signaling in patients with HCV: a mechanism for increased prevalence of type 2 diabetes. Hepatology 2003; 38: 1384-92. 16. Castera L, Hezode C, Roudot-Thoraval F, Lonjon I, Zafrani ES, Pawlotsky JM, Dhumeaux D. Effect of antiviral treatment on evolution of liver steatosis in patients with chronic hepatitis C: indirect evidence of a role of hepatitis C virus genotype 3 in steatosis. Gut 2004; 53: 420-24. G. Testino: Steatosi correlata ad epatite C 17. Patton HM, Patel K, Behling C, Bylund D, Blatt LM, Vallee M, Heaton S, Conrad A, Pockros PJ, McHutchinson JG. The impact of steatosis on disease progression and early and sustained treatment response in chronic hepatitis C patients. J Hepatol 2004; 40: 484-90. 18. Kumar D, Farrell GC, Fung C, George J. Hepatitis C virus genotype 3 is cytopathic to hepatocytes: reversal of hepatic steatosis after sustained therapeutic response. Hepatology 2002; 36: 1266-72. 19. Rubbia-Brandt L, Quadri R, Abid K, Giostra E, Male PJ, Mentha G, Spahr L, Zarski JP, Borisch B, Hadengue A, Negro F. J Hepatol 2000; 33: 106-15. 20. Perlemuter G, Sabile A, Letteron P, Vona G, Topico A, Chretien Y, Koike K, Pessayre D, Chapman J, Barba G, Brechot C. Hepatitis C virus core protein inhibits microsomal triglyceride transfer protein activity and very low density lipoprotein secretion: a model of viral-related steatosis. FASEB J 2002; 16: 185-94. 21. Ramesh S, Sanyal AJ. Hepatitis C and nonalcoholic fatty liver disease. Seminars in Liver Disease 2004; 24: 399-413. 22. Hezode C, Roudot-Thoraval F, Zafrani ES. Different mechanisms of steatosis in hepatitis C virus genotypes 1 and 3 infections. J Viral Hepat 2004; 11: 455-8. 23. Angulo P. Nonalcoholic fatty liver disease. N Engl J Med 2002; 346: 1221-31. 24. Brunt EM. Nonalcoholic steatohepatitis. Seminars in Liver Disease 2004; 24: 1-19. 25. Alberti A, Chemello L, Benvegnù L. Natural history of hepatitis C. J Hepatol 1999; 31: 17-24. 26. Everson GT. Treatment of chronic hepatitis C in patients with decompensated cirrhosis. Reviews in Gastroenterological Disorders 2004; 4: S31-S38. 27. Afdhal NH. The natural history of hepatitis C. Seminars in Liver Disease 2004; 24: 3-8. 28. Poynard T. Treatment of cirrhotic patients in the pegylated interferon era. Dig Liv Dis 2004; 36 (Suppl 3): S344-S348. 29. Pinzani M, Rombouts K. Liver fibrosis: from the bench to clinical targets. Dig Liv Dis 2004; 36: 231242. 30. Fabris P, Floreani A, Carlotto A, Giordani MT, Baldo V, Stecca C, Marchioro L, Tramarin A, Bertin T, Negro F, de Lalla F. Alcohol is an important co-factor for both steatosis and fibrosis in Northern Italian patients with chronic hepatitis C. J Hepatol 2004; 41: 644-51. 31. Cholet F, Nousbaum JP, Richecoeur M, Oger E, Cauvin JM, Lagarde N, Robaszkiewicz M, Gouerou H. Gastroenterol Clin Biol 2004; 28: 272-8. 32. Takato U, Sugawara H, Sujaku K, Hashimoto O, Tsuji R, Tamaki S, Torimura T, Inuzuka S, Sata M, Tanikawa K. Therapeutic effects of restricted diet and exercise in obese patients with fatty liver. J Hepatol 1997; 27: 103-7. 33. Hickman IJ, Clouston AD, Macdonald GA, Purdie DM, Prins JB, Ash S, Jonsson JR, Powell EE. Effect of weight reduction on liver histology and biochemistry in patients with chronic hepatitis C. Gut 2002; 51: 89-94. 34. Hickman IJ, Powell EE, Prins JB, Clouston AD, Ash S, Purdie DM, Jonsson JR. In overweight patients with chronic hepatitis C, circulating insulin is associated with hepatic fibrosis: implications for therapy. J Hepatol 2003; 39: 1042-48. 35. Collier JD, Woodall T, Wight DGD, Shore S, Gimson AE, Alexander JM. Predicting progressive hepatic fibrosis stage on subsequent liver biopsy in chronic hepatitis C virus infection. J Viral Hepatitis 2005; 12: 74-80. 631 36. Farrell GC, George J, McCullough AJ. Fatty liver disease – NASH and related disorders. Blackwell Publishing, Oxford: 2005. 37. Clouston AD, Jonsson JR, Purdie DM, Macdonald GA, Pandeya N, Shorthouse C, Powell EE. Steatosis and chronic hepatitis C: analysis of fibrosis and stellate cell activation. J Hepatol 2001; 34: 314-20. 38. Clouston AD, Powell EE, Walsh MJ, Richardson MM, Demetris AJ, Jonsson JR. Fibrosis correlates with ductular reaction in hepatitis C: roles of impaired replication, progenitor cells and steatosis. Hepatology 2005; 41: 809-818. 39. Kitase A, Hino K, Furutani T, Okuda M, Gondo T, Hidaka I, Hara Y, Yamaguchi Y, Okita K. In situ detection of oxidized n-3 polynsaturated fatty acids in chronic hepatitis C: correlation with hepatic steatosis. J Gastroenterol 2005; 40: 617-24. 40. Falcon V, Acosta-Rivero N, Shibayama M, Chinea G, Gavilondo JV, de la Rosa MC. HCV core protein localizes in the nuclei of nonparenchimal liver cells from chronically HCV-infected patients. Biochem Biophys Res Commun 2005; 329: 1320-8. 41. Suzuki R, Sakamoto S, Tsutsumi T, Rikimaru A, Tanaka K, Shimoike T. Molecular determinants for subcellular localization of hepatitis C virus core protein. J Virol 2005; 79: 1271-81. 42. Furukawa S, Fujita T, Shimabukuro M, Iwaki M, Yamada Y, Nakajima Y. Increased oxidative stress in obesity and its impact on metabolic syndrome. J Clin Invest 2004; 114: 1752-61. 43. Browning JD, Horton JD. Molecular mediators of hepatic steatosis and liver injury. J Clin Invest 2004; 147: 147-52. 44. Loguercio C, Federico A. Oxidative stress in viral and alcoholic hepatitis. Free Radical Biology and Medicine 2003; 34: 1-10. 45. Higuchi H, Gores GJ. Mechanisms of liver injury: an overview. Current Molecular Medicine 2003; 3: 483-90. 46. Okuda M, Li K, Beard MR, Showalter LA, Scholle F, Lemon SM, Weinman SA. Mitochondrial injury, oxidative stress, and antioxidant gene expression are induced by hepatitis C virus core protein. Gastroenterology 2002; 122: 366-75. 47. Jaeschke H, Gores GJ, Cederbaum AI, Hinson JA, Pessayre D, Lemaster JJ. Mechanisms of Hepatotoxicity. Toxicological Sciences 2002; 65: 166-76. 48. Pinzani M, Romanelli RG, Magli S. Progression of fibrosis in chronic liver diseases: time to tally the score. J Hepatol 2001; 34: 764-67. 49. Adinolfi LE, Gambardella M, Andreana A, Tripodi MF, Utili R, Ruggiero G. Steatosis accelerates the progression of liver damage of chronic hepatitis C patients and correlates with specific HCV genotype and visceral obesity. Hepatology 2001; 33: 1358-64. 50. Castera L, Hezode C, Roudot-Thoraval, Bastie A, Zafrani ES, Pawlotsky JM, Dhumeaux D. Worsening of steatosis is an independent factor of fibrosis progression in untreated patients with chronic hepatitis C and paired liver biopsies. Gut 2003; 52: 288-92. 51. Zhang LH, Fu Ji J. Molecular profiling of hepatocellular carcinomas by cDNA microarray. World J Gastroenterol 2005; 11: 463-68. 52. Fattowich G, Stroffolini T, Zagni I, Donato F. Hepatocellular carcinoma in cirrhosis: incidence and risk factors. Gastroenterology 2004; 127: S35-S50. 53. Moriya K, Nakagawa K, Santa T, Shintani Y, Fujie H, Miyoshi H. Oxidative stress in the absence of inflammation in a mouse model for hepatitis C virusassociated hepatocarcinogenesis. Carcinogenesis 2001; 61: 4365-70. 632 Recenti Progressi in Medicina, 96, 12, 2005 54. Roskamas T, Yang SQ, Koteish A, Durnez A, DeVos R, Huang X. Oxidative stress and oval cell accumulation in mice and humans with alcoholic and nonalcoholic fatty liver disease. Am J Pathol 2003; 163: 1301-11. 55. Ohata K, Hamasaki K, Toriyama K, Matsumoto K, Saeki A, Yanagi K. Hepatic steatosis is a risk factor for hepatocellular carcinoma in patients with chronic hepatitis C virus infection. Cancer 2003; 97: 3036-43. 56. Harrison SA, Brunt EM, Qazi RA, Oliver DA, Neuschwander-Tetri BA, Di Bisceglie AM, Bacon BR. Effect of significant histologic steatosis or steatohepatitis on response to antiviral therapy in patients with chronic hepatitis C. Clin Gastroenterol Hepatol 2005; 3: 604-9. 57. Ijaz S, Yang W, Winslet MC, Seifalian AM. Impairment of hepatic microcirculation in fatty liver. Microcirculation 2003; 10: 447-56. 58. Poynard T, Ratziu V, McHutchinson J, Manns M, Goodman Z, Zeuzem S, Younossi Z, Albrecht J. Effect of treatment with peginterferon or interferon alfa-2b and ribavirin on steatosis in patients infected with hepatitis C. Hepatology 2003; 38: 75-85. 59. Ferenci P. Predictors of response to therapy for chronic hepatitis C. Seminars in Liver Disease 2004; 24 (Suppl. 2): 25-31. 60. Everson GT. Impact of immunosuppressive therapy on recurrence of hepatitis C. Liver Transpl 2002; 10 (Suppl. 1): S19-S27. 61. Machicao VI, Krishna M, Bonatti H, Aqel BA, Nguyen JH, Weigand SD, Rosser BG, Hughes C, Dickson R. Hepatitis C recurrence is not associated with allograft steatosis within the first year after liver transplantation. Liver Transpl 2004; 10: 599-606. 62. Gisbert C, Prieto M, Berenguer M, Breto M, Carrasco D, de Juan M, Mir J, Berenguer J. Hyperlipidemia in liver transplant recipients: prevalence and risk factors. Liver Transpl Surg 1997; 3: 416-22. 63. Stegall MD, Everson G, Schroter G, Bilir B, Karrer F, Kam I. Metabolic complications after liver transplantation. Transplantation 1995; 15: 1057-60. 64. Ansaldi F, Bruzzone B, Testino G, Bassetti M, Gasparini R, Crovari P, Icardi G. Combination hepatitis C virus antigen and antibody immunoassay as a new tool for early diagnosis of infection. Journal of Viral Hepatitis 2005; in press. 65. Testino G., Icardi G. Hepatocellular carcinoma and Interferon therapy in HCV compensated cirrhosis: evaluation in relation to virological response. Hepato-Gastroenterology 2005; 52: IX. 66. Testino G, Ansaldi F, Andorno E, Ravetti GL, Ferro C, De Iaco F, Icardi GC, Valente U. Interferon therapy does not prevent hepatocellular carcinoma in HCV compensated cirrhosis. Hepato-Gastroenterology 2002; 49: 1636-38. 67. Andy SY, Emmet B, Keeffe EB. Nonalcoholic fatty liver disease. Reviews in Gastroenterological disorders 2002; 2: 11-19. 68. Oneta CM, Dufour JF. Nonalcoholic fatty liver disease: treatment options based on pathogenic considerations. Swiss Med WKLD 2002; 132: 493-505. 69. Nair S, Diehl AM, Wiseman M, Farr GH, Perrillo RP. Metformin in the treatment of non-alcoholic steatohepatitis: a pilot open label trial. Aliment Pharmacol Ther 2004; 20: 23-8. 70. Nammour FE, Fayad NF, Peikin SR. Metformininduced cholestatic hepatitis. Endocr Pract 2003; 9: 307-9. 71. Kohlroser J, Mathai J, Reichheld J, Banner BF, Bonkovsky HL. Hepatotoxicity due to troglitazone: report of two cases and review of adverse events reported to the United States Food and Drug Administration. Am J Gastroenterol 2000; 95: 272-6. 72. Manon KVN, Angulo P, Lindor KD. Severe cholestatic hepatitis from troglitazone in a patient with nonalcoholic steatohepatitis and diabete mellitus. Am J Gastroenterol 2001; 96: 1631-4. 73. Al-Salmar J, Arjomand H, Kemp DG, Mittal M. Hepatocellular injury in a patient receiving rosiglitazone. A case report. Ann Int Med 2000; 132: 121-4. 74. May LD, Lefkowitch JH, Kram MT, Rubin DE. Mixed hepatocellular-cholestatic liver injury after pioglitazone therapy. Ann Int Med 2002; 136: 449-52. 75. Laurin J, Lindor KD, Crippin JS. Ursodeoxycholic acid or clofibrate in the treatment of non-alcohol-induced steatohepatitis: a pilot study. Hepatology 1996; 23: 1464-67. 76. Basaranoglu M, Acbay O, Sonsuz A. A controlled trial of gemfibrozil in the treatment of patients with nonalcoholic steatohepatitis. J Hepatol 1999; 31: 384. 77. Apostolos H, Christos S, Georgia L, Ionnis S, Persefoni H, Anastasios L, Valentini T, Koliouskas D. Efficacy of omega-3 fatty acids, atorvastatin and orlistat in non-alcoholic fatty liver disease with dyslipidemia. Indian J Gastroenterol 2004; 23: 131-134. 78. Lavine JE. Vitamin E treatment of non-alcoholic steatohepatitis in children: a pilot study. J Pediatr 2000; 136: 734-8. 79. Hasegawa T, Yoneda M, Nakamura K. Plasma transforming growth factor-b1 level and efficacy of alpha-tocopherol in patients with non-alcoholic steatohepatitis: a pilot study. Aliment Pharmacol Ther 2001; 15: 1667-72. 80. Lyn P. Nonalcoholic fatty liver disease: relationship to insulin sensitività and oxidative stress. Treatment approaches using vitamin E, magnesium, and betaine. Alternative Medicine Review 2002; 7: 276-291. 81. Pietrangelo A, Borella F, Casalgrandi G, Montorsi G, Ceccarelli D, Gallesi D, Giovannini F, Gasparetto A, Masini A. Antioxidant activity of silybin in vivo durino long-term iron overload in rats. Gastroenterology 1995; 109: 1941-9. 82. Neuman MG, Cameron RG, Haber JA, Katz GG, Malkiewicz IM, Shear NH. Inducers of cytochrome P450 2E1 enhance methotrexate-induced hepatocytoxicity. Clin Biochem 1999; 32: 519-36. 83. Beckmann-Knopp S, Rietbrock S, Weyhenmeyer R, Bocker RH, Beckurts KT, Lang W, Hunz M, Fuhr U. Inhibitory effects of sibilin on cytochrome P-450 enzymes in human liver microsomes. Pharmacol Toxicol 2000; 86: 250-6. 84. Trappoliere M, Federico C, Tuccillo C, de Sio I, Di Leva A, Niosi M, D’Auria M, Loguercio C. Effects of new pharmacological complex (sylibin + vitamin E + phospholipids) on some markers of metabolic syndrome and of a liver fibrosis in patients with non-alcoholic fatty liver disease: a preliminary open pilot study. Minerva Gastroenterol Dietol 2005; 51: 193-9. 85. Jeong DH, Lee GP, Jeong WI, Do SH, Yang HJ, Yuan DW, Kim KJ, Jeong KS. Alterations of mast cells and TGF-beta 1 on the silymarin treatment for CCl(4)-induced hepatic fibrosis. World J Gastroenterol 2005; 28: 1141-8. 86. Katiuyar SK, Roy AM, Baliga MS. Silymarin induces apoptosis primarily through a p53-dependent pathway involving Bcl-2/Bax, cytochrome C release, and capsase activation. Mol Cancer Ther 2005; 4: 207-16. G. Testino: Steatosi correlata ad epatite C 87 Strickland GT, Tanamly MD, Tadros F, Labeeb S, Makld H, Nessim D. Two-year results of a randomized double-blinded trial evaluating silymarin for chronic hepatitis C. Dig Liv Dis 2005; 37: 54243. 88. Mahmood S, Kawanaka M, Kamei A, Izumi A, Nakata K, Njiyama G. Immunohistochemical evaluation of oxidative stress markers in chronic hepatitis C. Antioxidants and Redox Signaling 2004; 6: 19-24. 89. Cammà C, Di Marco V. Long-term course of Interferon-treated chronic hepatitis C. J Hepatol 1998; 28: 531-37. 90. Perasso A, Testino G, Ansaldi F, Venturino V, Icardi GC. Interferon alfa-2b/ Ribavirin and therapy followed by low-dose r-Interferon alfa-2b in chronic hepatitis C Interferon non-responders. Hepatology 1999; 29: 296-97. 91. Testino G, Ansaldi F. Interferon therapy in chronic hepatitis C virus in the prevention of worsening independently of ALT response: is it conceivable? Hepato-Gastroenterology 2001; 48: VIII. 92. Baker DE. Pegylated Interferon plus Ribavirin for the treatment of chronic hepatitis C. Reviews in Gastroenterological Disorders 2003; 3: 93-109. 93. Lee WL, Dienstag JL, Lindsay KL, Lok AS, Bonkovsky HL, Shiffman ML and the HALT-C Trial Group. Evolution of the HALT-C Trial: pegylated interferon as maintenance therapy for chronic hepatitis C in previous interferon nonresponders. Controlled Clinical Trials 2004; 25: 472-92. Indirizzo per la corrispondenza: Prof. Gianni Testino Azienda Ospedaliera San Martino Dipartimento dei Trapianti d’Organo Unità Operativa Dipartimentale Largo Rosanna Benzi, 10 10132 Genova 633 94. Craxi A, Cammà C. Prevention of hepatocellular carcinoma. Clin Liver Dis 2005; 9: 329-46. 95. Marrache F, Consigny Y, Ripault MP, Cazals-Hatem D, Martinot M, Marcellin P. Safety and efficacy of peginterferon plus ribavirin in patients with chronic hepatitis and brindging fibrosis or cirrhosis. J Viral Hepat 2005; 12: 421-8. 96. Powell EE, Jonsson JR, Clouston AD. Steatosis: co-factor in other liver diseases. Hepatology 2005; 42: 5-13. 97. Sumberaz A, Mattioli F, Grossi S, Garbero C, Testino G, Martelli A. DNA fragmentation in human lymphocytes in alcoholic and post-viral cirrhosis. XIV Congresso Nazionale della Società Italiana di Tossicologia, 2006. 98. Koike K. Hepatitis C virus infection can present with metabolic disease by inducing insulin resistance. Intervirology 2006; 49: 51-7. 99. Bataller R, Sancho-Bru P, Gines P, Brenner DA. Liver fibrogenesis. Antioxidant and Redox Signaling 2005; 7: 1346-55. 100. Gasbarrini G, Vero V, Miele L, Greco AC, Gasbarrini A, Greco A. Nonalcoholic fatty liver disease: defining a common problem. Eur Rev Med Pharmacol Sci 2005; 9: 251-2. 101. Trappoliere M, Tuccillo C, Federico A, Coppola F, D’Auria M, Loguercio C. The treatment of NAFDL. Eur Rev Med Pharmacol Sci 2005; 9: 299-304. 102. Melhem A, Stern M, Shibolet O, Zabrecky G, Cohen R, Ilan Y. Treatment of chronic hepatitis C virus infection via antioxidants: results of a phase I clinical trial. J Clin Gastroenterol 2005; 39: 737-42.






![[TRIESTE - 30] IL PICCOLO/CU/2 18/11/09 [TRIESTE - 30] IL PICCOLO/CU/2 18/11/09](http://s1.doczz.it/store/data/000398382_1-1fa9aae65cb1629d6682a48ce643cf6e-70x70.png)
