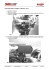Consorzio di Gestione Area Marina Protetta di
Transcript
Consorzio di Gestione Area Marina Protetta di
Consorzio di Gestione Area Marina Protetta di “Tavolara Punta Coda Cavallo” Rapporto finale 2010 Intervento B1 Approvato con DPN‐2010‐0013104 del 14/06/2010 e DPN‐2010‐0013794 del 17/06/2010 Direzione Protezione Natura del Ministero dell’Ambiente, della Tutela del Territorio e del Mare, con cui si approvano gli interventi, investimenti 2010 Monitoraggio dell’effetto riserva (4° annualità) ittico e ricci Consorzio di Gestione Area Marina Protetta Tavolara Punta Coda Cavallo Via Dante, 1 – 07026 – Olbia (SS) Telefono 0789 203013 Fax 0789 204514 e-mail [email protected] Monitoraggio dell’effetto riserva a livello ecosistemico presso l’Area Marina Protetta di Tavolara-Punta Coda Cavallo Relazione tecnica finale 31 Ottobre 2011 Partecipanti Paolo Guidetti – CoNISMa URL Lecce – Responsabile Scientifico Simona Bussotti Antonio Di Franco ______________________________________________________________ Convenzione tra il CoNISMa (Consorzio Nazionale Interuniversitario per le Scienze del Mare-URL Lecce) ed il Consorzio di Gestione dell’Area Marina Protetta di Tavolara-Punta Coda Cavallo. Ringraziamenti Un ringraziamento va al Direttore dell’AMP di Tavolara-Punta Coda Cavallo, Augusto Navone, per aver permesso questa ricerca nell’ambito del piano di gestione, ma anche a tutto lo staff della AMP per il clima positivo in cui il lavoro è stato svolto. Un ringraziamento particolare va a Pieraugusto Panzalis per il suo coinvolgimento nelle attività di visual census ed a Salvatore Vitale per l’aiuto durante le attività di campo e le preziose informazioni sui luoghi messe a disposizione. 2 Indice Introduzione ___________________________________________________ 4 Materiali e metodi ______________________________________________ 13 Risultati ______________________________________________________ 19 Conclusioni ___________________________________________________ 38 Bibliografia ___________________________________________________ 40 Appendice ____________________________________________________ 44 3 1. Introduzione Negli ultimi decenni si è assistito su scala mondiale ad una concentrazione delle popolazioni umane lungo le coste di mari ed oceani. Ciò ha determinato una espansione notevole delle città costiere ed un aumento consistente delle opere a difesa della costa, degli impianti industriali, dell’inquinamento e, in ultima istanza, degli impatti umani in ambiente marino costiero (Chapman & Bulleri, 2003). A ciò si deve aggiungere l’aumento costante della domanda di seafood a livello mondiale, che ha indotto l’industria della pesca ad aumentare il prelievo di risorse di pesca in modo drammatico. Oltre alla pesca industriale, che avviene sottocosta così come in mare aperto, un impatto non trascurabile sulle risorse costiere possono determinarlo la piccola pesca (spesso spinta dalle economie locali, es. il turismo, a prelevare ben oltre il sostenibile), la pesca ricreativa ed una miriade di forme di pesca illegale (es. pesca con gli esplosivi). Queste ultime tipologie di pesca legali ed illegali, in molti paesi sottosviluppati e non, incluso il bacino del Mediterraneo e l’Italia, possono determinare un effetto sommatorio devastante sugli stock ittici locali. Ai problemi sopra esposti non si può ovviamente rispondere con un’unica forma di gestione. Il mutamento dei mercati (es. globalizzazione) e le diverse economie legate alla pesca (da quelle locali a quelle mondiali) necessitano di un approccio integrato tra forme di gestione locali e lo spatial planning su ampia scala, almeno di bacino, per poi arrivare, si spera, ad un controllo del mercato e del consumo globale dei prodotti della pesca. Per quel che concerne la gestione a livello di piccola scala, le Aree Marine Protette (AMP) sono divenute negli ultimi decenni uno degli strumenti più popolari su scala mondiale (Halpern, 2003) finalizzati alla: 1) conservazione degli ecosistemi marini; 2) gestione delle risorse (incluse quelle di pesca) in aree costiere. L’esigenza di istituire AMP (in cui le attività di pesca sono vietate o regolamentate, così come altre attività antropiche a seconda della zonizzazione delle AMP stesse, cioè la suddivisione in subaree caratterizzate da diversi livelli 4 di protezione e misure di gestione) è scaturita dalle crescenti evidenze che lo sfruttamento eccessivo delle risorse alieutiche abbia, su larga scala, determinato: 1) un intenso impatto sulle popolazioni di specie bersaglio (es. diminuzione della densità e/o della taglia media di molte specie commerciali); 2) scompensi a livello di intere comunità ed ecosistemi (Jackson et al., 2001), con effetti deleteri su servizi e beni ecosistemici (Worm et al., 2006), dal momento che gran parte delle specie commerciali sono predatori di alto livello all’interno delle reti trofiche di cui fanno parte. Il fatto che la pesca impatti in particolar modo le specie bersaglio, cioè quelle di maggiore valore economico, ha come implicazione che il suo divieto dovrebbe produrre risposte più evidenti da parte delle popolazioni di queste specie, per esempio in termini di aumento delle densità e/o frequenza di individui di taglia più grande. La valutazione del cosiddetto ‘effetto riserva’ (ER; Fig. 1.1) consiste nello studio del possibile aumento della densità, taglia e biomassa (intesa come ‘peso fresco’ per unità di superficie campionaria) delle specie bersaglio all’interno di una AMP in confronto ad aree di controllo in cui la pesca è consentita (Guidetti, 2002). Fig. 1.1. Esempio di ‘effetto riserva’ (ER). Densità media (SE; numero di individui 125 m2) di sarago maggiore, Diplodus sargus, in siti protetti (P) dell’AMP di Miramare (Trieste) e non protetti (F1, F2) in relazione alla taglia (S: small = piccoli; M: medium = medi; L: large = grandi). Da Guidetti et al., 2005. Per quel che concerne il Mar Mediterraneo, sono numerosi gli studi che hanno indagato gli effetti ecologici delle AMP in termini di: 1) recupero di singole popolazioni, intere comunità o reti trofiche (Sala et al., 1998; Guidetti, 2006; Guidetti & Sala, 2007; Claudet et al., 2006); 2) benefici per la pesca (Harmelin-Vivien et al., 2008; Guidetti & Claudet, 2010; Guidetti et al., 2010). I risultati ottenuti sono intimamente legati alla protezione reale e non solo formale (Guidetti et al., 2008), così come al disegno ed alla gestione di 5 ogni singola AMP (Claudet et al., 2008). Va detto che gli effetti delle AMP sulle specie target della pesca non sono potenzialmente limitati a cambiamenti che si realizzano solo all’interno dei confini delle AMP. L’aumento della taglia, infatti, implica un aumento delle potenzialità di produzione di uova e larve da parte dei riproduttori (Kellner et al., 2007). Ciò, unito ad un export di biomassa di pesci adulti che si realizza con i loro movimenti attraverso i confini delle AMP (Harmelin-Vivien et al., 2008), può determinare un incremento dei rendimenti della pesca anche al di fuori delle AMP (White et al., 2008), grazie ad un fenomeno complessivo chiamato spillover (Fig. 1.2). Fig. 1.2. L’abbondanza di 8 specie ittiche commerciali è maggiore al centro dell’AMP (Torre Guaceto) per poi declinare verso i confini e procedendo oltre, a distanza crescente dai confini stessi dell’AMP. Da Lubchenco et al., 2007. Al di là dell’ER diretto (recupero delle popolazioni di specie bersaglio della pesca), le AMP possono determinare un recovery a livello di intere comunità. In Mediterraneo, per esempio, è ormai noto che il sarago maggiore (Diplodus sargus) ed il sarago fasciato (D. vulgaris), specie bersaglio dal punto di vista commerciale, svolgono un’importante funzione ecologica. Questi saraghi, infatti, predano i ricci di mare (giovani ed adulti) e possono controllarne le densità di popolazione. Diversamente, alcuni labridi come Coris julis e Thalassoma pavo predano solo i ricci piccoli. I ricci, ad elevate densità, possono determinare la transizione da substrati rocciosi ricoperti da macroalghe a barren (cioè substrati rocciosi denudati dalla copertura di macroalghe erette; Fig. 1.3). 6 Fig. 1.3: a: sarago maggiore, Diplodus sargus; b: sarago fasciato, Diplodus vulgaris; c: donzella, Coris julis; d: donzella pavonina Thalassoma pavo; e: riccio viola, Paracentrotus lividus; f: riccio nero, Arbacia lixula; g: substrato roccioso ricoperto da macroalghe erette; h: tipico barren. In zone dove la pesca dei saraghi è intensa si può assistere alla presenza di estesi barren a causa degli effetti indiretti che la pesca produce attraverso la rete trofica (il fenomeno complessivo prende il nome di cascata trofica) (Fig. 1.4). AMP Fuori AMP Fig. 1.4. Esempio di ‘cascata trofica’. Nella zona A dell’AMP di Torre Guaceto l’abbondanza dei saraghi tiene sotto controllo quella dei ricci. Ciò determina una maggiore copertura da parte delle macroalghe erette rispetto ai barren. Al di fuori della zona A e della AMP, i saraghi sono meno abbondanti e mediamente più piccoli, i ricci più abbondanti ed i barren più estesi. Da Gaines et al., 2011. Questa transizione implica non solo drammatici cambiamenti nella struttura di comunità (es., diminuzione della biodiversità), ma anche profondi cambiamenti nel funzionamento ecosistemico (es. produzione primaria e disponibilità di detrito). 7 Presso Torre Guaceto, per esempio, studi recenti hanno mostrato che le popolazioni di molte specie ittiche, inclusi D. sargus e D. vulgaris, mostrano densità e taglie più elevate nell’AMP rispetto a zone esterne aperte alla pesca (Guidetti 2006). L’estensione dei barren risulta maggiore al di fuori dell’AMP dove sono stati stimati tassi di predazione da parte dei pesci sui ricci di gran lunga inferiori rispetto alle zone A (Guidetti 2006) (Fig. 1.5). Fig. 1.5. I due scenari relativi agli stati alternativi delle comunità costiere di fondo duro in relazione all’impatto della pesca: a sinistra, nella zona A dell’AMP di Torre Guaceto, l’abbondanza dei saraghi tiene sotto controllo quella dei ricci. Ciò determina una maggiore copertura da parte delle macroalghe erette rispetto ai barren; a destra, al di fuori della zona A e della AMP, i saraghi sono meno abbondanti e mediamente più piccoli, i ricci più abbondanti ed i barren più estesi. Disegno di Alberto Gennari, 2011. L’esempio di Torre Guaceto suggerisce che le AMP possono contribuire ad un recupero non solo delle popolazioni di specie bersaglio, ma anche ad un ripristino delle loro funzioni ecologiche ed un recupero a livello delle intere comunità. 8 Tutto ciò è alla base del significativo successo, almeno dal punto di vista numerico, che le AMP hanno avuto negli ultimi decenni come strumenti di gestione dell’ambiente marino (a livello ecosistemico e precauzionale) e delle risorse di pesca. In Mar Mediterraneo le AMP sono aumentate vertiginosamente di numero negli ultimi anni (Abdulla et al., 2008). Sia in Mediterraneo che altrove, gli studi sull’efficacia delle AMP sono stati solitamente impostati in termini di valutazioni di differenze nella fauna ittica tra riserve integrali (es., le nostre Zone A) e controlli esterni alle AMP. Va ricordato che a livello internazionale (quindi a prescindere dalla legislazione italiana) il termine AMP è molto generico ed indica un ‘settore di costa o un’area di mare in cui le attività umane, pesca inclusa, sono in qualche modo gestite, limitate o totalmente vietate’ (Agardy et al., 2003). Diverso e molto più specifico è invece l’uso del termine ‘riserva’, di solito indicato come ‘no-take reserve’, cioè un ‘tratto di costa o un’area di mare in cui qualsiasi attività estrattiva di risorse è completamente vietata’. Le zone A delle AMP italiane andrebbero così definite come ‘no-access/no-take reserves’. In molti paesi nel mondo (es., USA, Australia) sono diffuse le ‘no-take reserves’. Per contro, in Mediterraneo (Italia inclusa) le AMP sono generalmente suddivise in sub-aree caratterizzate da differenti livelli di protezione. Le zone A (noaccess/no-take reserves), quindi, sono di piccola taglia e dovrebbero essere circondate da aree cuscinetto (le zone B e C) caratterizzate da livelli progressivamente meno restrittivi in termini di divieti e regolamentazione delle attività umane. Ciò ha senso se riferito allo specifico contesto del Mediterraneo, cioè un bacino le cui coste sono densamente popolate, meta di turisti da tutto il mondo, dove sono presenti grandi città e dove si svolgono gran parte delle attività umane. Malgrado ciò non è disponibile alcuno studio effettuato per valutare l’efficacia delle AMP in Mediterraneo ed in Italia che abbia considerato esplicitamente anche le zone cuscinetto, come le zone B e C delle AMP italiane, eccetto che per l’AMP Tavolara-Punta Coda Cavallo (Di Franco et al., 2009). Le informazioni provenienti da altre regioni del mondo sulle cosiddette ‘partial reserves’ sono piuttosto limitate (Denny and Babcock, 2004; Shears et al., 2006). Vi è più di un sospetto che le zone cuscinetto che circondano le 9 riserve integrali attirino e concentrino pescatori professionisti e ricreativi (Stelzenmuller et al. 2007; Lloret et al., 2008). Per altro vi sono evidenze crescenti che i pescatori ricreativi (o sportivi) possano causare un impatto significativo sulla fauna ittica, simile se non superiore a quello dei pescatori professionisti (Lewin et al., 2006; Lloret et al., 2008). Se così fosse, è evidente che sarebbero necessari specifici monitoraggi nelle zone cuscinetto oltre a indagini (del tutto mancanti ad oggi) sulla pesca ricreativa-sportiva al fine di mettere a punto misure adeguate di regolamentazione della pesca complessiva ed evitare che tale concentrazione di pescatori (professionisti e non) possa determinare un impatto sulla fauna ittica nelle zone cuscinetto addirittura maggiore di quello che si realizza all’esterno delle AMP (contraddicendo di fatto le ragioni per cui le zone cuscinetto sono instituite intorno alle riserve integrali). Va sottolineato che la letteratura sulla valutazione dell’efficacia delle AMP in Mediterraneo è rappresentata per la stragrande maggioranza da studi condotti su fondi sublitorali di natura rocciosa (Guidetti et al., 2008 e referenze ivi contenute). Questo è dovuto a ragioni diverse: 1) la fauna ittica di altri habitat risponde in modo meno efficace alla protezione (Francour, 1994); 2) gran parte delle AMP, soprattutto in Italia, comprendono fondali di tipo roccioso (Di Franco et al., 2009). Al di là dei sopra riportati aspetti legati alla salute degli stock ittici relativamente agli impatti delle diverse forme di pesca, è intuitivo pensare che senza l’apporto costante e significativo di giovanili le popolazioni locali di specie ittiche si estinguerebbero comunque, a causa della mortalità naturale a cui si aggiunge quella dovuta alla pesca o altri impatti umani. L’arrivo ciclico di nuovi individui giovani (chiamato ‘reclutamento’) è quindi fondamentale per il mantenimento degli stock ittici nel tempo, nel lungo periodo. Da questa prospettiva, è fondamentale che le AMP siano create o includano areali con ‘certe’ caratteristiche in termini di distribuzione e varietà di habitat (es., praterie di Posidonia oceanica, fondali rocciosi, etc). Per assicurare il ciclo biologico di tutte le specie costiere sono infatti indispensabili mosaici di differenti tipologie di habitat che gli individui delle varie specie usano sia da adulti, sia durante le fasi più precoci del ciclo vitale (Guidetti et al., 2009). Molte specie, da questa 10 prospettiva, usano habitat diversi da giovani e da adulti (es., molti sparidi). Si veda, per esempio, il caso del sarago fasciato o sarago testa-nera (Diplodus vulgaris), uno sparide molto comune e noto anche perché di importanza commerciale per la pesca ricreativa e professionale. Gli adulti (i riproduttori, essenziali per il mantenimento delle popolazioni sul lungo periodo) sono presenti fondamentalmente su fondali di natura rocciosa e su praterie di P. oceanica, uova e larve permangono per poco più di un mese nelle acque del largo, mentre gli stadi giovanili (dai piccoli pesci appena metamorfosati di taglia intorno ad 1 cm di lunghezza totale fino a giovanili che qualche mese dopo raggiungono i 5-6 cm di lunghezza) vivono per alcuni mesi in ambienti apparentemente banali, cioè su fondali molto vicini a costa dove la roccia si alterna a lenti di sabbia a circa 1-3 m di profondità (Fig. 1.6). Tali zone ed habitat, in cui i giovanili trascorrono una parte della loro vita prima di aggregarsi alle frazioni adulte delle popolazioni, prendono il nome di nursery areas (vedi Guidetti et al., 2009). Fig. 1.6. Ciclo vitale di Diplodus vulgaris, sarago fasciato o testa-nera. Disegno di Alberto Gennari, 2011. 11 Il presente progetto, condotto presso l’AMP di Tavolara-Punta Coda Cavallo, quindi, è quindi finalizzato: 1) a proseguire il monitoraggio dell’ER sulla fauna ittica (orami in corso dal 2005) in ambiente sublitorale roccioso in zone a riserva integrale (zone A), in zone cuscinetto (zone B e C) ed all’esterno dell’AMP; 2) a valutare in via preliminare le potenzialità di nurseries di alcuni siti costieri campione, all’interno dei confini dell’AMP. 12 2. Materiali e metodi 2.1 Area, tecnica e disegno di campionamento per la valutazione dell’ER Il presente studio è stato condotto presso l’AMP di Tavolara-Punta Coda Cavallo (Sardegna nord-orientale). L’AMP si estende per quasi 16.000 ettari; è stata istituita formalmente nel 1997, ma è soggetta ad un efficace controllo solo dal 2003-2004. La costa è prevalentemente rocciosa e di natura granitica, eccettuato qualche inserto calcarenitico, come l’Isola di Tavolara, Capo Figari e Figarolo (Fig. 2.1.1a, b; vedi anche Guidetti et al., 2004). a b Fig. 2.1.1 a, b: area di indagine ed immagine della costa presso l’AMP di Tavolara-Punta Coda Cavallo. I censimenti per la valutazione dell’ER nel sublitorale roccioso sono stati effettuati in aree soggette ad impatto potenzialmente crescente delle attività di pesca (nel complesso 4 livelli di protezione dalla pesca): nelle zone A (in cui tutte le forme di pesca sono vietate), nelle zone B (in cui sono consentite solo alcune attività di pesca professionale), in zona C (in cui sono consentite attività di pesca professionale e sportiva tranne la pesca subacquea in apnea) ed in zone esterne all’AMP (in cui è consentita anche la pesca subacquea in apnea). Fig. 2.1.2: zonizzazione dell’AMP di TavolaraPunta Coda Cavallo e localizzazione delle località oggetto del campionamento. 13 Il piano di campionamento appositamente elaborato ha previsto l’esecuzione di censimenti visuali della fauna ittica (vedi dettagli in seguito) presso 2 località per ognuno dei 4 livelli di protezione: Tavolara e Molarotto (zone A); Molara e Capo Ceraso (zone B); Monte Pedrosu e Capo Coda Cavallo (zone C); Capo Ceraso e Capo Figari (zone esterne all’AMP) (Fig. 2.1.2). Presso ognuna delle 8 località sono stati selezionati randomicamente 2 siti, presso ognuno dei quali sono stati effettuati 4 transetti (i.e. repliche) a 2 livelli di profondità (5-10 e 12-18 m), per un totale di 128 rilevamenti. Una prima campagna è stata condotta nel Maggio 2011, mentre una seconda campagna è stata effettuata nell’ Agosto 2011. Nel complesso, quindi, sono stati svolti 256 rilevamenti nel sublitorale roccioso per la valutazione dell’ER. La valutazione dell’ER è stata effettuata attraverso censimenti visuali della fauna ittica, utilizzando la tecnica dei transetti (Harmelin-Vivien et al., 1985). Tale tecnica consiste nel censire, direttamente in immersione subacquea, le specie ittiche (con particolare riguardo per le specie bersaglio) lungo ‘corridoi’ di fondale roccioso di 25 x 5 m, valutandone l’abbondanza e la taglia (come lunghezza totale, LT) (Fig. 2.1.3a, b). a b Fig. 2.1.3. a: operatore subacqueo intento a raccogliere dati durante un visual census; b: rappresentazione schematica di un transetto di 25 m di lunghezza e 5 m di larghezza. Per gran parte delle specie ittiche, comprese quelle bersaglio (es., il sarago maggiore Diplodus sargus sargus), la taglia è stata valutata secondo classi di 2 cm di ampiezza, mentre per specie di dimensioni assolute più grandi (es., la cernia bruna Epinephelus marginatus ed anche la corvina Sciaena umbra) sono state utilizzate classi dimensionali di 5 cm. 14 I rilevamenti sono stati eseguiti da personale scientifico esperto dell’URL CoNISMa di Lecce in collaborazione con una unità del personale dell’AMP di Tavolara-Punta Coda Cavallo opportunamente addestrata (Dr. P. Panzalis). Ciò rientra in un processo di formazione continua del personale tecnico dell’AMP. Per quel che concerne la valutazione dell’ER nel sublitorale roccioso è stato utilizzato il seguente disegno di campionamento: 1. fattore PROTEZIONE (Pr), fisso, con quattro livelli: zona A, B, C ed Esterno; 2. fattore LOCALITA’ (Lo), random, gerarchizzato (nested) in Pr, con due livelli (A1, A2; B1, B2; C1, C2; E1, E2); 3. fattore SITO (Si) random, gerarchizzato (nested) in Lo, con due livelli (S1, S2); 4. Profondità (De), fisso, ortogonale, con due livelli: 5-10 m; 12-18 m; 5. Tempo (Ti), random, ortogonale, con due livelli (t1, t2). In sintesi, quindi, per ogni tipologia di zona (A, B, C ed Esterno) e per ognuna delle due diverse campagne di campionamento (Maggio 2011, Agosto 2011) sono state selezionate due località. In ciascuna località sono stati ulteriormente selezionati (randomicamente) due siti (i.e. tratti di litorale di alcune decinecentinaia di metri di lunghezza), presso ognuno dei quali sono stati censiti i popolamenti ittici attraverso 8 transetti (repliche), di cui 4 sono stati condotti tra 5 e 10 m ed altri 4 tra 12 e 18 m di profondità. 2.2 Valutazioni sui giovanili di specie ittiche I dati relativi alla presenza, abbondanza e taglia dei giovanili di specie ittiche sono stati raccolti presso 4 siti ‘campione’ rappresentativi delle tipologie ambientali a bassa profondità dell’area in esame, con particolare riguardo per gli habitat nursery a bassa profondità (vedi Bussotti e Guidetti, 2011). I censimenti dei giovanili sono stati condotti al fine di fornire una prima analisi preliminare delle potenzialità dei siti costieri in termini di nurseries. I dati sono stati raccolti presso 4 siti di campionamento: 1) Capo Ceraso; 2) Tavolara Cimitero; 3) Tavolara Tramontana; 4) Isola di Raulino. 15 Presso Capo Ceraso i censimenti sono stati svolti all’interno di baie o insenature, in cui i bassifondi (0-3 m) erano costituiti da paretine e massi di granito alternati a sabbia grossolana. Presso Tavolara Cimitero il fondale tra 0 e 3 m di profondità era costituito da roccia granitica affiorante caratterizzata da bassa pendenza (~20%) ed elevata copertura a macroalghe erette (>90%), inframmezzata da sabbia grossolana ed ampi tratti a ciottoli chiari. Presso Tavolara Tramontana il fondale tra 0 e 3 m circa era prevalentemente costituito da rocce con alghe (>90%) a media pendenza (30-50%), alternata a fondale a ciottoli chiari (copertura macroalghe=40%; pendenza 30%) e ampi tratti con alternanza di roccia, sabbia e Posidonia oceanica a bassa pendenza (0-20%). Presso Isola Raulino, infine, il bassofondo era rappresentato sostanzialmente da falesie più o meno esposte, con rientranze riparate, elevata pendenza (6090%) ed elevata copertura a macroalghe (>90%). Fig. 2.2.1: tipologie di ambienti costieri a bassa profondità che presentano caratteristiche potenzialmente idonee per essere aree nursery per i giovanili di molte specie ittiche costiere. Tali località sono state preselezionate nel Maggio 2011, in seguito ad un presurvey. Nell’Agosto 2011 sono stati svolti i censimenti visivi sui giovanili. In particolare sono state svolte 3 repliche di visual census lungo transetti di 10 x 2 m, randomicamente posizionati presso le 4 località preselezionate. Durante l’esecuzione dei transetti, percorsi in circa 10 minuti, sono stati raccolti dati relativi alla abbondanza e taglia degli individui appartenenti a tutte specie osservate di cui sono state osservate fasi giovanili. 16 2.3 Analisi dei dati I dati raccolti per la valutazione dell’ER sono stati analizzati mediante tecniche di analisi multivariata ed univariata al fine di esaminare sia la struttura dei popolamenti (composizione in specie ed abbondanze relative), sia singole variabili (e.g., densità/biomassa di singole specie) in relazione al livello di protezione, alla profondità ed alle differenti scale spaziali considerate (località e siti). In particolare va sottolineato che le analisi a livello dei popolamenti sono state condotte escludendo le specie di nessun interesse commerciale così come quelle gregarie e planctonofaghe, le quali solitamente influiscono in modo molto marcato sui pattern di variabilità (essendo numericamente preponderanti), ma a prescindere dagli effetti della protezione (Harmelin-Vivien et al., 2008). Sulla base delle densità e dei valori stimati delle taglie sono state stimate le biomasse (peso umido) per unità di campionamento utilizzando le relazioni lunghezza-peso disponibili in letteratura per le specie oggetto di analisi (www.fishbase.org). Sono stati scelti i coefficienti di correlazione relativi a relazioni stabilite su campioni raccolti in Mediterraneo. Le differenze nella struttura dei popolamenti ittici associati al sublitorale roccioso (in termini di densità e biomassa) sono state testate attraverso analisi statistiche multivariate condotte con il package PRIMER 6 (Plymouth Marine Laboratory, UK) implementato con le routine Permanova+. Dalla matrice ad n colonne x m righe è stata calcolata, tramite il coefficiente di similarità di BrayCurtis, una matrice triangolare di similarità. Basandosi su tale matrice, il test dell’ipotesi della presente indagine è stato condotto utilizzando Permanova (Permutational Multivariate Analysis of Variance; Anderson, 2001). La visualizzazione dei pattern multivariati è stata ottenuta mediante nMDS (nonmetric Multi Dimensional Scaling), una procedura multivariata di ordinamento che permette di costruire una ‘mappa’ dei campioni a due o tre dimensioni, tale che le distanze tra i punti (i campioni, in questo studio le singole repliche o transetti) sulla mappa riflettano la maggiore o minore similarità tra i campioni stessi. 17 L’analisi della varianza (PERMANOVA univariata) è stata condotta al fine di testare l’ipotesi di possibili differenze nella distribuzione di densità e biomassa delle principali specie ittiche target: la cernia bruna, la corvina ed il sarago maggiore. I dati relativi alla taglia degli individui delle specie target censiti nelle località a diverso grado di protezione sono stati riportati in grafici lunghezza/frequenza al fine di permettere un confronto visuale tra le distribuzioni di taglia. I dati relativi ai giovanili sono stati rappresentati in grafici specie per specie, relativamente ad ognuno dei 4 siti campionati. 18 3. Risultati 3.1 “Effetto Riserva” nel sublitorale roccioso: comparazione tra zone A, B, C ed esterno Nel sublitorale roccioso sono stati censiti complessivamente 54 taxa della fauna ittica durante le due campagne di campionamento (Tab. 3.1.1). Tab. 3.1.1: Lista dei taxa della fauna ittica censiti nel sublitorale roccioso presso l’AMP Tavolara-Punta Coda Cavallo e nelle località esterne in esame nella presente indagine. Famiglia Genere specie Apogonidae Apogon imberbis Blennidae Parablennius rouxi Parablennius gattorugine Parablennius zvonimiri Carangidae Lichia amia Seriola dumeriili Centracanthidae Spicara maena Spicara smaris Gobiidae Gobius bucchichi Gobius cobitis Gobius cruentatus Gobius geniporous Gobius paganellus Gobius vittatus Labridae Coris julis Labrus merula Labrus viridis Symphodus cinereus Symphodus doderleini Symphodus mediterraneus Symphodus melanocercus Symphodus ocellatus Symphodus roissali Symphodus rostratus Symphodus tinca Thalassoma pavo Serranidae Epinephelus costae Epinephelus marginatus Serranus cabrilla Serranus scriba Sciaenidae Sciaena umbra Mugilidae Pomacentridae Chromis chromis Sparidae Boops boops Dentex dentex Diplodus annularis Diplodus puntazzo Diplodus sargus Diplodus vulgaris Oblada melanura Pagrus pagrus Sarpa salpa Sparus aurata Spondyliosoma cantharus Pomatomidae Pomatomus saltatrix Sphyraenidae Sphyraena viridensis Scorpaenidae Scorpaena maderensis Scorpaena porcus Scorpaena scrofa Tripterygiidae Tripterygion delaisi Tripterygion minutus Mullidae Mullus surmuletus Muraenidae Murena helena Phycidae Phycis phycis 19 Considerando la densità totale del popolamento ittico è stata osservata una differenza significativa tra zone a diverso livello di protezione; è stata inoltre evidenziata una variabilità significativa tra anni ed alla scala di siti ed alcune significative interazioni tra fattori (Tab. 3.1.2). Tab. 3.1.2. PERMANOVA condotta su dati di abbondanza della fauna ittica. Fattori: Ti=Tempo di campionamento, Zo=zona; De=profondità; Ti=Tempo di campionamento, Lo=località; Si=sito. In grassetto-sottolineato sono riportati i valori di P statisticamente significativi. _____________________________________________________________________ Source df SS ZO 3 25413 DE 1 3032,7 TI 1 16341 LO(ZO) 4 6770,7 ZOxDE 3 2754,4 ZOxTI 3 3661 DExTI 1 1013,7 SI(LO(ZO)) 8 20698 LO(ZO)xDE 4 3474,7 LO(ZO)xTI 4 13492 ZOxDExTI 3 2107 SI(LO(ZO))xDE 8 4462,8 SI(LO(ZO))xTI 8 12700 LO(ZO)xDExTI 4 2565,3 SI(LO(ZO))xDExTI 8 6384,4 Res 192 1,0349E5 Total 255 2,2836E5 MS Pseudo-F P(perm) 8471,2 4,066 0,0488 3032,7 1,9519 0,155 16341 4,8446 0,032 1692,7 0,55033 0,9594 918,15 0,99266 0,501 1220,3 0,36179 0,8941 1013,7 1,5806 0,2363 2587,2 1,6298 0,0756 868,66 1,3899 0,1981 3373,1 2,1249 0,0466 702,33 1,0951 0,4275 557,85 0,69901 0,8472 1587,5 2,9452 0,0001 641,32 0,8036 0,6681 798,05 1,4806 0,0107 539 perms 9911 9950 9812 9926 9928 9953 9922 9905 9912 9938 9956 9913 9855 9923 9825 P(MC) 0,0001 0,1001 0,0031 0,9901 0,5105 0,9879 0,1838 0,0451 0,0906 0,0118 0,3981 0,8971 0,0001 0,7216 0,0196 ______________________________________________________________________ Dal successivo test pairwise si evidenzia come la zona A sia diversa da tutte le altre zone (p<0,01 per tutti e tre i confronti). Non sono evidenti differenze significative tra la zona B, la zona C e le località esterne. La figura 3.1.1-a mostra una separazione piuttosto evidente dei campioni relativi alla zona A da quelli delle altre zone. I dati relativi alle due campagne (che non sono stati distinti dato che l’interazione TixZo non è risultata significativa; Tab. 3.1.2), infatti, mostrano comunque una elevata variabilità per i campioni della zona A se plottati come singole repliche. Se plottati come centroidi delle località (caratterizzate da diverso livello di protezione) emerge chiaramente come le due località in zona A siano quelle maggiormente variabili, (Fig. 3.1.1-b). 20 Fig. 3.1.1. Struttura dei popolamenti ittici (densità totali). a: nMDS delle singole repliche relative alle 4 tipologie di zona; b: nMDS dei centroidi relativi alle località caratterizzate da diversi livelli di protezione. Le analisi multivariate condotte sulle biomasse totali hanno evidenziato una differenza statisticamente significativa relativamente al livello di protezione (Tab. 3.1.3), oltre che tra i due tempi di campionamento. I test pairwise a posteriori hanno mostrato che la zona A differisce da tutte le altre zone (p<0,05). Tab. 3.1.3. PERMANOVA condotta su dati di biomassa della fauna ittica. Fattori: Ti=Tempo di campionamento, Zo=zona; De=profondità; Ti=Tempo di campionamento, Lo=località; Si=sito. In grassetto-sottolineato sono riportati i valori di P statisticamente significativi. _______________________________________________________________ Source df SS ZO 3 50545 DE 1 4648 TI 1 29051 LO(ZO) 4 14622 ZOxDE 3 3788,1 ZOxTI 3 8994,9 DExTI 1 2100,5 SI(LO(ZO)) 8 25078 LO(ZO)xDE 4 3951 LO(ZO)xTI 4 15518 ZOxDExTI 3 3670,2 SI(LO(ZO))xDE 8 10171 SI(LO(ZO))xTI 8 29163 LO(ZO)xDExTI 4 4371,7 SI(LO(ZO))xDExTI 8 7323,1 Res 192 1,5894E5 Total 255 3,7194E5 MS Pseudo-F P(perm) 16848 3,1152 0,0298 4648 1,859 0,1829 29051 7,4884 0,0153 3655,6 1,0409 0,4332 1262,7 1,0653 0,4383 2998,3 0,77286 0,6929 2100,5 1,9219 0,1766 3134,8 0,85995 0,6501 987,76 0,80497 0,7837 3879,5 1,0642 0,4171 1223,4 1,1194 0,4092 1271,3 1,3888 0,132 3645,3 4,4036 0,0001 1092,9 1,1939 0,3079 915,39 1,1058 0,2596 827,81 perms 9940 9947 9837 9910 9926 9932 9941 9922 9916 9929 9942 9904 9833 9909 9861 P(MC) 0,0005 0,1159 0,0003 0,4315 0,4121 0,7513 0,0806 0,7418 0,849 0,401 0,3716 0,0879 0,0001 0,257 0,2623 _______________________________________________________________ 21 Il plot nMDS relativo alle biomasse totali (Fig. 3.1.2 a), non evidenzia una chiarissima separazione tra i popolamenti ittici delle zone a protezione differente. Plottando i centroidi relativi alle singole località si evidenzia come alcune località (le due della zona A, B2 ed EXT1) si separino dal resto delle località indagate (Fig. 3.1.2 b). Fig. 3.1.2: struttura dei popolamenti ittici (biomasse totali). a: nMDS delle singole repliche relative alle 4 tipologie di zona; b: nMDS dei centroidi relativi alle località caratterizzate da diversi livelli di protezione. I dati di densità totale (numero medio di individui per 125 m2, considerando insieme tutte le specie) mostrano valori più elevati in zona A, seguita in ordine da zona B, zona C e località esterne (Fig. 3.1.3). Fig. 3.1.3: densità totale della fauna ittica (media±SE) nelle diverse tipologie di zona (pooling tra località, siti, profondità e tempi). 22 L’analisi statistica ha mostrato differenze dal punto di vista statistico relativamente ai diversi livelli di protezione (Tab. 3.1.4). Analizzando i confronti a coppie, però nessuno di questi risulta significativo e l’unica differenza che si avvicini alla significatività è quella tra i valori registrati in zona A e tutte le altre zone (p=0,08 per tutte e tre i confronti a coppie). Tab. 3.1.4. PERANOVA condotta su dati di densità totale della fauna ittica. Fattori: Zo=zona; De=profondità; Ti=tempo di campionamento; Lo=località; Si=sito. In grassetto-sottolineato sono riportati i valori di P statisticamente significativi. _______________________________________________________________ Source df ZO 3 DE 1 TI 1 LO(ZO) 4 ZOxDE 3 ZOxTI 3 DExTI 1 SI(LO(ZO)) 8 LO(ZO)xDE 4 LO(ZO)xTI 4 ZOxDExTI 3 SI(LO(ZO))xDE 8 SI(LO(ZO))xTI 8 LO(ZO)xDExTI 4 SI(LO(ZO))xDExTI 8 Res 192 Total 255 7819,2 SS 2042,8 9,7656 517,56 59,906 20,766 139,09 0,5625 178,19 52,406 130,66 3,2188 145,19 703,56 120,28 207,81 3487,5 MS Pseudo-F P(perm) 680,92 11,633 0,0171 9,7656 2,9154 0,1639 517,56 15,845 0,0184 14,977 1,8734 0,1292 6,9219 2,6098 0,1163 46,365 1,4194 0,3416 0,5625 1,8706E-2 0,8932 22,273 0,25326 0,9673 13,102 0,81043 0,6434 32,664 0,37141 0,8432 1,0729 3,568E-2 0,9905 18,148 0,69865 0,7096 87,945 4,8417 0,0003 30,07 1,1576 0,3928 25,977 1,4301 0,1806 18,164 perms 9920 9962 9751 9946 9953 9955 9839 9945 9950 9945 9974 9947 9926 9961 9945 P(MC) 0,01 0,1503 0,0173 0,1731 0,1586 0,3518 0,9019 0,9683 0,6419 0,8219 0,9891 0,6904 0,0001 0,3995 0,1865 _______________________________________________________________ La biomassa totale (gr. per 125 m2, considerando insieme tutte le specie osservate) ha mostrato una chiara variazione in funzione della protezione (Fig. 3.1.4). 23 Fig. 3.1.4: biomassa totale della fauna ittica (media±SE) nelle diverse tipologie di zona (pooling tra località, siti, profondità e tempi). Così come per i dati di abbondanza l’analisi statistica ha evidenziato differenze significative relativamente ai diversi livelli di protezione (Tab. 3.1.5), con la zona A che differisce da tutte le altre zone (p<0,05 per tutti e tre i confronti a coppie) e che presenta i valori di biomassa medi per transetto più elevati. Tab. 3.1.5. PERMANOVA condotta su dati di biomassa totale della fauna ittica. Fattori: Zo=zona; De=profondità; Ti=tempo di campionamento; Lo=località; Si=sito. In grassettosottolineato sono riportati i valori di P statisticamente significativi. _______________________________________________________________ Source df SS ZO 3 1,8517E5 DE 1 5908,7 TI 1 4137,8 LO(ZO) 4 8747,6 ZOxDE 3 10164 ZOxTI 3 4378,9 DExTI 1 573,94 SI(LO(ZO)) 8 19957 LO(ZO)xDE 4 1886,1 LO(ZO)xTI 4 4435,7 ZOxDExTI 3 2182,2 SI(LO(ZO))xDE 8 4932,7 SI(LO(ZO))xTI 8 19903 LO(ZO)xDExTI 4 8978,3 SI(LO(ZO))xDExTI 8 5778,4 Res 192 1,4719E5 Total 255 4,3432E5 MS Pseudo-F P(perm) 61723 17,231 0,0147 5908,7 7,7987 0,033 4137,8 3,7314 0,1262 2186,9 1,2973 0,332 3388 4,698 0,0262 1459,6 1,3163 0,3841 573,94 0,2557 0,6398 2494,6 1,0027 0,5044 471,54 0,41726 0,9203 1108,9 0,44572 0,7719 727,41 0,32407 0,806 616,59 0,85364 0,5779 2487,9 3,2453 0,0021 2244,6 3,1075 0,077 722,3 0,94221 0,493 766,61 perms 9938 9963 9732 9958 9953 9952 9862 9949 9947 9951 9966 9951 9945 9954 9943 P(MC) 0,0019 0,0749 0,1234 0,3348 0,0397 0,3866 0,6525 0,5008 0,909 0,7731 0,8174 0,59 0,0013 0,0804 0,474 _______________________________________________________________ 24 Le distribuzioni di abbondanza e biomassa delle tre specie bersaglio della pesca utilizzate come indicatori dell’ER presso l’AMP di Tavolara-Punta Coda Cavallo sono di seguito riportate. La cernia bruna (Epinephelus marginatus; Fig. 3.1.5) ha mostrato pattern di densità e biomassa Fig. 3.1.5: esemplare di cernia bruna, Epinephelus marginatus. media maggiori nella zona A rispetto alle altre tre zone in esame (Fig. 3.1.6 a, b). Fig. 3.1.6: densità (a) e biomassa (b) (media±SE) della cernia bruna nelle 4 tipologie di zona (A, B, C ed esterno). 25 Questo andamento è confermato dall’analisi formale sia per la densità sia per la biomassa media per transetto (Tab. 3.1.6 e 3.1.7). Nelle altre zone i valori sono risultati chiaramente inferiori e simili tra zone B, C ed esterno (Fig. 3.1.6 a, b). Tab. 3.1.6. PERMANOVA condotta su dati di densità della cernia bruna nell’infralitorale roccioso. Fattori: Zo=zona; De=profondità; Ti=tempo di campionamento; Lo=località; Si=sito. In grassetto-sottolineato sono riportati i valori di P statisticamente significativi. _______________________________________________________________ Source df SS MS Pseudo-F P(perm) perms ZO 3 9,043 3,0143 7,6489 0,0669 9791 DE 1 2,0664 2,0664 8,1364 0,031 9957 TI 1 3,2852 3,2852 4,4973 0,097 8923 LO(ZO) 4 0,85938 0,21484 0,93548 0,5442 9936 ZOxDE 3 0,35547 0,11849 2,5469 0,1199 9960 ZOxTI 3 0,82422 0,27474 0,37611 0,8005 9924 DExTI 1 3,5156E-2 3,5156E-2 4,8128E-2 0,8337 9343 SI(LO(ZO)) 8 1,9062 0,23828 0,34463 0,9424 5654 LO(ZO)xDE 4 1,2344 0,30859 0,51724 0,8569 9916 LO(ZO)xTI 4 2,9219 0,73047 1,0565 0,4378 9946 ZOxDExTI 3 7,4219E-2 2,474E-2 3,3868E-2 0,9895 9963 SI(LO(ZO))xDE 8 1,4063 0,17578 1,0976 0,4579 4535 SI(LO(ZO))xTI 8 5,5312 0,69141 2,5166 0,0118 9933 LO(ZO)xDExTI 4 2,9219 0,73047 4,561 0,032 9946 SI(LO(ZO))xDExTI 8 1,2813 0,16016 0,58294 0,7855 9927 Res 192 52,75 0,27474 Total 255 86,496 P(MC) 0,0135 0,0339 0,1025 0,5689 0,1689 0,7745 0,8394 0,9254 0,8104 0,4389 0,9886 0,4499 0,01 0,0333 0,7945 _______________________________________________________________ Tab. 3.1.7. PERMANOVA condotta su dati di biomassa della cernia bruna nell’infralitorale roccioso. Fattori: Zo=zona; De=profondità; Ti=tempo di campionamento; Lo=località; Si=sito. In grassetto-sottolineato sono riportati i valori di P statisticamente significativi. _______________________________________________________________ Source df SS MS Pseudo-F P(perm) ZO 3 1,1352E8 3,7841E7 42,147 0,0648 DE 1 3,8264E7 3,8264E7 75,469 0,0002 TI 1 9,0621E5 9,0621E5 4,3462E-2 0,6798 LO(ZO) 4 5,4069E6 1,3517E6 0,15149 0,9981 ZOxDE 3 7,924E7 2,6413E7 56,469 0,0001 ZOxTI 3 1,2238E5 40795 1,9565E-3 0,9802 DExTI 1 4110,6 4110,6 1,3516E-4 0,9638 SI(LO(ZO)) 8 9,4725E7 1,1841E7 3,2886 0,0338 LO(ZO)xDE 4 3,6235E6 9,0588E5 0,19408 0,9938 LO(ZO)xTI 4 8,3402E7 2,085E7 5,791 0,0177 ZOxDExTI 3 3,0132E5 1,0044E5 3,3025E-3 0,9933 SI(LO(ZO))xDE 8 6,5296E7 8,162E6 1,2403 0,2472 SI(LO(ZO))xTI 8 2,8804E7 3,6005E6 0,45588 0,9439 LO(ZO)xDExTI 4 1,2165E8 3,0413E7 4,6216 0,0284 SI(LO(ZO))xDExTI 8 5,2644E7 6,5805E6 0,83319 0,6582 Res 192 1,5164E9 7,898E6 Total 255 2,2043E9 perms 9860 9965 9339 9952 9961 9925 9182 9909 9949 9953 9972 9908 9926 9959 9901 P(MC) 0,0006 0,0006 0,8455 0,9973 0,0003 1 0,9909 0,0562 0,9895 0,0175 0,9998 0,3787 0,8858 0,0332 0,5716 _______________________________________________________________ 26 Le distribuzioni di taglia della cernia bruna nelle 4 tipologie di zona caratterizzate da diversi livelli di protezione evidenzia che gli esemplari di taglia più grande (>60 cm LT) si trovano solo in zona A (Fig. 3.1.7). Fig. 3.1.10: distribuzione di taglia della cernia bruna nelle 4 tipologie di zona (A, B, C ed esterno). 27 La corvina, Sciaena umbra (Fig. 3.1.8), ha mostrato pattern generali simili a quelli della cernia bruna. Densità e biomassa, infatti, sono risultati maggiori in zona A (Fig. 3.1.9 a, b). Fig. 3.1.8: esemplare di corvina, Sciaena umbra. Fig. 3.1.9: densità (a) e biomassa (b) (media±SE) della corvina nelle 4 tipologie di zona (A, B, C ed esterno). 28 Data l’elevata variabilità, l’analisi formale non ha rivelato differenze apprezzabili in termini di densità (Tab. 3.1.8), mentre differenze significative per il fattore Zona sono state riscontrate in termini di biomassa per transetto (3.1.9). Tab. 3.1.8. PERMANOVA condotta su dati di densità della corvina nell’infralitorale roccioso. Fattori: Zo=zona; De=profondità; Ti=tempo di campionamento; Lo=località; Si=sito. _______________________________________________________________ Source ZO DE TI LO(ZO) ZOxDE ZOxTI DExTI SI(LO(ZO)) LO(ZO)xDE LO(ZO)xTI ZOxDExTI SI(LO(ZO))xDE SI(LO(ZO))xTI LO(ZO)xDExTI SI(LO(ZO)xDExTI Res Total df 3 1 1 4 3 3 1 8 4 4 3 8 8 4 8 192 255 SS MS Pseudo-F 33,105 11,035 2,095 3,5156E-2 3,5156E-2 0,39301 17,535 17,535 5,1069 5,3594 1,3398 0,58014 0,51172 0,17057 0,43385 16,699 5,5664 1,6212 2,4414 2,4414 0,56054 16,594 2,0742 1,1179 34,922 8,7305 1,3861 13,734 3,4336 1,8505 5,1055 1,7018 0,39073 35,094 4,3867 1,2953 14,844 1,8555 0,74961 17,422 4,3555 1,286 27,094 3,3867 1,3682 475,25 2,4753 715,75 P(perm) 0,0872 0,8058 0,0906 0,8426 0,853 0,266 0,4945 0,4035 0,2871 0,1915 0,7703 0,296 0,6938 0,3488 0,1958 perms 9931 9967 9586 9948 9963 9962 9819 9309 9945 9955 9969 9899 9932 9970 9933 P(MC) 0,2364 0,813 0,0882 0,8088 0,7942 0,3187 0,4948 0,4284 0,3013 0,2204 0,7648 0,3555 0,6539 0,352 0,2229 _______________________________________________________________ Nello specifico, dai test a posteriori si evince come la zona A sia differente da tutte le altre zone considerate (p<0,05 per tutti e tre i confronti a coppie). Nessuna differenza è stata invece riscontrata tra le zone B, C ed esterne. Tab. 3.1.9. PERMANOVA condotta su dati di biomassa della corvina nell’infralitorale roccioso. Fattori: Zo=zona; De=profondità; Ti=tempo di campionamento; Lo=località; Si=sito. In grassettosottolineato sono riportati i valori di P statisticamente significativi. _______________________________________________________________ ZO 3 DE 1 TI 1 LO(ZO) 4 ZOxDE 3 ZOxTI 3 DExTI 1 SI(LO(ZO)) 8 LO(ZO)xDE 4 LO(ZO)xTI 4 ZOxDExTI 3 SI(LO(ZO))xDE 8 SI(LO(ZO))xTI 8 LO(ZO)xDExTI 4 SI(LO(ZO))xDExTI 8 Res 192 Total 255 1,0074E9 8,7479E7 8,6546E7 2,2945E8 1,8279E8 1,3041E8 4,6884E7 5,3195E8 1,5805E8 3,897E8 8,5105E7 3,6936E8 5,1287E8 2,4333E8 3,9112E8 8,4739E9 1,2926E10 3,3579E8 8,7479E7 8,6546E7 5,7363E7 6,0931E7 4,3469E7 4,6884E7 6,6493E7 3,9512E7 9,7425E7 2,8368E7 4,617E7 6,4109E7 6,0833E7 4,889E7 4,4135E7 4,2964 1,7167 0,88833 0,74105 1,7938 0,44618 0,7707 1,0372 0,82616 1,5197 0,46633 0,94436 1,4526 1,2443 1,1077 0,017 0,2821 0,4333 0,814 0,1871 0,8458 0,4512 0,427 0,7088 0,1734 0,8084 0,5856 0,0191 0,3237 0,2796 9869 9971 9809 9904 9959 9960 9939 9868 9921 9942 9953 9923 9849 9945 9838 0,0008 0,2126 0,4696 0,8025 0,0935 0,9069 0,5319 0,4665 0,7092 0,1786 0,8857 0,5561 0,0832 0,3013 0,3197 _______________________________________________________________ 29 La distribuzione di taglia della corvina (Fig. 3.1.10) mostra come gli individui di taglia grande (>35 cm LT) siano stati osservati solo in zona A, mentre in zona C ed all’esterno dell’AMP sono stati registrati solo individui di piccole dimensioni. Fig. 3.1.10: distribuzione di taglia della corvina nelle 4 tipologie di zona (A, B, C ed esterno). 30 Il Fig. 3.1.11: distribuzione di taglia della corvina nelle 4 tipologie di zona (A, B, C ed esterno). sarago maggiore, Diplodus sargus (Fig. 3.1.11) ha mostrato sia densità (Fig. 3.1.12 a) sia biomasse (Fig. 3.1.12 b) maggiori in zona A rispetto a tutte le altre zone in esame. Fig. 3.1.11: esemplare di sarago maggiore, Diplodus sargus. Fig. 3.1.12: densità (a) e biomassa (b) (media±SE) del sarago maggiore nelle 4 tipologie di zona (A, B, C ed esterno). 31 Anche le analisi formali (PERMANOVA univariata e confronti a posteriori) hanno confermato queste evidenze sia in termini di densità (Tab. 3.1.10) sia in termini di biomassa (3.1.11). Tab. 3.1.10. PERMANOVA condotta su dati di densità del sarago maggiore nell’infralitorale roccioso. Fattori: Zo=zona; De=profondità; Ti=tempo di campionamento; Lo=località; Si=sito. _______________________________________________________________ Source df SS ZO 3 2042,8 DE 1 9,7656 TI 1 517,56 LO(ZO) 4 59,906 ZOxDE 3 20,766 ZOxTI 3 139,09 DExTI 1 0,5625 SI(LO(ZO)) 8 178,19 LO(ZO)xDE 4 52,406 LO(ZO)xTI 4 130,66 ZOxDExTI 3 3,2188 SI(LO(ZO))xDE 8 145,19 SI(LO(ZO))xTI 8 703,56 LO(ZO)xDExTI 4 120,28 SI(LO(ZO))xDExTI 8 207,81 Res 192 3487,5 Total 255 7819,2 MS Pseudo-F P(perm) 680,92 11,633 0,0171 9,7656 2,9154 0,1639 517,56 15,845 0,0184 14,977 1,8734 0,1292 6,9219 2,6098 0,1163 46,365 1,4194 0,3416 0,5625 1,8706E-2 0,8932 22,273 0,25326 0,9673 13,102 0,81043 0,6434 32,664 0,37141 0,8432 1,0729 3,568E-2 0,9905 18,148 0,69865 0,7096 87,945 4,8417 0,0003 30,07 1,1576 0,3928 25,977 1,4301 0,1806 18,164 perms 9920 9962 9751 9946 9953 9955 9839 9945 9950 9945 9974 9947 9926 9961 9945 P(MC) 0,01 0,1503 0,0173 0,1731 0,1586 0,3518 0,9019 0,9683 0,6419 0,8219 0,9891 0,6904 0,0001 0,3995 0,1865 _______________________________________________________________ Tab. 3.1.11. PERMANOVA condotta su dati di biomassa del sarago maggiore nell’infralitorale roccioso. Fattori: Zo=zona; De=profondità; Ti=tempo di campionamento; Lo=località; Si=sito. In grassetto-sottolineato sono riportati i valori di P statisticamente significativi. _______________________________________________________________ Source df SS MS Pseudo-F P(perm) perms P(MC) ZO 3 2,0877E8 6,9591E7 8,7876 0,0145 9897 0,0277 DE 1 2,6101E6 2,6101E6 1,4054 0,3709 9968 0,3483 TI 1 1,9238E5 1,9238E5 1,5628 0,2778 9647 0,2803 LO(ZO) 4 3,0922E7 7,7305E6 7,4821 0,0015 9950 0,0023 ZOxDE 3 9,2083E6 3,0694E6 2,8732 0,0913 9948 0,1207 ZOxTI 3 6,0854E5 2,0285E5 1,6478 0,313 9967 0,3139 DExTI 1 1,2331E6 1,2331E6 3,2491 0,1504 9851 0,1419 SI(LO(ZO)) 8 8,8649E6 1,1081E6 0,74787 0,6659 9961 0,6604 LO(ZO)xDE 4 3,5768E6 8,942E5 1,98 0,1294 9959 0,164 LO(ZO)xTI 4 4,9241E5 1,231E5 8,3083E-2 0,9838 9961 0,9834 ZOxDExTI 3 9,1856E5 3,0619E5 0,8068 0,5507 9975 0,5549 SI(LO(ZO))xDE 8 3,8144E7 4,768E6 0,5128 0,853 9961 0,8158 SI(LO(ZO))xTI 8 1,1854E7 1,4817E6 0,39075 0,9376 9932 0,9278 LO(ZO)xDExTI 4 1,518E6 3,7951E5 4,0816E-2 0,9949 9957 0,9969 SI(LO(ZO))xDExTI 8 7,4384E7 9,2979E6 2,4521 0,0058 9926 0,0166 Res 192 7,2804E8 3,7919E6 Total 255 1,1213E9 _______________________________________________________________ 32 Per quel che concerne la distribuzione di taglia, il sarago maggiore ha mostrato una chiara e progressiva diminuzione degli individui di taglia maggiore in relazione al decrescente livello di protezione (Fig. 3.1.13). Fig. 3.1.13: distribuzione di taglia (LT: lunghezza totale) del sarago maggiore nelle 4 tipologie di zona (A, B, C ed esterno). 33 3.2 Indagine preliminare sui giovanili e le aree nursery a bassa profondità Nel complesso delle 4 località indagate sono stati censiti nell’Agosto 2011 i giovanili appartenenti a 13 taxa della fauna ittica costiera (Tab. 3.2.1). Tab. 3.2.1. Lista dei taxa della fauna ittica e relativi valori medi di densità (no. individui/50 m2) dei giovanili censiti presso le 4 località di campionamento (CC: Capo Ceraso; TC: Tavolara Cimitero; TT: Tavolara Tramontana; IR: Isola Raulino). Atherina sp. Chromis chromis Coris julis Diplodus sargus Diplodus puntazzo Diplodus vulgaris Mullus surmuletus Oblada melanura Symphodus ocellatus Sarpa salpa Symphodus roissali Symphodus tinca Thalassoma pavo CC 0.0 33.3 0.0 20.7 0.0 4.3 0.0 15.3 0.0 3.3 0.3 0.7 0.0 TC 6.7 33.3 0.0 10.0 0.0 4.7 0.0 1.3 3.3 0.0 1.0 2.0 0.3 TT 0.0 0.0 0.0 17.0 0.0 4.7 1.0 36.7 0.0 2.0 0.0 1.3 0.0 IR 66.7 33.3 5.0 3.3 0.3 5.3 17.3 0.0 0.7 0.0 1.3 0.0 0.0 Per quel che concerne i dati di densità, i giovanili di Chromis chromis (castagnola) sono risultati i più abbondanti. Si tratta, tuttavia, di una specie fortemente gregaria i cui giovanili formano gruppi numerosi sui fondali rocciosi ricchi di anfratti. A seguire i giovanili di Oblada melanura (occhiata), Diplodus sargus sargus (sarago maggiore) e Diplodus vulgaris (sarago fasciato o testanera). Da notare che i giovanili dei due Diplodus sono gli unici ad essere risultati presenti in tutte e 4 le località indagate (Fig. 3.2.1). 34 Fig. 3.2.1: densità dei giovanili delle specie ittiche censite presso le 4 località di indagine (CC: Capo Ceraso; TC: Tavolara Cimitero; TT: Tavolara Tramontana; IR: Isola Raulino). 35 3.3 Formazione del personale dell’Area Marina Protetta La formazione del personale dell’Area Marina Protetta nella valutazione dell’ER tramite l’uso del visual census è cominciata nel 2005 (nell’ambito di una convenzione tra l’AMP ed il DipTeRis, Università di Genova) ed è poi proseguita nel tempo (nell’ambito di convenzioni tra l’AMP ed il CoNISMa URL Lecce). L’attività di formazione si è basata in particolare sull’affiancamento durante l’attività di campo condotta per l’acquisizione dei dati. L’Area Marina Protetta ha indicato una unità del suo personale tecnicoscientifico, Dr. Pieraugusto Panzalis, il quale ha sempre accompagnato il personale scientifico del CoNISMa nelle attività di raccolta dei dati di campo relative alla presente indagine. 36 3.4 Pubblicazioni scientifiche Le attività di monitoraggio della fauna ittica presso l’AMP di Tavolara-Punta Coda Cavallo hanno consentito di pubblicare nel 2009 il seguente lavoro scientifico su rivista internazionale con impact factor: Di Franco A., Bussotti S., Navone A., Panzalis P., Guidetti P., 2009. Evaluating effects of total and partial restrictions to fishing on Mediterranean rocky-reef fish assemblages. Marine Ecology Progress Series, 387: 275-285. Tale contributo è stato recentemente citato come caso di studio nell’ambito del Booklet internazionale The Science of Marine Reserves (Gaines et al., 2011) di prossima pubblicazione. Un ulteriore contributo scientifico è in via di valutazione da parte della rivista internazionale Journal of the Marine Biology Association of UK, mentre altri contributi scientifici, in forma di poster o comunicazioni orali, sono stati presentati a vari congressi di carattere nazionale. 37 4. Conclusioni Questa indagine, per quel che concerne l’ER nell’infralitorale roccioso, conferma in generale i risultati ottenuti negli anni precedenti presso l’AMP Tavolara-Punta Coda Cavallo. Nello specifico, l’ER è stato osservato esplicarsi sia in termini di densità, sia di taglia dei pesci e quindi, complessivamente, anche in termini di biomassa. A livello di struttura dei popolamenti (i.e. composizione in taxa e contributo relativo alla densità e biomassa), è stato osservato che sostanzialmente la zona A differisce da tutto il resto, sia in termini di densità, sia di taglia. Lo stesso pattern è stato osservato anche sulle abbondanze o biomasse totali (ottenute sommando i contributi di tutti i taxa censiti). Per quel che concerne le specie target qui usate come indicatori dell’ER (la cernia bruna, la corvina ed il sarago maggiore), tutte e tre sembrano suggerire un chiaro ER in zona A rispetto alle altre tipologie di ‘zona’ (B, C ed esterno). Cernia bruna, corvina e sarago maggiore hanno mostrato maggiori densità, taglie e biomasse in zona A. A seconda dei casi, in zona B, C ed esterno sono stati registrati valori comparabili o via via decrescenti (i.e. correlati con il livello di protezione vigente nelle diverse tipologia di zona ed all’esterno dell’AMP). Nel complesso, quindi, l’ER presso l’AMP di Tavolara-Punta Coda Cavallo sembra emergere chiaramente per le zone A. Tale ER, in aggiunta, sembra esplicitarsi soprattutto in un aumento considerevole della taglia, o meglio, nella presenza di individui di taglia molto grande solo nelle condizioni di massima protezione (i.e. in zona A). Per entrare invece nel merito di una accurata comparazione spaziale e temporale della fauna ittica tra le zone B, C ed esterno nel sublitorale sarebbero necessarie informazioni quantitative sulle tipologie di pesca permesse (vedi metodi) e sullo sforzo di prelievo complessivo. La carenza di dati quantitativi sulla pressione delle singole tipologie di pesca professionale e/o ricreativasportiva che insistono sulle zone B, C ed all’esterno dell’AMP, tuttavia, non consente di trarre conclusioni definitive. In zona B, infatti, potrebbero concentrarsi maggiormente i pescatori professionisti, così come in zona C 38 potrebbero concentrarsi i pescatori sportivi che, in assenza dell’AMP, pescherebbero anche al di fuori dei suoi confini. Questo effetto di attrazione, che sia puramente psicologico o dovuto alla maggiore abbondanza di pesce dentro l’AMP, è comunque un fenomeno sempre più comune presso le AMP e potrebbe addirittura contrastare gli stessi obiettivi di conservazione/gestione delle zone B e C (aree buffer). Un simile fenomeno potrebbe spiegare perché in alcuni anni tra zona B, C ed all’esterno dell’AMP Tavolar-Punta Coda Cavallo non emergono pattern differenti (Di Franco et al., 2009). Urge, da questa prospettiva, la necessità di avere dati quantitativi sulla distribuzione spaziale della pesca professionale e sportiva-ricreativa all’interno dell’AMP al fine di quantificare la reale pressione delle diverse tipologie di pesca e, conseguentemente, proporre adeguate misure per prevenire effetti deleteri sulla fauna ittica e la biodiversità locali. Questi aspetti sarebbero di notevole interesse per meglio gestire le zone B e C. Resta comunque il fatto che grazie alla protezione efficace (e non solo sulla carta) nelle zona A dell’AMP Tavolara-Punta Coda Cavallo (vedi Guidetti et al., 2008) l’ER si osserva molto chiaramente ed oramai da diversi anni. Il presente studio ha permesso inoltre di fornire prime indicazioni sulle potenzialità dei tratti costieri a bassa profondità (tra 0 e 3 m di profondità circa) come habitat nursery per molte specie ittiche costiere. Questo risultato, sebbene i dati siano limitati nel tempo e nello spazio, suggerisce comunque che la tipologia costiera inclusa nell’AMP Tavolara-Punta Cosa Cavallo abbia probabilmente tutte le caratteristiche per essere efficiente in termini di aree nursery, data la presenza di molte baie riparate e di una ampia varietà di tipologie di habitat costieri, in grado di soddisfare le necessità di molte specie costiere (Bussotti e Guidetti, 2011 e referenze ivi contenute), alcune delle quali di rilevante interesse sia ecologico, sia socio-economico come i saraghi maggiore e fasciato (Sala et al., 1998; Bussotti et al., 2011). 39 Bibliografia Abdulla A. et al., 2008. Status of Marine Protected Areas in the Mediterranean Sea. IUCN, Malaga and WWF, France: 152 pp. Agardy T. et al., 2003. Dangerous targets? Unresolved issues and ideological clashes around marine protected areas. Aquatic Conservation-Marine And Freshwater Ecosystems 13: 353-367. Anderson M.J., 2001. A new method for non-parametric multivariate analysis of variance. Austral Ecology 26: 32-46. Bussotti S. & Guidetti P., 2011. Timing and habitat preferences for settlement of juvenile fishes in the Marine Protected Area of Torre Guaceto (south-eastern Italy, Adriatic Sea). Italian Journal of Zoology, 78, 243-254. Bussotti S. et al., 2011. Relationships between sea urchins and their predatory fishes in the Marine Protected Area Tavolara-Punta Coda Cavallo. 42° Congresso della Società Italiana di Biologia Marina, Olbia, 23-28 maggio 2011. Chapman M.G. & Bulleri F., 2003. Intertidal seawalls - new features of landscape in intertidal environments. Landscape Urban Planning 62: 159–172. Claudet J. et al., 2006. Assessing the effects of marine protected area (MPA) on a reef fish assemblage in a northwestern Mediterranean marine reserve: Identifying community-based indicators. Biological Conservation 130: 349-369. Claudet J. et al., 2008. Marine reserves: size and age do matter. Ecology Letters 11: 481-489. Denny C.M. & Babcock R.C., 2004. Do partial marine reserves protect reef fish assemblages? Biological Conservation 116: 119-129. 40 Di Franco A. et al., 2009. Evaluating effects of total and partial restrictions to fishing on Mediterranean rocky-reef fish assemblages. Marine Ecology Progress Series 387: 275-285. Francour P., 1994. Pluriannual analysis of the reserve effect on ichthyofauna in the Scandola natural reserve (Corsica, Northwestern Mediterranean). Oceanologica Acta 17: 309 -317. Gaines S. et al., 2011. Partnership for Interdisciplinary Studies of Coastal Oceans. 2011. The Science of Marine Reserves (2nd Edition, Europe): 22 pp. Guidetti P., 2002. Mediterranean MPAs: the importance of experimental design in detecting the effects of protection measures on fish. Aquatic Conservation: Marine and Freshwater Ecosystems 12: 619-634. Guidetti P., 2006. Marine reserves reestablish lost predatory interactions and cause community changes in rocky reefs. Ecological Applications, 16: 963-976. Guidetti P. & Sala E., 2007. Community-wide effects of marine reserves in the Mediterranean Sea. Marine Ecology Progress Series 335: 43-56. Guidetti P. & Claudet J., 2010. Co-management practices enhance fisheries in marine protected areas. Conservation Biology 24: 312-318. Guidetti P. et al., 2004. Living on the rocks: substrate mineralogy and the structure of subtidal rocky substrate communities in the Mediterranean Sea. Marine Ecology Progress Series 274: 57-68. Guidetti P. et al., 2005. Evaluating the effects of protection on fish predators and sea urchins in shallow artificial rocky habitats: a case study in the northern Adriatic Sea. Marine Environmental Research, 59: 333-348. 41 Guidetti P. et al., 2008. Italian marine reserve effectiveness: does enforcement matter? Biological Conservation, 141: 699-709. Guidetti P. et al., 2009. Nursery habitats for Mediterranean coastal fishes: the need for a quantitative approach. Biologia Marina Mediterranea, 16: 197-200. Guidetti P. et al., 2010. Assessing the potential of an artisanal fishing comanagement in the Marine Protected Area of Torre Guaceto (southern Adriatic Sea, SE Italy). Fisheries Research 101: 180-187. Halpern B.S., 2003. The impact of marine reserves: do reserves work and does reserve size matter? Ecological Applications 13: 117-137. Harmelin-Vivien M.L. et al., 1985. Evaluation des peuplements et populations de poissons. Méthodes et problèmes. Revue Ecologie (Terre Vie) 40: 467-539. Harmelin M. et al., 2008. Gradients of abundance and biomass across reserve boundaries in six Mediterranean marine protected areas: evidence of spillover? Biological Conservation 141: 1829-1839. Kellner J.B. et al., 2007. Fishing the line near marine reserves in single and multispecies fisheries. Ecological Applications 17: 1039-1054. Jackson J.B.C. et al., 2001. Historical overfishing and the recent collapse of coastal ecosystems. Science 293: 629-638. Lewin W.C. et al., 2006. Documented and potential biological impacts of recreational fishing: Insights for management and conservation. Reviews In Fisheries Science 14: 305-367. 42 Lloret J. et al., 2008. Spearfishing pressure on fish communities in rocky coastal habitats in a Mediterranean marine protected area. Fisheries Research 94: 8491. Lubchenco J. et al., 2007. The Science of Marine Reserves (2nd Edition, International Version). PISCO: Partnership for Interdisciplinary Studies of Coastal Oceans. 22 pp. Sala E. et al., 1998. Fishing, trophic cascades, and the structure of algal assemblages: evaluation of an old but untested paradigm. Oikos 82:425-439. Shears N.T. et al., 2006. Long-term trends in lobster populations in a partially protected vs. no-take Marine Park. Biological Conservation 132: 222-231. Stelzenmuller V. et al., 2007. Spatial assessment of benefits of a coastal Mediterranean Marine Protected Area. Biological Conservation 136: 571-583. White C. et al., 2008. Marine reserve effects on fishery profit. Ecology Letters 11: 370-379. Worm B. et al., 2006. Impacts of biodiversity loss on ocean ecosystem services. Science, 314: 787-790. 43 Appendice Autori Paolo Guidetti: nato a Genova il 31 Maggio 1969, è attualmente ricercatore in Zoologia presso l’Università del Salento (Lecce). Si è laureato in Scienze Biologiche presso l’Università di Genova ed ha ottenuto il Ph.D. in Ecologia Fondamentale presso l’Università di Lecce. E’ stato visiting scientist nel 2003 e 2004 presso il prestigioso Scripps Institution of Oceanography (University of California, San Diego, USA). Ha tenuto corsi universitari riguardanti 1) l’ecologia della fauna ittica, 2) la biologia e gestione della pesca, 3) la conservazione in ambiente marino presso le Università di Genova e Lecce/Salento. E’ stato responsabile scientifico di oltre 18 progetti nazionali ed internazionali sulle aree marine protette, con particolare riguardo per la conservazione dei popolamenti ittici e la gestione sostenibile della piccola pesca artigianale. E’ autore di oltre 150 contributi scientifici, di cui 78 pubblicati su riviste internazionali. Simona Bussotti: nata a Genova il 25 Aprile 1967, è attualmente assegnista di ricerca presso l’Università del Salento (Lecce). Si è laureata a Genova in Scienze Biologiche ed ha ottenuto il Ph.D. in Biologia Ambientale presso l’Università di Siena. Ha partecipato a numerosi progetti nazionali ed internazionali, anche con incarichi di responsabilità, nell’ambito di ricerche riguardanti studi di biocenosi di substrato duro (comprese le grotte marine) e Posidonia oceanica, valutazione dell’effetto riserva e spillover presso Aree Marine Protette, reclutamento di specie ittiche litorali in ambiente di fondo duro ed a fanerogame marine. Ha tenuto numerosi seminari presso l’Università del Salento nell’ambito di argomenti inerenti le sue ricerche. E’ autrice di 56 pubblicazioni su riviste nazionali ed internazionali. Antonio Di Franco: nato a Palermo il 24 Ottobre 1983, è attualmente assegnista di ricerca presso l’università del Salento (Lecce). Si è laureato in Risorse Biologiche Marine (laurea specialistica) presso l’Università di Palermo ed ha ottenuto il Ph.D. in Ecologia Fondamentale presso l’Università del Salento. E’ stato visiting student nel 2008 presso il CEAB-CSIC di Blanes (Spagna) e nel 2011 presso il Southern Seas Ecology Laboratory di Adelaide (Australia). Ha partecipato a numerosi progetti sulle aree marine protette, con particolare riguardo per l’effetto riserva su specie ittiche e bentoniche e sull’effetto della frequentazione turistica sui popolamenti biologici. E’ autore di oltre 30 contributi scientifici, di cui 7 su riviste internazionali. . 44