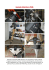Appunti RMN (fegato, vie biliari,pancreas)
Transcript
Appunti RMN (fegato, vie biliari,pancreas)
Azienda Ospedaliera di Rilievo Nazionale e di Alta Specializzazione PP.OO. “Civico e Benfratelli “, “G.Di Cristina”, “M.Ascoli” Palermo DIPARTIMENTO DI “ SCIENZE RADIOLOGICHE “ Se r v i zi o di Di a g no st i c a pe r i m m a g i ni e Ra di o l o g i a i n t e r v e nt i st i c a Ospedale Civico e Benfratelli ( Primario :Prof. Vince nzo Alessi ) Appunti di RISONANZA MAGNETICA Imaging dell’Addome Te s t o - a t l a n t e ( c o n 2 0 4 f i g u r e ) P a r t e 1 a : F EG A TO , V I E B I L IA R I, P A N C R EA S V i n c en zo A l es s i 20 0 8 AP 1 RISONANZA MAGNETICA DELL’ADDOME PREMESSA Per chi ha esperienza di tomografia computerizzata dell‟addome introdursi nello studio dell‟addome con Risonanza magnetica sarà molto facile, a condizioni che abbia approfondito preliminarmente le cognizioni di fisica, che stanno alla base della formazione del segnale RM. Non gli mancano infatti le conoscenze adeguate di anatomia e di farmacodinamica dei mezzi di contrasto di tipo interstiziale. Volendo esemplificare al massimo, nello studio dell‟addome fondamentalmente la RM ha in più rispetto alla TC la possibilità di acquisire le immagini in T2, oltre che in T1, e per questo oggi la TC , specie con le apparecchiature multidettore, si ritiene più che sufficiente a risolvere i quesiti diagnostici, lasciando alla RM il ruolo di indagine alternativa in caso di controindicazione alle radiazioni ionizzanti ed ai mezzi di contrasto organoiodati. Lo studio in T1 senza e con mdc è paragonabile alla TC sia dal punto di vista anatomico che metodologico ed interpretativo, e non da in genere ulteriori informazioni. Il mezzo di contrasto paramagnetico di tipo interstiziale ha la stessa farmacodinamica e gli stessi effetti del mezzo di contrasto organoiodato. E pertanto non comporterà alcuna difficoltà per il neofita che si appresta a questo studio. Nell‟interpretare l‟immagine in T1 bisognerà soltanto tener presente che i parenchimi hanno una intensità di segnale di tipo intermedio, i liquidi sono spiccatamente ipointensi (alla TC ipodensi) , il tessuto fibroso meno ipointenso (alla TC di densità intermedia) , il grasso invece è iperintenso (alla TC francamente ipodenso). Pertanto la differenza 2 maggiore tra TC ed RM è l‟intensità del segnale del grasso. Inoltre la presenza di alcune sostanze nei liquidi (ad es. le proteine) determina un innalzamento del loro segnale in T1 ed un abbassamento del segnale in T2. Del che se ne dovrà tener conto nell‟interpretare le immagini relative alle cisti. Analoghi problemi esistono per l‟interpretazione del sangue, la cui intensità di segnale, come vedremo, cambia in rapporto alla trasformazione dei prodotti dell‟emoglobina. Bisogna tener presente che quella in T1 è sostanzialmente un‟immagine a basso contrasto, il cui impiego è giustificato non già al fine di acquisire informazioni sui dettagli anatomici, quanto sulle modificazioni che l‟immagine subirà dopo la somministrazione del mezzo di contrasto, in caso di CE infiammatorio o neoplastico. La novità per il neofita sta nell‟utilizzazione delle sequenze pesate in T2 che sono di complemento a quelle pesate in T1. L‟immagine in T2 rispetto a quella in T1 ha un maggior contrasto ed è quindi più idonea a studiare la struttura degli organi (vedi ad es. l‟utero). Inoltre dal confronto tra le immagini in T1 e T2 ne derivano ulteriori informazioni sulla struttura del tessuto che si esamina. Infatti mentre il segnale dell‟acqua è molto basso in T1, diviene molto alto in T2, il tessuto fibroso non modifica il segnale nelle due sequenze (basso), così come il grasso (alto). Cosicché sostanzialmente la differenza di segnale tra le immagini in T1 e quelle in T2 dipende dal contenuto in acqua delle strutture anatomiche. Questa valutazione, di tipo analogico consente all‟operatore di interpretare le immagini, a differenza che in TC dove la valutazione è molto facilitata dalla misurazione elettronica delle densità. Questa possibilità invece è negata alla RM, dove ad es. per valutare minime differenze di presa di contrasto ci si dovrà invece affidare alla sottrazione tra l‟immagine dopo contrasto e quella di base. Da quanto detto si può dedurre che, visto che l‟immagine in T1 fornisce scarse informazioni di tipo strutturale, l‟acquisizione in T2 deve essere considerata fondamentale nella diagnostica RM, perché è quella che ci da i maggiori dettagli anatomici oltre che morfologici. Questo significa che forse, in caso di mancanza di alterazioni anatomiche, si potrebbe rinunciare allo studio in T1 (è proprio il caso dell„utero!!!!)., ricorrendovi soltanto in 3 presenza di reperti patologici evidenziati in T2, per poter ad es. stabilire infatti se una iperintensità in T2 è da attribuire a grasso (iperintenso in T1) o ad acqua (ipointenso in T1), oppure se ad ipointensità in T2 corrisponda una iperintensità in T1 (sangue). E successivamente, sulla base delle informazioni ottenute in T1, si potrà valutare l‟opportunità di ulteriori sequenze, come ad es. quelle con soppressione del grasso, o quelle dopo somministrazione del mezzo di contrasto. La possibilità di utilizzare sequenze con soppressione del grasso rappresenta una novità per il neofita. Con queste sequenze si ottiene la possibilità annullare il segnale iperintenso del grasso, sia in T1 che in T2., in modo da dimostrare che una iperintensità in T1 e T2 (tipica del grasso o del sangue) sia grasso o sangue, abbassandosi il segnale nel primo caso e rimanendo invariato nel secondo caso. Nel pancreas l‟utilizzazione della saturazione del grasso in T1 consente di esaltare il contrasto tra l‟organo e le strutture circostanti e di differenziare il tessuto normale (relativamente iperintenso) da quello che ha subito una involuzione fibrotica (relativamente ipointenso). Nel surrene la soppressione del grasso consente di dimostrare la presenza di una lesione, caratteristica dei tumori benigni rispetto ai maligni. Altra novità è la possibilità di effettuare acquisizioni cosiddette in fase ed in contrasto di fase in T1 modificando alcuni parametri della sequenza. Si ottiene una sorta di soppressione del grasso che consente di dimostrare in alcuni processi neoplastici se la lesione ha un contenuto in grasso ed è quindi benigna, come nel caso degli adenomi surrenalici. Altre novità derivano dai mezzi di contrasto. Ci si riferisce fondamentalmente a quelli epatobiliari(da utilizzare in T1) ed a quelli RES-specifici(da utilizzare in T2). Con i primi si può effettuare uno studio delle vie biliari di calibro normale (nel caso di ostruzione invece i risultati sono scarsi). Inoltre, data la loro maggiore persistenza negli epatociti si può eseguire uno studio ritardato, molto valido nella quantizzazione delle lesioni metastatiche (che non contengono epatociti e non captano il mdc) . Con i secondi (mdc captati dal sistema reticolo-istiocitario, determinanti un drastico abbassamento del segnale in T2 del tessuto normale) si ottiene una esaltazione del contrasto tra parenchima reso ipointenso e qualsiasi lesione non contenga cellule di Kuppfer (ad es. le metastasi), oppure si ottiene un abbassamento del segnale 4 in T2 anche n lesioni che contengono cellule di Kuppfer (ad l‟iperplasia nodulare focale). Nessuna differenza tra TC ed RM nelle procedure angiografiche, che come in TC si basano sulla somministrazione a bolo di mezzo di contrasto e sulla elaborazione MIP delle immagino ottenute. AA: nel consultare questi appunti si consiglia di soffermarsi attentamente sulle immagini in modo da prendere confidenza non tanto sull’anatomia, che è già ben nota, ma sul segnale delle strutture anatomiche normali e patologiche. RM FEGATO E DELLE VIE BILIARI I problemi tecnici e metodologici nella RM del fegato sono comuni a quelli relativi allo studio di organi che possono presentare artefatti da movimenti respiratori e cardiaci. In realtà lo studio del fegato è possibile nella misura in cui si utilizzano macchine adeguate, che consentano un più favorevole rapporto segnale/rumore e un adeguato contrasto (macchine ad elevata intensità del campo magnetico ed omogeneità di campo) e la possibilità di ottenere immagini praticamente prive da artefatti da movimento mediante gradienti di potenza elevata, tali da consentire l’impiego delle sequenze veloci ed ultraveloci, ad esempio le Gradient-echo (GE) e le Fast e le Turbo Spin Echo (FSE ed TSE), che consentono acquisizioni in T1 in tempi compatibili con l’apnea. Ed anche con le sequenze T2 oggi è possibile ottenere immagini in tempi brevi (ad es. le cosiddette sequenze multishot Haste). I risultati dipendono fondamentalmente dalla tecnica di studio e della ottimizzazione dei protocolli. Dato l’ampio spettro di sequenze consentito dalle macchine più evolute e sofisticate, si potrebbe essere tentati di vagare nella giungla di queste sequenze, vanificando di fatto quanto è possibile ottenere dalla velocizzazione delle acquisizioni (la rapidità dell’esame), ed in sostanza producendo 5 un eccessivo ed ingiustificato allungamento delle indagini, che diventano intollerabili per il paziente. Bisogna avere la consapevolezza che l’indagine RM normalmente segue altre procedure, quali l’ecografia e la TC, e non può dunque che essere un’indagine che ricerchi semplicemente aspetti non evidenziati con le altre metodiche (ad es. lo studio con contrasto in RM non deve mirare ad acquisire informazioni sulla modalità di enhancement che risultino essere identiche a quelle già evidenziate con una TC, come nel caso dell’angioma). Pertanto in qualsiasi caso la RM deve essere effettuata quando con questa metodica si abbia la possibilità di evidenziare nuovi aspetti che servano ad avere una migliore caratterizzazione della lesione che si vuole studiare (ad es. una migliore definizione delle componenti strutturali di una lesione, liquide, fibrose,emorragiche,adipose, etc., che possa essere di qualche utilità ai fini diagnostici), oppure una maggiore possibilità di individuazione e localizzazione delle lesioni. Cosi che l’impiego dei mezzi di contrasto, soprattutto quelli cosiddetti epatospecifici ( a localizzazione epatocitaria o reticoloistiocitaria), può essere proposto solo se è in grado di dare un ulteriore contributo sia ai fini della individuazione delle lesioni, sia per quanto riguarda la loro caratterizzazione. Per quanto riguarda lo studio delle vie biliari, non v’è dubbio che la possibilità di visualizzare queste strutture senza far ricorso al mezzo di contrasto (che in radiodiagnostica non è più disponibile ) ha prospettive ed applicazioni di notevole interesse. PROTOCOLLI DI STUDIO DEL FEGATO 1.Studio in respirazione spontanea : a) con sincronizzazione dell’acquisizione alla fase d’intervallo tra espirazione ed inspirazione ( tecnica prospettica ) b) senza sincronizzazione ma con riordino retrospettivo dei dati nello spazio K (non si può tuttavia usare con le sequenze veloci) 6 Con questo protocollo si possono acquisire immagini utilizzando le classiche sequenze SE T1 e T2 pesate : T1 : TR 300-500 ms TE : il minimo consentito dall’apparecchiatura: ad es. 5 ms T2 : TR 2000-3000 ms TE : 60-140 ms In realtà le SE T2 non vengono utilizzate in quanto presentano tempi di acquisizione molto lunghi (10-15’) e difficilmente potrebbero essere esenti da artefatti da movimento. Al loro posto, nelle acquisizione in respirazione spontanea, possono essere utilizzate le sequenze Turbo e Fast Spin echo multishot, nelle quali dopo ogni TR vengono inviati più di un impulso, il che consente ( a secondo del numero degli impulsi che si decide di dare) di ridurre drasticamente il numero dei TR e dei relativi tempi che questi comportano. La riduzione dei tempi di acquisizione è proporzionale al numero di impulsi utilizzati in un TR (anche di 32 volte rispetto ai 10’ di una classica SE T2) e consente di utilizzare matrici più elevate e di migliorare la qualità dell’immagine. Ovviamente la necessità di utilizzare la sincronizzazione con le FSE e le TSE viene meno nella misura in cui si utilizzano fattori turbo (numero di impulsi tra due TR) più o meno elevati, che rendono più o meno necessario il ricorso alla sincronizzazione, piuttosto che l’esecuzione dell’acquisizione in apnea. 2.Studio in apnea E’ la tecnica oggi più usata se si dispone di sequenze veloci o ultraveloci, in grado da effettuare l’acquisizione nell’arco di 15-20 sec (come in una TC spirale) 2a.Studio in T1 : vengono utilizzate le sequenze GE (o Flash) (nella nostra machina è denominata RF Fast) con i seguenti parametri : TR < 150-175 ms , TE < 10 ms ( ad es. 4,2 ms ), FA 80-90° : tempo di acquisizione di 15-20 secondi (per 12-15 sezioni). (vedi fig.1) Questo studio viene eseguito di base e dopo MDC. 7 Altra possibilità è data dalla sequenza RF Fast con soppressione del grasso, con la quale è possibile la caratterizzazione di una lesione iperintensa all’esame di base, della quale si sospetti una componente adiposa (Fig.1b). 8 Un altro modo di dimostrare la natura adiposa di una lesione è l’utilizzo di sequenze cosiddette in phase ed out phase. Trattasi di sequenze in cui il segnale in una (in phase) è data dalla somma del segnale dell’acqua e del grasso, e nell’altra (out phase) dalla differenza tra questi due segnali. Il risultato è che in caso di componente adiposa da steatosi focale il segnale si abbassa passando dalla prima alla seconda sequenza(Fig.1c), mentre nelle lesioni che non contengono grasso intracellulare, neoplastiche o metastatiche, avviene il contrario (fig.5.1) 2b.Studio in T2 : vengono utilizzate le sequenze Fast SE single shot (un solo impulso iniziale a TR infinito e multipli TE quanti sono i passi di codifica di una riga dello spazio K) (Fig.2). Il tempo di acquisizione è di 1 sec. per ogni strato, in pratica poco meno della sequenza GE T11. 1 La sequenza GE T2 non può essere utilizzata nell’acquisizione in apnea perché avrebbe un tempo complessivo troppo lungo in rapporto alla lunga durata del TR e del TE che caratterizza la pesatura in T2. 9 Questa sequenza presenta l’inconveniente della iperintensità del tessuto adiposo che potrebbe ridurre la visibilità delle lesioni, specie quelle sottoglissoniane. Per ovviare a questo inconveniente si può ricorrere alla soppressione del segnale del grasso, e quindi adoperare la sequenza Fast SE STIR T2 (fig.3 ) . Questa sequenza, essendo caratterizzata, come ben sappiamo, dall’abbassamento del segnale del parenchima epatico, di fatto aumenta il contrasto tra il parenchima e l’eventuale lesione. L’effetto è simile a quanto si ottiene con le out-phase. 10 Fig.4. Risultato analogo a quello della figura 3 utilizzando una sequenza che impiega una diversa modalità di soppressione del grasso, ovvero la saturazione spettrale del segnale (FSE Fat Sat), migliorando la dimostrazione della lesione. In sostanza gli studi in apnea prevedono le seguenti sequenze: GE T1 (RF Fast) + FSE T2 o FSE STIR o FSE Fat sat oppure RF Fast in phase ed out phase 3.Studio senza contrasto : trattandosi di immagini statiche si deve cercare il miglior compromesso tra risoluzione, contrasto e tempi di acquisizione, cercando di ridurre al minimo gli artefatti da movimento. Quindi è possibile utilizzare tanto sequenze lente purchè in sincronizzazione, tanto le sequenze veloci. Lo studio si basa sull’acquisizione in T1 (RFFast) ed in T2 (Fast Spin-Echo). 4.Sudio con mezzi di contrasto 4a MDC interstiziale (GD DTPA) . Si tratta di un agente di contrasto che riduce il T1 dei tessuti dove si diffonde, aumentandone l’intensità del segnale (iperintensità). I 11 suoi meccanismi di diffusione sono molto simili a quelli dei mezzi di contrasto organoiodati. (Fig. 1) L’acquisizione dopo somministrazione di MDC interstiziale, analogamente a quanto avviene per la TC, deve essere di tipo veloce, in modo da coglierne le diverse fasi. Sostanzialmente la sequenza impiegata è la RF Fast T1 da utilizzare anche per effettuare l’esame di base. Dose : 0,1 mml/Kg alla velocità di 1-2 ml/sec. 4b MDC epatobiliare (GD Bopta o Multihance). Si tratta di agenti rilassanti T1 caratterizzati dalla captazione epatocitaria e la escrezione biliare. Nel caso del Multihance il mdc persiste negli epatociti dura fino a 2 ore (consentendo quindi l’impiego di sequenze meno veloci), durante la quale il parenchima normale del fegato diviene iperintensa. Il miglior rapporto tra l’enhancement del parenchima e le lesioni (che se non contengono epatociti restano ipointense) si raggiunge tra 60’ e 90’(Fig.5) La somministrazione a bolo di Multihance (Bracco) e l’acquisizione precoce, con sequenze adeguate, consente lo studio della fase vascolare della diffusione della sostanza. Di norma si utilizza la sequenza RF FAST T1W con la quale si ottengono ottime immagini del parenchima epatico, con un notevole contrasto rispetto alle aree lesionali. 12 Probabilmente questi mezzi di contrasto soppianteranno definitivamente quelli di tipo interstiziale (troppo simili nella farmacodinamica e nel tipo d’informazione a quelli della TC,che di solito è preliminare alla RM), specie la dove sia necessario definire con precisare la presenza ed il numero delle lesioni. Dato il meccanismo di captazione epatocellulare questi agenti di contrasto potrebbero essere utilizzati nella differenziazione delle lesioni che contengono epatociti ( la iperplasia nodulare focale, il nodulo di rigenerazione,l’iperplasia adenomatosa,l’adenoma e l’epatocarcinoma) da lesioni prive di epatociti (le metastasi). Ciò perché, a differenza delle metastasi, le lesioni che contengono epatociti finiscono per captare il contrasto ed a ritenerlo più a lungo del parenchima sano (lento wash out), sicchè nelle fasi tardive (dopo ore) l’intensità del segnale nelle lesioni risulta più elevata che nel parenchima sano. (fig.5.1). * *artefatto Dose : 0,05 mml/Kg di peso corporeo, a bolo o per infusione a seconda che interessino informazioni sulla fase vascolare. Per lo studio del parenchima l’acquisizione deve avvenire dopo 1 ora. 4c MDC RES specifico (Feo) . Questi agenti di contrasto si fissano nelle cellule di Kuppfer del fegato sano e nelle lesioni che contengono cellule di Kuppfer ( iperplasia 13 nodulare focale). Si tratta di agenti T2 rilassanti (superparamagnetici), che provocano una riduzione del segnale nei siti di captazione, aumentando di fatto il contrasto tra il fegato sano e le lesioni che non contengono queste cellule (Fig.6) Le sequenze da utilizzare sono quelle pesate in T2, convenzionali (SE) o veloci(TSE FSE, GE).Tra queste quelle che sono più sensibili sono le GE. Il contrasto tra la lesione ed il parenchima può essere ulteriormente migliorato utilizzando anche la soppressione del grasso (sequenza TSE STIR T2) 14 LESIONI EPATICHE BENIGNE ( diffuse ) STEATOSI EPATICA Non rappresenta, nella forma diffusa; un’indicazione all’esame RM, dal momento che l’RM “vede” male il grasso intracellulare, e non perviene agli stessi risultati della Ecografia (in termini di sensibilità) e della TC (in termini di quantizzazione), specie nel caso di aree steatosiche focali o di aree indenni da steatosi, che possono simulare lesioni di altra natura. Il grasso intracellulare della steatosi ha infatti un T1 breve e dunque ad una pesatura in T1 si ha una modesta iperintensità del fegato, che però è difficilmente valutabile. Pertanto è molto probabile che ci si trovi comunque di fronte ad una negatività del quadro RM, che tuttavia, a fronte di una positività delle altre metodiche (eco e TC), potrebbe avere il valore di avallare la presenza di aree di steatosi focale o di aree focali di risparmio da steatosi. In realtà il protocollo che normalmente utilizziamo, basantesi sul confronto tra i reperti Eco (iperecogenicità ETG + ipodensità TC nei foci di steatosi, ipoecogenicità ETG+ normodensità TC nelle aree indenni) è sicuramente affidabile e conclusivo, tanto da non richiedere il ricorso alla RM. Vi sono comunque sequenze GE cosiddette in fase o in contrasto di fase(out phase), con le quali le aree steatosiche si presentano rispettivamente iperintensa ed ipointense rispetto al parenchima sano. Questa tecnica si basa sulla adozione di un adeguati valori di TE utilizzando apparecchi ad alta intensità di campo ( tra 2,2 ms,in phase e 4,3ms out phase). Ma non si sa quanto valga la pena utilizzarle (Fig.1c). 15 Ruolo delle metodiche - protocolli diagnostici - Riconoscimento ETG Steatosi diffusa Quantizzazione follow-up Forme pseudoneoplastiche Skip area atipica Steatosi focale atipica caratterizzazione TC smdc RMN smdc Fat sat RMN mdc Steatosi focale ETG TC RMN 16 EMOCROMATOSI L’accumulo di Fe abbassa fondamentalmente il T2 , ed in misura minore il T1 (analogamente a quanto avviene dopo la somministrazione del FeO come agente di contrasto). Nelle sequenze T2 il fegato emocromatosico si presenta ipointenso, diffusamente o focalmente, ed in misura variabile a seconda del grado di accumulo. Soltanto nelle forme gravi l’ipointensità è visibile anche nelle sequenze pesate in T1. Data la difficoltà di valutare con l’RM in assoluto il segnale del fegato, per questa valutazione occorre basarsi sul confronto tra i segnali del fegato e quelli della milza. Pur essendo allo studio metodi di quantificazione RM (misura della suscettibilità magnetica con un magnetometro), tuttavia allo stato attuale la correlazione tra la quantità di ferro intracellulare (mediante biopsia) ed i dati densitometrici dell’imaging è possibile solo con la TC, anche se si tratta di una valutazione molto approssimativa. Infatti i dati densitometrici della TC sono più o meno falsati dalla variabile presenza di una componente fibrotica o edematosa nel parenchima emocromatosico. Fig.7. Emocromatosi.Sequenza T2 : notevole abbassamento del segnale del parenchima epatico da accumulo di ferro, con presenza di nodulo di HGC. 17 MORBO DI WILSON Si tratta di un accumulo di rame nel fegato a causa della difettosa sintesi della ceruloplasmina, responsabile del trasporto del Fe in circolo. Questa condizione non è svelabile né alla ETG né alla TC. Anche la RM non fornisce reperti significativi nonostante il rame sia dotato di effetto superparamagnetico, e per ciò stesso dovrebbe abbassare l’intensità del segnale del parenchima, almeno nelle sequenze T2 pesate. SINDROME DI BUDD-CHIARI Nessuna ulteriore informazione rispetto a quanto sia possibile ottenere con la TC( basale e dopo contrasto : alterazioni parenchimali ) e con l’eco-CD (alterazioni dei vasi venosi intraparenchimali). L’angio-RM potrebbe essere utile per ottenere una visione d’insieme del sistema vascolare non, per dimostrare le cause di ostruzione al livello della vena cava inferiore (trombi, membrane o altro ) e la presenza di circoli collaterali. EPATITI Nessuna indicazione nelle forme croniche, sia per quanto riguarda i segni intraparenchimali, sia per quanto riguarda i segni associati ed accessori (ipertensione portale, splenomegalia, ascite). Forse qualche utilità nello studio dei circoli collaterali. Scarsa indicazione nelle forme acute, dove la riduzione dei tempi di rilassamento T1 e T2, a causa dell’edema infiammatorio, con riduzione del segnale in T1 ed accentuazione in T2, in pratica sono scarsamente percepibili ed utilizzabili ai fini diagnostici. CIRROSI Vale il discorso precedentemente fatto per le epatiti croniche. E’ comunque da segnalare un aspetto ritenuto significativo, consistente nella possibilità di dimostrare, soltanto nelle forme gravi, una iperintensità parenchimale da infiltrazione lipidica del fegato, che risulta anche aumentato di volume. Tale condizione forse potrebbe 18 essere rilevata anche alla TC, ma , a mio avviso, non costituisce di per se un’indicazione all’esecuzione di un esame RM. Si ammette che la RM abbia una maggiore possibilità di dimostrare i noduli di rigenerazione (Fig.8). Alla TC detti noduli possono presentarsi moderatamente iperintensi all’esame di base. Nelle sequenze pesate T2 (maggior contrasto) sia SE che GE alcuni noduli contenenti emosiderina (la cui frequenza è del 25%) sono visibili perché ipointensi. LESIONI EPATICHE BENIGNE ( focali ) CISTI Conosciamo bene le caratteristiche morfologiche delle cisti (pareti regolari e contenuto liquido). Il contenuto liquido (T1 e T2 lunghi) fa si che la lesione appare fortemente ipointensa in T1 e fortemente iperintensa in T2. (Fig.2a) Il grado di ipointensità marcata ed omogenea in T1 è di per se inequivocabile, tanto da chiedersi quanto sia necessaria l’ulteriore pesatura in T2 per la diagnosi. Lo studio con mdc è invece sempre necessario per escludere che trattasi di angioma. 19 Se il contenuto è emorragico il segnale si modifica in rapporto alle varie fasi di degradazione dell’emoglobina (iperintensità T1 e T2 da emoglobina nel sanguinamento precoce, ipointensità da emosiderina in T1 e T2 ), permettendo di valutare l’età del sanguinamento. Ovviamente nelle cisti non vi è enhacement dopo MDC. Inoltre la RM non dimostra le calcificazioni parietali. E’ da ricordare in caso di cisti multiple, spesso vi è la coesistenza di cisti a carico della milza e dei reni (policistosi epato-renale). Le cisti epatiche però in genere sono di tipo sieroso, mentre quelle renali hanno aspetto multiforme , potendo avere un contenuto emorragico o proteico. (Fig.93) Nella cisti da echinococco la diagnosi si basa sugli aspetti multiloculari e sulla dimostrazione di una membrana (pericistio), di spessore fino a 4 mm, che è tessuta da connettivo fibroso (T1 lungo e T2 breve ) che appare alla RM ipointensa sia in T1 che in T2. (fig.9A). Fig.9A - CISTI IDATIDEA. Acquisizione in T2. Presenza di parete ipointensa (fibrosa) e contenuto iperintenso disomogeneo. Un aspetto particolare si riscontra nella micropolicistosi epatica. Si tratta in realtà di una amartomatosi nella quale sono presenti numerose immagini cistiche di dimensioni millimetriche, per la cui valutazione ci si può valere di una rappresentazione panoramica mediante CPRM. (Fig.9B). Spesso vi si associano immagini analoghe in sede renale e pancreatica 20 Fig.9B . AMARTOMATOSI EPATICA (m. di Von Meyenburg) . CPRM:numerose cisti di dimensioni millimetriche (frecce). ASCESSO Come nella TC l’ascesso si differenzia dalla cisti per la irregolarità delle sue pareti, ben visibile in T1. In T2 tuttavia si osserva un aspetto caratteristico della parete, che è composta da uno strato interno ipointenso, e da un alone esterno iperintenso determinato dall’edema parenchimale circostante la raccolta La somministrazione di MDC interstiziale dimostra un enhancement della parete: Questa però manca nell’ascesso amebico. L’evoluzione fibrocicatriziale dell’ascesso viene documentata dalla scomparsa delle iperintensità T2 della raccolta ascessuale, al cui posto resta un’area ipointensa T2 (fibrosi.) 21 ANGIOMA A titolo esemplificativo l’angioma ha un comportamento RM simile alla cisti, differendone soltanto per l’aspetto dei margini : T1 e T2 lunghi e quindi spiccata ipointensità in T1 e spiccata iperintensità in T2. Negli angiomi l’iperintensità in T2 viene tipicamente mantenuta elevata anche in caso di aumento della pesatura T2 (TE>120 ms). Ma questi aspetti li ritroviamo ugualmente nelle metastasi ipervascolarizzate. Il ricorso alla somministrazione del MDC di tipo interstiziale (Ga.DTPA) ripropone gli aspetti già conosciuti alla TC (enhancement nodulare periferico precoce con successivo riempimento centripeto, possibilità di aree centrali di mancato enhacement da fibrosi o trombosi) (fig.10 e 10b). Le stesse sono le problematiche diagnostiche (indistiguibilità dalle metastasi ipervascolari qualora l’enhancement sia precocemente omogeneo). 22 Un aspetto particolare, che attualmente viene ritenuto patognomonico si osserva paragonando le immagini T2 pesate prima e dopo somministrazione di MDC RES specifico (superparamagnetico) : nelle immagini T2 dopo mdc si osserva una discreta riduzione del segnale nell’angioma che può spiegarsi con una captazione dell’agente di contrasto da parte delle cellule reticoloendoteliali dell’angioma (Fig.11). 23 Sembra infatti che questo comportamento non si osservi negli epatocarcinomi e nelle metastasi ipervascolari. Sicchè questo procedimento potrebbe rappresentare un utile contributo alla diagnosi. Probabilmente , per un uso razionale delle metodiche, si dovrebbe operare nel modo seguente : a) sospetto ecografico di grosso angioma TAC senza e con mdc alla ricerca del tipico comportamento dell'angioma b) sospetto ecografico di piccolo angioma RMN T1+T2 seguita da studio con RES in T1 e T2. c) Enhacement TC atipico (precoce omogeneità) RMN T1 e T2 seguita da RES in T1 e T2. IPERPLASIA NODULARE FOCALE (FNH) Ricordiamo il nesso tra questa lesione ed il sesso femminile, l’età (20-50 anni), e l’assunzione prolungata di estroprogestinici. La lesione ha una struttura stellata con tralci di tessuto connettivo che dal centro, dove esiste una sorta di cicatrice (scar) si irradia verso la periferia. Nello scar centrale si annida un peduncolo vascolare. All’interno della struttura vi sono epatociti stipati, misti a cellule di Kuppfer, sinusoidi e dotti biliari, come in un fegato normale. Nel contesto della lesione si possono riscontrare aree di necrosi e di emorragia. La lesione è dimensionalmente ed istologicamente stabile nel tempo, non suscettibile quindi di evoluzione neoplastica. Come tale non ha un’indicazione chirurgica, e per questo pone problemi di diagnostica differenziale con l’adenoma, il carcinoma fibrolamellare e l’epatocarcinoma, che hanno indicazioni rigorosamente chirurgiche o comunque ablative. Il problema diagnostico nasce però solo in mancanza degli aspetti tipici delle FNH. La lesione FNH di solito in condizioni basali, sia in T1 che in T2, è scarsamente differenziabile dal parenchima circostante (Fig.5.1), e la possibilità di differenziazione è correlata all’intensità di campo del magnete: quando distinguibile la lesione è moderatamente ipointensa in T1, con possibile presenza di una piccola area di lieve iperintensità e in T2 (da riferire allo scar centrale) (Fig.12). L’acquisizione in T1 out phase, a confronto con quella in phase, può mostrare la lesione con il tipico aspetto dello scar centrale (presente tuttavia soltanto nel 50% dei casi) , che si distingue dal tessuto patologico circostante per la maggiore ipointensità in T1 24 (Fig.5.1,12). Quando visibile lo scar centrale si presenta come una maggiore iperintensità in T2. Questo aspetto non si ritrova in nessuna altra lesione. L’aspetto descritto in T2 può essere ulteriormente esaltato dalla somministrazione di mdc RES specifico, che oltre ad accentuare l’iperintensità dello scar centrale, riduce il segnale sia della lesione che del parenchima sano circostante. Ciò è da ascriversi alla presenza di cellule di Kuppfer nel contesto della lesione. Dopo MDC di tipo interstiziale la lesione si presenta precocemente iperintensa ( con aspetto talvolta a ruota di carro), per poi divenire isointensa con il parenchima sano. Di contro lo scar centrale presenta un comportamento opposto alla lesione, in quanto resta ipointenso in fase precoce, per poi divenire iperintenso in fase venosa, segno che il peduncolo vascolare all’interno dello scar rappresenta lo scarico venoso della lesione. Gli aspetti descritti a proposito del comportamento della scar sia nella acquisizione di base che dopo mdc sono patognomonici. Un ulteriore contributo potrebbe essere dato dall’impiego dei mezzi di contrasto epatobiliari, che pur non fornendo aspetti peculiari nell’FNH, tuttavia possono inquadrare la lesione tra quelle che contengono epatociti. Utilizzando il mdc epatobiliare sembra tipico il comportamento dell’FNH, che presentando un lento wash-out del mdc dagli epatociti, fa riconoscere la lesione nell’acquisizione a 3 ore, allorquando essa si presenta iperintensa rispetto al parenchima circostante. Ciò suggerisce l’opportunità d’impiego di questo mdc sin dall’inizio nel sospetto di un FNH, dal momento che viene consentito di individuare non solo l’enhancement in fase arteriosa ed il successivo decremento del segnale, ma soprattutto l’enhancement a 3 ore dalla somministrazione del mdc, con possibilità di dimostrare anche lo scar ipointenso centrale (Fig.12). Altri contributi potrebbero derivare dall’impiego dei mdc RES specifici. Questi mdc hanno infatti presupposti d’impiego analoghi a quelli della medicina nucleare (la captazione del contrasto superparamagnetico così come dei radiofarmaci di tipo colloidale da parte del fegato) e dovrebbero rendere indistinguibili dal fegato sano la lesione evidenziata all’esame di base, per il fatto che questa capta l’agente di contrasto e riduce egualmente il suo segnale. Tuttavia allo stato attuale sembra che questi presupposti comuni non abbiano consentito risultati paragonabili a quelli della medicina nucleare. 25 Da notare nella fig.12 l’iperintensità della colecisti nell’acquisizione a 3h dovuta alla escrezione biliare del mdc. In caso di aspetto non tipico ( che si ritrova più frequentemente nelle lesioni di piccole dimensioni) si pone il problema di diagnosi differenziale con tutte le lesioni che presentano un’enhancement precoce e fugace. ADENOMA Si tratta di una neoplasia benigna, ma tendente all’accrescimento ed alla degenerazione maligna, anch’essa correlata all’assunzione prolungata di estroprogestinici. Anche questa lesione, coma la FNH, è costituita da elementi del fegato normale (cellule di Kuppfer, sinusoidi, dotti biliari ) oltre ad epatociti ben differenziati, ma disposti in modo disordinato. A differenza della FNH e dell’epatocarcinoma la vascolarizzazione di questa lesione è scarsa. 26 La lesione quando è distinguibile dal parenchima sano ha di base gli stessi caratteri della FNH (lieve ipointensità in T1 e lieve iperintensità in T2). Come la FNH può presentare aree intralesionali di necrosi (ipointense in T1, iperintense in T2) o di emorragia ( iperintense in T1 e T2 se sono recenti, ipointense in T1 e T2 se di vecchia data). Inoltre è presente, come nell’epatocarcinoma, una pseudocapsula , che appare ipointensa in T1 e T2. Anche questa lesione può avere uno scar centrale (in circa il 30% dei casi). Pur avendo aspetti molto simili le differenze tra FNH ed adenoma sono evidenti nei casi tipici: infatti lo scar centrale dell’adenoma non ha una componente vascolare e quindi resta ipointenso T2 basale ed in T1 dopo MDC. La presenza dello scar centrale serve anche a differenziare le due lesioni tra loro, e rispetto a quelle lesioni che scar non hanno pur avendo lo stesso comportamento contrastografico (carcinoma fibrolamellare ed epatocarcinoma). Dopo MDC la lesione si presenta precocemente e disomogeneamente iperintensa, ma rispetto alle altre lesioni che contengono epatociti, ha un wash out, che per quanto rapido, risulta più lento, restando visibile l’enhancement fino alla fase portale . Anche per l’adenoma valgono le stesse considerazioni fatte per l’impiego dei mdc RES specifici: queste lesioni infatti dovrebbero presentare una riduzione del segnale nelle T2 pesate, analogamente a quanto avviene per il parenchima sano. In mancanze di scar centrale ed in presenza di pseudocapsula perilesionale i maggiori problemi si pongono con gli epatocarcinomi ben differenziati provvisti di capsula, che presentano identico aspetto. E’ da ricordare che rispetto agli epatocarcinomi l’enhancement dopo mdc negli adenomi è meno intenso, più disomogeneo, e meno fugace. Ma si tratta sempre di aspetti inaffidabili per una sicura diagnosi differenziale. Bisogna in fondo riconoscere che il semplice dubbio tra adenoma ed epatocarcinoma, non cambia sostanzialmente il trattamento terapeutico, che deve essere rigorosamente ablativo in entrambe i casi, data la riconosciuta potenzialità degli adenomi di degenerare malignamente. 27 IPERPLASIA ADENOMATOSA (pseudo nodulo di rigenerazione) E’ una lesione macronodulare che insorge tipicamente su parenchima cirrotico. Si distingue dai noduli di rigenerazione solo per le sue dimensioni superiori. Non ha caratteristiche istologiche di malignità (la lesione è composta da piccoli epatociti), ma ha insita la possibili di degenerare malignamente. La lesione spesso si presenta moderatamente iperintesa in T1, in virtù del suo contenuto glicoproteico, mentre può risultare isointensa o moderatamente ipointensa in T2. Questo comportamento (iperintensità in T1) può essere utile per una differenziazione con le lesioni tendenti ad essere ipointense in T1, tra le quali la maggior parte degli epatocarcinomi. Tuttavia bisogna tener presente che una piccola parte di epatocarcinomi, di piccole dimensioni e ad alto grado di differenziazione, presentano un comportamento analogo (iperintensità in T1). Ciò che però contraddistingue l’iperplasia adenomatosa da tutte le altre lesioni contenenti epatociti (FNH, adenoma, epatocarcinoma) è la mancanza di enhancement precoce dopo la somministrazione di MDC. Il riscontro di aree di enhancement all‟interno di tali noduli depone per la presenza malignità. Quindi : iperintensità in T1 ( espressione di componente glicoproteica ) Iperplasia adenomatosa o epatocarcinoma differenziato Con MDC interst. : mancanza di CE nella iperplasia adenomatosa LESIONI EPATICHE MALIGNE EPATOCARCINOMA Classificazione macroscopica : - tipo nodulare (50%): - nodulo singolo - nodulo con lesione satellite - plurinodularità confluente - tipo infiltrativo (35%) - tipo diffuso ( cancrocirrosi ) 15%) 28 Il tipo nodulare è il più frequente (50% dei casi) ed caratterizzato dalla presenza di una psedocapsula peritumorale fibrosa, che si sviluppa a carico del parenchima sano, quale reazione delle cellule all’azione compressiva del tumore. Nel tipo infiltrativo questa capsula manca, probabilmente per la prevalenza dell’azione aggressiva della neoplasia rispetto alla reazione del parenchima sano. L’epatocarcinoma capsulato di solito è anche ben differenziato! Dal punto di vista istologico si distinguono diversi gradi di differenziazione. Un particolare epatocarcinoma è quello definito fibrolamellare, che predilige i pazienti giovani, senza predilezione di sesso, non si accompagna ad epatopatia cronica né ad aumento di alfafetoproteina, ha un grado di malignità inferiore, essendo nella maggior parte dei casi resecabile chirurgicamente. Il riconoscimento dell’epatocarcinoma di solito avviene nel corso dei controlli ETG cui vengono sottoposti ripetutamente i pazienti con epatopatia cronica. Ricordiamo che questa metodica può essere già diagnostica quando con l’ecoCD riesca a rilevare la vascolarizzazione centrale e periferica dell’epatocarcinoma, che denota l’ipervascolarizzazione, con presenza di alte velocità di flusso intralesionali. Alla RM di base le lesioni presentano il seguente pattern: - in genere ipointensità in T1 probabilmente legata al contenuto in acqua all’interno del tumore. Possono aversi tuttavia aspetti di isointensità o di moderata iperintensità correlati al minor contenuto in acqua o alla variabile entità di contenuto glicoproteico nel contesto della lesione (come risultato di produzione di trigliceridi e polisaccaridi da parte degli epatociti maligni), con secondario abbassamento del T1. Aree di minore ipointensità sono espressione necrosi, mentre aree d’iperintensità sono espressione di emorragia. La capsula è ipointensa e di spessore variabile da 1 a 10 mm, in rapporto alle dimensioni del tumore. - iperintensità moderata in T2 .La presenza di aree di marcata iperintensità è correlata alla presenza di aree tanto di necrosi colliquativa, che di emorragia o di 29 sinusoidi dilatati. La capsula non sempre è visibile, ma quando visibile si presenta come una sottile banda ipointensa, o come una banda a due strati, di cui l’interno ipointenso e l’esterno iperintenso determinato dai vasi disposti perifericamente unitamente a dotti biliari dislocati e compressi. AA!!: i gradi di intensità in T1 ed in T2 sono in qualche modo correlati con il grado di differenziazione della neoplasia. In generale quanto più un tumore è differenziato tanto più tende ad accentuare la sua intensità in T1 (divenendo iperintenso) e a ridurla in T2 (divenendo isointenso). Sicchè una neoplasia francamente ipointensa inT1 e più iperintensa in T2 risulta essere meno differenziata. In poche parole è come se il tessuto neoplastico differenziato avesse un T1 ed un T2 più bassi rispetto ad un tumore meno differenziato. (Fig.13) Dopo MDC di tipo interstiziale e pesatura in T1, a differenza di noduli di rigenerazione e d’iperplasia adenomatosa, che non presentano enhancement gli epatocarcinomi hanno, come nella TC, un’enhancement precoce ed intenso ( in fase arteriosa ), seguito da isointensità in fase portale, e da ipointensità in fase tardiva. La capsula resta ipointensa in fase precoce, e diviene regolarmente iperintensa in fase tardiva. (Fig.13). Questo aspetto è patognomonico e richiede l’adozione di un timing adeguato alla rilevazione del CE precoce e tutto sommato fugace. Dopo MDC di tipo epatobiliare , oltre agli aspetti rilevabili in fase vascolare, a seguito della somministrazione a bolo, assolutamente identici a quelli derivanti dall’impiego del mdc interstiziale, si rileva un’enhancement persistente anche nelle fasi tardive. Rispetto al parenchima sano, a causa del ridotto wash-out intralesionale del mdc si ha una più prolungata persistenza della iperintensità secondaria alla captazione del mdc. Dopo MDC RES specifici di solito si ottiene la dimostrazione della lesione, che appare iperintensa rispetto all’ipointensità indotta dall’agente di contrasto sul parenchima sano. Ciò naturalmente può avvenire solo nel caso di una lesione che di base si presenta isointensa rispetto al parenchima. 30 T2 L’RM è utile anche nel valutare i risultati del trattamento. Nel trattamento con alcolizzazione l’epatocarcinoma subisce una necrosi coagulativa, che è ben diversa dalla necrosi colliquativa, in quanto non contiene acqua. Pertanto al controllo dopo alcolizzazione la lesione si presenterà iperintensa in T1 e ipointensa in T2 all’esame di base. In sostanza la necrosi coagulativa presenta un comportamento speculare rispetto a quella colliquativa in ragione del differente contenuto in acqua. Di fatto con la solo sequenza T2 di base si può valutare il successo del trattamento dimostrando la necrosi coagulativa del tessuto, che sarà spiccatamente ipointenso, perché disidratato (fig.14). 31 Nei casi dubbi, dopo somministrazione di MDC, in T1 non si avrà alcun enhancement a dimostrazione della distruzione del tessuto neoplastico, o lo si avrà in caso di presenza di tessuto neoplastico residuo. Nel trattamento di termoablazione con radiofrequenza ed in quello di chemioembolizzazione i rilievi all’esame di base non sono sufficienti a definire i risultati della terapia, ma è necessario ricorrere allo studio dopo somministrazione di MDC di tipo interstiziale o epatocellulare, per dimostrare la presenza di eventuali residui di neoplasia che presentano enhancement. V’è da dire che dal momento che il lipiodol non interferisce con l’imaging dei tessuti, cosa che invece avviene per la TC, lo studio con mdc risulta più attendibile : le aree in cui si è localizzato il lipiodol risulteranno iperintense in T1 ed ipointense in T2, mentre quelle in cui persiste il tessuto neoplastico saranno relativamente ipointense in T1 ed iperintense in T2; inoltre dopo MDC si osserverà enhancement del tessuto neoplastico residuo. 32 COLANGIOCARCINOMA Si tratta di un gruppo di neoplasie a partenza dalle vie biliari comprendente vari aspetti anatomopatologici: - forme intraepatiche formanti massa (20-25%) - forme ilari e periilari periduttali infiltranti(quelli che coinvolgono la biforcazione del dotto epatico sono denominati tumori di “Klatskin”) (50-50%) - forme intraduttali (20-25%) Si tratta di tumori che a seconda della sede e delle dimensioni possono associarsi a dilatazione ostruttiva delle vie biliari, a vario livello (dotto epatico comune, confluenza dei dotti epatici, ramo dx. o ramo sn., presentandosi fondamentalmente sotto tre aspetti principali: solo massa epatica, massa epatica con ostruzione delle vie biliari a diversi livelli, solo ostruzione delle vie biliari. Nella forma intraepatica il tumore ha una morfologia irregolare e non presenta capsula. Anche in questo tumore si può osservare una cicatrice centrale e la presenza di noduli satelliti. 33 34 A parte gli aspetti alle sequenze di base ( ipointensità omogenea in T1 e moderata iperintesità disomogenea in T2) è da tener presente un aspetto ritenuto tipico del 75% dei casi colangiocarcinoma all’esame dopo mdc: nelle immagini precoci si osserva un minimo o moderato CE ad anello più o meno sottile alla periferia del tumore, con progressivo concentrico riempimento della lesione nelle immagini tardive, senza che, a differenza dell’angioma, si raggiunga un riempimento omogeneo.(Fig.15,16,17). Tale comportamento è da ascriversi alla presenza di una importante componente fibrosa stromale che trattiene il mdc più a lungo rispetto al parenchima epatico. Le forme ilari e intraduttale saranno trattate successivamente nel capitolo delle vie biliari. METASTASI Rappresentano la più frequente patologia del fegato. Possono essere più o meno vascolarizzate in relazione alla neoplasia primitiva. Ad es. ipervascolari risultano le mts da adenocarcinoma renale, da feocromocitoma , insulinoma e carcinoide. La vascolarizzazione è sempre arteriosa. All’esame di base metastasi si presentano solitamente ipointense moderatamente in iperitense in T1 T2, e non avendo dunque alcun aspetto caratteristico (Fig.18). Inoltre le metastasi ipervascolari hanno un aspetto simile a quello degli angiomi, risultando fortemente iperintense in T2. La somministrazione interstiziale ripropone di gli MDC di tipo aspetti già conosciuti alla TC ( enhancement periferico ed irregolare più o meno evidente nelle metastasi non vascolarizzate , enhancement precoce e transitorio in quelle vascolarizzate) , di per sé non portando ad alcun ulteriore contributo diagnostico (fig.19). 35 Alcuni tipi di metastasi presentano aspetti particolari. Ad es. le metastasi da melanoma spesso sono iperintense in T1 ed ipointense in T2, mentre le metastasi da tumori che producono mucina (da adenocarcinoma pancreatico) sono spiccatamente iperintese in T1. Ai fini del riconoscimento del numero lesioni sembra che migliori risultati derivino dall’impiego dei mdc epatobiliari, che aumentano notevolmente il contrasto tra parenchima sano e le lesioni metastatiche, rendendone più facile l’identificazione anche in rapporto alle ridotte dimensioni.(Fig.5). Analoghi risultati sembra possano ottenersi con i mdc RES specifici, che abbassando il segnale del fegato sano rendono maggiormente evidenti le iperdensità delle lesioni metastatiche nelle sequenze pesate in T2 (Fig.6). A tal punto che la RM con mezzi di contrasto RES specifici, con pesatura T2, forse sarà la metodica da proporre come indagine d’elezione nella valutazione preoperatoria delle metastasi epatiche. 36 DIAGNOSTICA DIFFERENZIALE : T1 Cisti Ascesso Angioma Iperplasia Nodulare Focale Adenoma Nodulo di rigenerazione Epatocarcinom a differenziato Epatocarcinom a indifferenziato Metastasi ipervascolari Metastasi ipovascolari T1+ MDC T2 T2+RES epatobiliar e acquis. 60‟ Ipointensita No CE (*) No CE Iperintensità non indicato marcata marcata Ipointensita CE perilesionale No Ce Iperintensità non indicato marcata marcata Pareti Parete ipoirregolari iper Ipointensità -CE nodulare periNo CE Iperintensità Riduzione della ipermarcata ferico con riempimarcata densità in T2 mento centripeto rispetto alla CE precoce, iperdensità in T1 omogeneo dopo MDC. non fugace -Ipointensità CE precoce, CE - Isointensità lesione lieve di omogeneo tardivo Iperintensità - Iperdensità scar lesione fugace (++) lesione moderata les. -Ipointensità - CE tardivo scar marcata scar Iperintensità marcata scar - Isointensità CE precoce, CE - Isointensità lesione -ipointensità omogeneo tardivo Iperintensità - ipointesità scar lieve les. fugace (+) lesione moderata les. capsula - NO CE scar ipoint. Iperintensità eventuale marcata scar scar ipointenso -Iperintensità NO CE CE -Ipointensità Isointensità lesione lieve tardivo lieve -Isointensità -Isointensità -Iperintensità - CE capsula CE -Ipointesità Isointensità lesione -Isointensità tardivo -Isointensità -Ipointensità CE precoce, -Capsula omogeneo Iperintensità ipoin. fugace (+++) lesione - Capsula ipo o stratificata ipo-iper Iperintensità Iperintensità lesione - Ipointensità - Ipointensità T1+MDC interst Minor fugacità nelle MTS - Iperdensità ( melanoma , T. - No CE precoce secer.mucina) - Ce tardivo Ipodensit à Ipodensit à -Iperintesità marcata Aumento del - Ipointensità contrasto moderata lesione/parenchima Iperintensità moderata (*) CE = contrast enhancement 37 1. LESIONI IPERINTENSE IN T1 : - NODULO DI RIGENERAZIONE - EPATOCARCINOMA DIFFERENZIATO - MTS (da melanoma o cistoadenocarcinomad del pancreas secernente mucina) Sono tutte ipointense in T2. Si differenziano in quanto l’epatocarcinoma differenziato è di solito provvisto di capsula. Fondamentalmente però la differenziazione dovrebbe basarsi sul mancato enhancement precoce con mdc di tipo interstiziale da parte del nodulo di rigenerazione, e sulla mancata presa di contrasto tardiva con mdc epatobiliare da parte delle metastasi. In pratica in mancanza della capsula, che orienta subito verso l’epatocarcinoma ( e l’adenoma) è da proporsi immediatamente lo studio con mdc epatobiliare, che dovrebbe essere di tipo bifasico: nella fase arteriosa (25’ dal bolo) si tende ad individuare il CE precoce e fugace , che depone per l’epatocarcinoma ( e non per il nodulo di rigenerazione); nella fase tardiva (60’) il mancato CE della lesione depone per la metastasi 2.LESIONI CON SCAR INTRALESIONALE : - IPERPALSIA NODULARE FOCALE - ADENOMA Lo scar è ipointenso in T1 in entrambe le lesioni. In T1 postcontrasto ed in T2 senza MDC invece : FNH Adenoma Scar iperintenso Scar ipointenso 3.LESIONI CON PSEUDOCAPSULA : - ADENOMA - EPATOCARCINOMA DIFFERENZIATO Nell’adenoma (30% dei casi ) presenza di scar intralesionale. L’adenoma,poichè è meno vascolarizzato dell’epatocarcinoma, ha un’enhancement meno intenso, disomogeneo e meno fugace. 38 4.LESIONI CON PRESA DI CONTRASTO PRECOCE : - ANGIOMA ATIPICO - FNH atipico (senza scar) - ADENOMA ATIPICO (senza scar né capsula) - EPATOCARCINOMA senza capsula - METASTASI IPERVASCOLARI Gli angiomi che non presentano il caratteristico enhancement periferico a gettoni e ad andamento centripeto e gli epatocarcinomi hanno un enhancement più intenso rispetto alle altre lesioni. L’enhancement degli angiomi è però meno fugace. La FNH ha un enhancement intenso e precoce, ma disomogeneo, con aspetto talvolta a ruota di carro. Le altre lesioni hanno un enhancement meno intenso e meno fugace. Con il mezzo di contrasto epatobiliare si possono differenziare le lesioni che contengono epatociti (FNH, Adenoma, Epatocarcinoma) da quelli che non li contengono (angiomi e MTS ipervascolari) Infine con il mdc RES specifico gli angiomi, rispetto alla MTS, presentano una caratteristica riduzione della iperintensità in T2 rispetto alla iperintensità in T1 dopo MDC. STUDIO DELLE VIE BILIARI La tecnica della colangiografia a RM consente di ottenere immagini delle vie biliari e del dotto pancreatico, simili a quelle contrastografiche, sia mediante l’utilizzo del mezzo di contrasto (Colangiografia a RM o CRM escretoria), sia senza l’utilizzo di alcun mezzo di contrasto (Colangiopancreatografia diretta o CPRM). La CRM si basa sull’innalzamento del segnale in T1 a seguito dell’escrezione di un mdc epatobiliare, Il TESLASCAN ( Manganìfodipir TriaNa o Mn-DPDP ), che, essendo eliminato per circa il 50% attraverso le vie biliari, ne consente la rappresentazione, a condizione che la funzione epato-biliare sia integra, in pratica in assenza di una situazione ostruttiva. Viene perciò utilizzato per il planing anatomico pretrapianto da donatore sano. 39 Il protocollo è quello seguente. 40 La CPRM è una nuova tecnica di imaging che consente di ottenere immagini colangiografiche, simili a quelle della Colangiopancreatografia per via Endoscopica (ERCP) ed alla Colangiografia Percutanea Transepatica (PTC) , ma senza l’utilizzo di mezzo di contrasto e senza alcuna manovra invasiva sul paziente. La CPRM è basata sull‟impiego di sequenze superveloci, fortemente pesate in T2, che determinano esaltazione del segnale dei liquidi statici normali (bile, urina, LCR) e patologici (raccolte liquide) , che vengono rappresentati in bianco rispetto ai tessuti circostanti. Il contrasto tra liquidi e le altre strutture può essere ulteriormente amplificato utilizzando impulsi che sopprimono il segnale del grasso. Dal momento che le classiche sequenze Spin Echo veloci richiedono tempi di acquisizione tra 30-60 sec., incompatibili con uno studio in apnea, sono state proposte nuove sequenze della famiglia FSE : la RARE e la HASTE. 41 La HASTE (Half-fourier Acquisition Single Shot TSE ) è quella più utilizzata perché più rapida in quanto, pur utilizzando anch‟essa un treno di 128 impulsi, acquisisce solo la metà dei passi della codifica di fase (sfruttando la possibilità di ricostruire l‟intero spazio K che viene considerato simmetrico). Il tempo di acquisizione in pratica è dimezzato rispetto alla RARE, e ciò consentirebbe di ottenere fette più sottili sulle quali poter effettuare il post-processing con tecniche MIP ed MPR. Nell‟apparecchiatura utilizzata alla Radiologia del Civico di Palermo (Marconi Ecclipse 1,5T) la Haste è denominata EXPRESS, e può essere eseguita con 128 impulsi (multislice) o con 254 impulsi (single slice). Quella a 256 impulsi viene eseguita con soppressione del grasso e viene denominata EXPRESS STIR. La soppressione del grasso in questa sequenza si rende necessaria perché trattandosi di una sola fetta, di spessore variabile da 20 a 70 mm, è necessario annullare il notevole effetto volume parziale sulle strutture ad intensità non elevata che si sovrappongono nella stessa fetta, determinando una sorta di effetto MIP con visualizzazione esclusiva delle strutture ad alta intensità di segnale (i liquidi). Alcuni, ma non noi, utilizzano anche una sequenza volumetrica Fast Spin Echo (FSE) a 64 impulsi ottenendo immagini dello spessore di 1,5-2mm. che utilizzano per una ricostruzione 3D con algoritmo MIP. Tuttavia questa metodica richiede una elaborazione più lunga e per noi è meno pratica rispetto a quella che utilizza la sequenza con Express, il cui tempo di acquisizione è di appena 4”, rapidamente ripetibile a seconda delle esigenze dello studio che si sta conducendo. 42 SFSE T2 single slice (HASTE-STIR) - Sequenza di acquisizione EXPRESS : TI:135 ms, TE 210 ms - TR 8000 ms, FT 264, matrice 512x384; soppressione grasso - Spessore slice : 20-75 mm (una sola slice) - Durata dell’acquisizione 4” - Proiezioni : a) coronali ; c) oblique; c) sagittali; d) assiali Lo spessore della singola slice va calibrato in modo da includere le strutture che si vogliono rappresentare e/o di escludere quelle che possono interferire nella rappresentazione delle vie biliari.. La metodologia da seguire è riportata qui di seguito. Si parte da una acquisizione multislice (immagine a sn. della Fig. seguente), scegliendo una immagine di riferimento sulla quale si 43 posizionare il volume d‟interesse con un orientamento ed uno spessore adeguati a rappresentare la via biliare. Nel caso mostrato sotto si otterrà un‟immagine coronale nella quale vi è una rappresentazione panoramica delle vie biliari e del Wirsung, dilatati a causa di una ostruzione distale. Fig.20 : 3 volumi d‟interesse su piani diversi in modo da dissociare le strutture (A,B,C). e corrispondenti immagini. Si può notare come l‟immagine A dimostra bene la colecisti , mentre il piano C è assolutamente necessario per dissociare la porzione terminale del coledoco e del Wirsung, che nella visione coronale (piano B) risultano sovrapposti, e migliorare la visualizzazione delle vie biliari intraepatiche. 44 Fig.21. METODOLOGIA IN CPRM. Partendo dall’immagine di riferimento assiale multislice (in alto a sn.) ed utilizzando il volume indicato tra frecce si ottiene coronale (in alto a dx.). Da questa si ottiene un’immagine assiale che dimostra bene il Wirsung . Da quest’ultima secondo il piano indicato nella figura (sagittale obliquo) si ottiene una rappresentazione sagittale delle vie biliari intra ed extraepatiche, della colecisti e di un tratto di Wirsung. Altri aspetti metodologici, comuni alle due tecniche, sono rappresentati da: 1. Eventuale somministrazione superparamagnetico segnale dei liquidi per os di un mezzo di contrasto ( a base di ferro, o succo di mirtillo) per annullare il intestinali, potenzialmente interferenti sulla rappresentazione delle vie biliari;(Fig.35) 2. Somministrazione di acqua per ottenere la contemporanea rappresentazione del duodeno. Con la CPRM il coledoco ed i dotti epatici sono interamente visibili, in condizioni normali, fino alle principali diramazioni. I dotti periferici invece sono visibili solo se dilatati. (fig.20 e 21) La colecisti, se distesa, è visibile così come il dotto cistico. Per ottenere una migliore visione della regione papillare si ricorre al riempimento del duodeno con acqua somministrata per os. (Fig.22) 45 CPRM senza mdc: indicazioni 1.Valutazione del paziente itterico 2. Studio della calcolosi biliare 3. Stenosi biliari benigne 4. Monitoraggio dei pazienti dopo colecistectomia laparoscopica 5. Anastomosi bilio-digestive 6. Neoplasie Per quanto riguarda la valutazione del paziente itterico valgono le seguenti considerazioni: A) Nella pratica clinica l‟inquadramento preliminare del paziente itterico avviene mediante l‟ETG al fine di distinguere l‟ittero medico dall‟ittero chirurgico. Questa metodica infatti è in grado di dimostrare con accuratezza molto elevata (99%) la dilatazione delle vie biliari, ma risulta invece poco efficace nella definizione della sede e la causa dell‟ostacolo. B) La CPRM può dare una definizione esatta della la morfologia delle vie biliari anche se non dilatate, indicando il calibro e la relativa estensione della dilatazione, la sede dell‟occlusione, e la morfologia dell‟arresto in base alla quale risalire alla natura dell‟ostruzione, con un‟ imaging ed una semeiotica sovrapponibili a quelle delle indagini strumentali con opacizzazione diretta delle vie biliari (ERCP, PTC, colangiografia intraoperatoria). C) Nell‟iter diagnostico del paziente itterico la CPRM può sostituire in pieno tutte le altre metodiche, in quanto individua molto meglio della ecografia la presenza di una dilatazione delle vie biliari, fornisce aspetti morfologici sovrapponibili a quelli della ERCP e PTC, ed è in grado, come la TC, di studiare le strutture circostanti alle vie biliari e di riconoscervi la presenza di processi patologici estrinseci. Le Ostruzioni di qualsiasi natura rappresentano la principale indicazione per lo studio con CPRM. L‟accuratezza diagnostica nell‟identificare un‟ostruzione (attraverso il reperto di dilatazione delle vie biliari) è notevole (91-100%), mentre risulta inferiore nell‟identificare la sede dell‟ostacolo (85%) e la sua natura. Rispetto alla PTC la RM presenta il vantaggio della 46 minore invasività, mentre rispetto alla ERCP, offre il vantaggio di una visione migliore del tratto a monte dell‟ostruzione. In ogni caso la RM rispetto alle due metodiche radiologiche predette offre la possibilità di ottenere una rappresentazione delle vie biliari più fisiologica, in quanto indenne indenne da sovradistensioni. Considerati questi risultati la RM si può proporre nel controllo dei pazienti con trapianto di fegato alla ricerca di ostruzioni a livello anastomotico ed extranastomotico, così come nel controllo delle anastomosi biliodigestive e dei drenaggi biliari, per valutare lo stato di detenzione delle vie biliari a seguito del trattamento terapeutico. Fig.22. Quadro normale. Da notare la rappresentazione anche del tratto terminale del Wirsung (freccia nell’immagine dx.) anche se sottile di calibro.La presenza di liquido ne duodeno permette di apprezzarne la plicatura e la papilla (freccia nell’immagine sn.). Fig.23. Situs inversus. Dilatazione delle vie biliari e del Wirsung da alterazione neoplastica della parete duodenale in sede papillare (freccia). 47 Nello studio della calcolosi biliare valgono le seguenti considerazioni . A) L‟ecografia è a tutt‟oggi considerata la metodica di prima scelta, ma la sua accuratezza diagnostica presenta un‟ampia variabilità (20-80%), con una sensibilità di appena il 60% , e con forti limitazioni nel caso di localizzazione nel coledoco distale. Attualmente il suo impiego è soltanto giustificato dall‟ampia disponibilità delle apparecchiature, dalla facilità di esecuzione ed i bassi costi. B) In caso di fallimento dell‟ecografia si è fatto ricorso alla ERCP. Ma questa metodica è invasiva ( morbilità del 10%,mortalità 0,4-1%). Esistono inoltre alcune condizioni in cui la ERCP non può essere eseguita (derivazioni biliodigestive, gastroresezione secondo Bilroth II, processi patologici della papilla). Inoltre i risultati iconografici non sempre sono adeguati per la diagnosi. C) La CPRM rappresenta la metodica alternativa non invasiva per lo studio della litiasi biliare. L‟elevata risoluzione di contrasto consente di discriminare in maniera ottimale le formazioni litiasiche dalla bile circostante, indipendentemente dal contenuto in Ca. I calcoli presentano assenza di segnale che si contrappone all‟iperintensità della bile, e appaiono come “difetti di riempimento” o “immagini di arresto a casco” , analogamente a quanto si osserva nella colangiografia tradizionale. L‟accuratezza diagnostica delle CPRM è elevata ( sensibilità 90%, specificità 98%), e grazie alla elevata risoluzione di contrasto è possibile identificare calcoli anche delle dimensioni di 2 mm (fig.24). 48 Fig.24.LITIASI DELLA COLECISTI E DEL COLEDOCO.La CPRM dimostra aree di assenza di segnale all’interno della colecisti (freccia bianca) ed arresto a “casco” a livello del coledoco distale (freccia verde), da litiasi. L’immagine a dx. (Haste multislice) dimostra calcolo nel coledoco (freccia verde); coesiste falda di ascite peri epatica(frecce). Fig.25. . Malattia di Caroli con litiasi. Sequenza Haste multislice. Multiple dilatazioni cistiche delle vie biliari intraepatiche, con incluse aree di assenza di segnale da litiasi(frecce). D) I limiti della metodica riguardano la valutazione delle piccole formazioni litiasiche con CPRM single slice (Haste-Stir), in quanto l‟assenza di segnale 49 dei calcoli può essere mascherata dalla iperintensità della bile. La presenza di piccoli calcoli con questa sequenza può venir sospettata anche in base ad una circoscritta e sfumata riduzione del segnale della bile, da valutare mediante il ricorso ad acquisizioni multislice. Fig.26). E‟ opportuno infatti tener presente che la CPRM a fetta spessa (Haste Stir) è molto utile per dimostrare in una visione panoramica le vie biliari a monte dell‟ostruzione litiasica, tuttavia, a causa del volume parziale correlato con lo spessore della fetta, necessita sempre l‟ integrazione con le immagini a fette sottili (Haste )(fig.26,27,28). Altro problema è il riconoscimento di bolle d‟aria dopo sfinterotomia, anch‟esse determinanti un‟assenza di segnale, che può essere risolto soltanto dimostrando la dislocazione antigravitaria di un reperto di assenza di segnale. In questo caso infatti solo la TC senza mdc può essere dirimente. Fig.26. .A(CPRM);B (Hastemultislice).Calcolosi della colecisti (freccia rossa), del cistico (freccia verde) e del coledoco. Notare la miglior definizione del calcolo del cistico e del coledoco distale nella immagine a strato sottile (B). Da notare in A il difetto riempimento indicato dalla freccia bianca, da riferire ad ipertrofia della papilla duodenale. 50 Fig.27.Calcolosi del coledoco. Importanza della integrazione tra l’immagine con CPRM Haste-Stir(fetta da 50 mm dell’immagine a sn.), che pur offrendo un’immagine panoramica delle vie biliari e del Wirsung, fa solo sospettare la presenza di alterazioni del segnale (riduzione) a livello del coledoco distale. L’immagine con Haste multislice a dx.(fetta da 6 mm) dimostra con certezza che trattasi di calcoli. Fig.28. Calcolosi del coledoco. Considerazioni analoghe a quelle della figura precedente. Notare come l’area di assenza di segnale da calcolo è sfumata in CPRM Haste-Stir, e netta in Haste. Ciò si verifica quanto più il coledoco è dilatato aumentando l’effetto volume dell’iperintensità della bile parziale sulla ipointensità della formazione litiasica. L‟integrazione tra Haste-Stir ed Haste è tanto più necessaria, quanto maggiore è il calibro della via biliare, e raggiunge il massimo nel caso della colecisti (Fig.29). 51 Fig.29. Calcolosi della colecisti Notare come nella immagine a sn (Haste-Stir da 50mm) si dimostra un grosso calcolo della colecisti (freccia vuota) e si ha una rappresentazione delle vie biliari intraepatiche e dell’epatocoledoco che hanno un aspetto normale . A dx.(Haste da 6 mm.) si evidenzia un secondo calcolo in sede infundibulare (freccia piena). E) Nella litiasi della colecisti, la CPRM non trova un ruolo in quanto l‟elevata accuratezza diagnostica dell‟Ecografia rende quest‟ultima la metodica di prima scelta. ); Alla CPRM possono sfuggire i piccoli calcoli e la sabbia biliare a meno che questa non si presenti con un aspetto pluristratificato delle bile, determinato dal differente peso specifico della microlitiasi (fig.30,31A ) o non determini un drastico e diffuso abbassamento del segnale, che tuttavia può simulare la presenza di una neoplasia,dalla quale quindi va differenziata (fig.31B). Fig.30. Sabbia biliare . ETG(a sn) ed Haste (a dx) . In ETG Aspetto a triplice strato; la bile è rappresentata dalla porzione anecogena posta in sede antigravitaria rispetto ai due strati sottostanti determinati da microcalcoli .Analogo aspetto in RM dove i due strati inferiori hanno una intensità inferiore alla bile sovrastante (sabbia sedimentata). 52 Fig.31A. Sabbia biliare . Haste : aspetto a duplice strato. La sabbia è sedimentata nella porzione declive (freccia) formando un livello con la sovrastante bile iperintensa. . Fig.31B. Sabbia biliare . Haste multislice : aspetto omogeneo. La sabbia determina un innalzamento del segnale della bile che assume una intensità di tipo intermedio, anziché essere iperintensa come le vie biliari. Questo aspetto può simulare una neoplasia. Ma in questo caso le pareti della colecisti hanno un aspetto regolare. La CPRM può però essere considerata importante nella fase preoperatoria : a) per la ricerca di una calcolosi della VBP associata (FIg.24,26) o di una concomitante papillite stenosante ai fini dell‟indicazione ad una sfinterotomia (Fig.32,33,34) ; b) per la individuazione di anomalie del cistico (corto o lungo) ; 53 Fig.32. Calcolosi della colecisti ed oddite stenosante. Haste-Stir (50mm). L’esame preoperatorio è utile a dimostrare l’indicazione alla sfinterotomia, esistendo una condizione di stenosi papillare benigna (freccia rossa), con dilatazione del coledoco e del Wirusng. Nelle Stenosi benigne (iatrogene o post-infiammatorie) la RM consente di ottenere una mappa panoramica delle vie biliari a monte della stenosi, molto utile ai fini di un intervento. Non sempre tuttavia si può affermare il carattere benigno della stenosi sulla base dell‟immaging (in questi casi sono d‟ausilio i precedenti anamnestici e la clinica ). Oltre a quella di natura infiammatoria una delle più comuni cause di stenosi benigna è quella iatrogena a seguito di interventi di colecistectomia laparoscopia . Nelle stenosi flogistiche (post-papillitiche) l‟ecografia è insufficiente. La CPRM ha invece una elevata accuratezza diagnostica, in quanto da invece un‟una adeguata rappresentazione morfologica di un albero biliare non normale (dilatazione diffusa, aspetto a becco di flauto del tratto distale), spesso associata a dilatazione del Wirsung. (fig.31,32,33). In mancanza di questo classico reperto la diagnosi si basa sulla esclusione di una calcolosi distale o di una formazione espansiva peripapillare (neoplasia duodenale, neoplasia della testa del pancreas) mediante acquisizione in T1 dell‟area d‟interesse duodenopancreatica. 54 Fig.33. Oddite stenosante. Haste multislice e CPRM Haste-Stir. Aspetto a becco di flauto della porzione terminale del coledoco. Fig.34. Oddite stenosante. CPRM. Aspetto a becco di flauto della porzione terminale del coledoco. Nel caso a sn coesiste dilatazione del Wirsung con aspetto “a corona di rosario” (freccia) tipico della pancreatite cronica. Nel caso a dx. il Wirsung è normale (frecce) 55 Nelle stenosi iatrogene (post-colecistectomia), solitamente localizzate al 1/3 medio della VBP, la CPRM permette una visualizzazione completa dell‟albero biliare, mostrando la dilatazione a monte, nonché la stenosi stessa (aspetto imbutiforme), con tendenza alla sovrastima del suo grado (Fig.35). Collateralmente la RM può dimostrare l‟assenza di tessuto patologico attorno alla via biliare in stenosi. Fig.35. Stenosi iatrogena post-colecistectomia. La stenosi ha un aspetto imbutiforme (freccia) e determina dilatazione delle vie biliari a monte. Vi è un un tratto tubo di drenaggio residuato in situ ed una raccolta liquida collaterale (freccia vuota) al tratto stenotico. 56 Fig.36. Sindrome di Mirizzi. (CPRM Haste-Stir). La colecisti litiasica esercita un’azione compressiva sull’ilo epatico, determinando la dilatazione delle vie biliari intraepatiche,un salto del coledoco prossimale e un’impronta sul tratto intermedio del coledoco, che appare disteso a causa di una papillite. stenosante (freccia vuota). Un‟altra forma, seppur rara, di stenosi benigna è quella determinata da una colecisti idropica, secondariamente a litiasi localizzata anche al cistico, con compressione del coledoco e secondaria dilatazione delle vie biliari intraepatiche (sindrome di Mirizzi). In questa forma di stenosi si determina un quadro che può essere difficilmente differenziabile da una neoplasia della via biliare principale, dal momento che l‟aspetto è quello di un “salto” dell‟epatocoledoco, laddove compresso dalla “massa colecistica” (Fig.36). Nelle Stenosi maligne la CPRM ha la possibilità di individuare la lesione intrinseca solo attraverso la morfologia del tratto stenotico (salto, irregolarità dei margini, effetto massa).(Fig.37,38,39). 57 Fig.37. Neoplasia del coledoco al di sotto della confluenza degli epatici. PCRM coronale (a sn) ed assiale(a dx). Nell’immagine coronale “salto” del tratto iniziale coledoco (freccia verde) con dilatazione a monte; coesistenza di piccolo calcolo nel coledoco distale (freccia rossa). L’immagine assiale rappresenta la normale confluenza degli epatici dimostrando che l’ostruzione è al disotto della confluenza. Con le acquisizioni assiali in T1 può inoltre essere dimostrata la formazione neoplastica. Fig.38. Neoplasia Ilare. Alla TC tessuto patologico in sede ilare da neoplasia a livello della confluenza degli epatici, con dilatazione delle vie biliari intraepatiche. Alla CPRM (Haste-Stir assiale) salto delle confluenza degli epatici (frecce) e dilatazione delle vie biliari intraepatiche. 58 Fig.39A.COLANGIOCARCINOMA . Stesso caso della Fig.15 (vedi anche studio in T1 e T1 mdc). A sn. T2 assiale che dimostra la formazione moderatamente iperintensa (freccia) e la dilatazione delle vie biliari intraepatiche. A dx. CPRM coronale (CPRM) che evidenzia il salto della via biliare a livello ilare (frecce). Fig. 39B. Colangiocarcinoma. Stesso caso della Fig.15. All’immagine in T1mdc (a sn.) massa neoplastica con relativo CE periferico e scar centrale, con segni di dilatazione delle vie biliari e noduli neoplastici satelliti (frecce vuote). All’immagine CPRM Haste-Stir coronale la massa si presenta come un’area di modesta e disomogenea iperintensità (frecce), che disloca le vie biliari intraepatiche e determina compressione e spiccata stenosi dell’epatico di sinistra(freccia vuota) e dilatazione delle vie biliari a monte. Normali il coledoco ed il Wirsung. Nell’immagine in T1mdc le vie biliari si presentano come aree di assenza di segnale(frecce) puntiformi poste perifericamente alla massa e tortuose in corrispondenza del lobo sn. 59 coronale Fig.39C.COLANGIOCARCINOMA . All’immagine Haste si nota la dilatazione delle VB intraepatiche che all’ilo presentano un salto. Le immagini CPRM coronale ed assiale danno una visione panoramica delle vie biliari che presentano un salto a livello ilare. In questo caso lo studio in T1 con mdc potrebbe dimostrare l’enhancement della neoplasia. assiale Nel caso di Carcinoma della testa del pancreas la CPRM può documentare la duplice dilatazione, che riguarda il coledoco ed il Wirsung (segno del doppio dotto) (Fig.40) o l‟aspetto allungato o compresso “a coda di topo” del tratto stenotico Fig.40A. Ostruzione del coledoco e del Wirsung da Carcinoma della testa della testa del Pancreas. La neoplasia determina stop infiltrativo a livello della confluenza del coledoco e del Wirsung con spiccata dilatazione a monte, ed effetto massa sul duodeno (freccia) . 60 Fig.40B. Ostruzione del coledoco da Carcinoma della testa del Pancreas . Aspetti differenti a livello dell’ostruzione in due casi diversi ( a sn aspetto “costretto”, a dx. aspetto compresso. Nella neoplasia della colecisti (Fig.41) la RM può essere di utile complemento all‟indagine ecografia. Il tessuto neoplastico è isointenso in T1 di base e moderatamente iperintenso in T2 di base, mentre presenta un intenso CE dopo somministrazione di mdc (Fig.41) 61 Nelle immagini Haste multislice (T2) si può avere una rappresentazione del tessuto neoplastico, che presenta intensità di tipo intermedio, ed appare come una immagine di difetto riempimento delimitato dalla bile. Con questa sequenza inoltre è possibile dimostrare l‟eventuale coesistenza di calcoli, che spesso si associano alla neoplasia (Fig.42). Fig.42. Neoplasia della colecisti con litiasi. Alla CPRM(70 mm) si nota una dilatazione delle vie biliari intraepatiche ed una immagine iperintensa composta dalla colecisti(freccia piena) e da anse intestinali ripiene di liquido (freccia vuota) MISCELLANEA Fig.43A. Colecistite acuta.All’ETG ipoecogenicità pericolecistica (teste di frecce). Alla RMT2 (Haste) :Iperintensità pericolecistica da edema flogistico. a ). Alla Haste coronale multislice (6 mm) la colecisti è occupata da tessuto neoplastico (T) ad intensità di segnale intermedia, e da un calcolo(freccia) che presenta assenza completa di segnale. Si nota dilatazione delle vie biliari intraepatiche da infiltrazione del coledoco. 62 Fig.43B. Colangite sclerosante. CPRM assiale : immagini di dilatazioni e di restringimenti delle vie biliari intraepatiche. Fig.43C. Anastomosi bilio-digestiva. CPRM coronale in fasi sequenziali : assenza di dilatazione delle vie biliari intra ed extraepatiche, che evoca un deflusso regolare. La freccia indica il punto in cui il coledoco è abboccato all’ansa intestinale. Fig.43D. Anastomosi bilio-digestiva. CPRM coronale: dilatazione delle vie biliari intra ed extraepatiche, che evoca un deflusso rallentato. La freccia indica il punto in cui il coledoco è abboccato all’ansa intestinale. 63 PANCREAS Lo studio del pancreas non rappresenta soltanto una alternativa alla TC nei casi in cui vi è controindicazione dall‟impiego dei MDC iodati, ma offre delle opportunità che saranno qui di seguito rappresentate. Fondamentalmente questo studio mira a tre obbiettivi: 1. Studio del parenchima 2.Sudio del sistema escretore 3. Studio dei vasi. Lo studio del parenchima si basa sulle acquisizioni RFFast T1 e SSFSE T2 di base ed RFFast T1 dopo mdc paramagnetico. Nelle sequenze di base,sia T1 che T2, il pancreas si presenta sostanzialmente isointenso rispetto al fegato, con aspetto ipointenso in T1 ed iperintenso in T2 del coledoco intrapancreatico e del Wirsung. Dopo mdc presenta un CE, analogamente a quanto avviene per la TC. Con il mdc si ricercano aree di alterato CE, in diminuzione (come nei tumori e nelle pancreatici focali) o in aumento (come nell‟insulinoma). 64 Una notevole opportunità è data dall‟impiego delle sequenza FSET1 o GRET1 con soppressione del grasso, con le quali si ottiene un‟esaltazione del contrasto del parenchima pancreatico (Fig.44,45) e la possibilità di evidenziare aree di ipointensità da attribuire a processi patologici, quali la fibrosi parenchimale nell‟ambito della pancreatine cronica (FIG.45), o aree d‟iperdensità di natura emorragica (Fig.46) Fig. 44 65 FSE T1 con soppressione del grasso Fig.46 66 Fig.47.Pancreas normale in FSE T2. Notare l’iperintensità del coledoco intrapancreatico (VB) e del Wirsung (W) . Ciò rappresenta il presupposto per la CPRM Fig.48. Pancreas senile in involuzione adiposa . Notare l’aumento dell’intensità di segnale del parenchima. Lo studio del sistema escretore si basa sulla CPRM (colangiopancreatografia diretta o statica), basata sull‟utilizzo di sequenze veloci T2 pesate la cui tecnica è già stata esposta a proposito dello studio delle vie biliari. Accanto a questa tecnica vi è la possibilità di effettuare studi CPRM previa somministrazione di secretina (Wirsungrafia con secretina) con la finalità di migliorare il riempimento de dotti escretori. Si tratta di uno studio seriato dopo somministrazione e.v. di 1 UI/Kg di peso corporeo) e previa somministrazione per os di un mdc superparamagnetico al fine di annullare il segnale dei liquidi i preesistenti nello stomaco e nel duodeno (Fig.49) 67 Nello studio con secretina si utilizzano sequenze ultra veloci (Haste-Stir) a fetta spessa : un‟acquisizione al minuto per 5 minuti, successivamente un‟acquisizione ogni 5 minuti. Vengono misurate le modificazioni di calibro ed il tempo necessario per il ritorno ad un calibro normale. Normalmente viene considerato patologico un ritorno alla norma oltre i 10‟. I presupposti di questo studio sono qui di seguito indicati. Fig.49. CPRM Haste-Stir. Studio con secretina. Acquisizione seriata a partire da 1’ dalla somministrazione di secretina. Notare che a 1’ si ha una migliore visualizzazione del coledoco e del wirsung, secondariamente all’ipertono dell’Oddi. Nelle successive acquisizioni fino a 5’ si assiste al progressivo riempimento del duodeno. 68 Fig.50 . Studio con secretina . Il test di capacità secretoria si considera normale allorquando il riempimento del duodeno abbia raggiunto il Treitz. Lo studio con secretina consente di mettere in evidenza l‟anomalia del sistema escretore connessa alla condizione di pancreas divisum, che rappresenta una delle condizioni predisponenti all‟insorgere di una pancreatine cronica. (Fig 51). Fig.51. Studio con secretina:Pancreas divisum (2 casi). Notare come in entrambe i casi venga migliorata la rappresentazione dei dotti.:A sn. A livello dello sbocco intrapapillare (testa di freccia); a dx. a livello del dotto accessorio(testa di freccia vuota) . 69 Infine lo studio della vascolarizzazione, che mira a rappresentare i grandi assi arteriosi (arteria e vena splenica), specie in rapporto alla presenza di patologie tumorali infiltrativi. Pancreatite cronica La pancreatite cronica (P.C) è un processo infiammatorio, caratterizzato da cronicità, irreversibilità ed evolutività, ad etiologia varia (genetica, immunologica, meccanica), che inizia con un alterato flusso del liquido pancreatico nel sistema duttale e possibile deposizione endoluminale di materiale proteico o calcifico, e successivamente coinvolge il parenchima, che va incontro progressivamente a fibrosi, atrofia ed infine ad insufficienza secretoria. Il quadro clinico evolve attraverso due fasi sequenziali : Una fase precoce (primi 5 anni) caratterizzata dalle crisi dolorose in assenza di alterazioni funzionali e morfologiche di grosso rilievo. Una fase tardiva (oltre il decimo anno) caratterizzata dalla riduzione delle crisi dolorose e dalla comparsa dei segni e sintomi clinici dell„ insufficienza pancreatica esocrina ed endocrina (malassorbimento con steatorrea, diabete), e delle complicanze della malattia. Ai fini dell‟utilizzo dell‟Imaging diagnostico è opportuna una semplificazione dei quadri macroscopici, distinguendo : • PANCREATITE CRONICA CALCIFICANTE con litogenesi intraduttale che rappresenta il 90-95% dei casi • PANCREATITE CRONICA OSTRUTTIVA, secondaria a stenosi papillari benigne o maligne, distrofia cistica delle parete duodenale, pancreas divisum, pseudocisti. • PANCREATITE CRONICA COMPLICATA cisti , pseudocisti , ostruzioni biliari, coinvolgimenti vascolari. Presupposti dell’ Imaging nella Pancreatite cronica sono : 1. le alterazioni dimensionali e strutturali del parenchima legate al processo infiammatorio, ed alla sua lenta evoluzione verso la fibrosi e l‟atrofia. 70 2. la compromissione del sistema escretore pancreatico con distorsione e dilatazione dei dotti, e deposizione endocanalicolare di sostanze proteiche che spesso calcificano (calcoli). 3. le possibili cause di ostruzione 4. la comparsa di pseudocisti o di cisti da ritenzione, con eventuale sanguinamento o suppurazione. 5. la comparsa di compromissione delle vie biliari 6. il deficit della funzione secretoria del parenchima Nello studio della P.C. la RM offre le seguenti opportunità: • Migliore valutazione del parenchima (immagini tomografiche con soppressione del grasso) • Rappresentazione simil-ERCP del sistema duttale pancreatico e delle vie biliari (CPRM : colangiopancreatografia a RM senza o con secretina) • Valutazione della capacità secretoria (test di risposta alla somministrazione di Secretina) Gli aspetti relativi alla compromissione del parenchima vengono definite tramite l‟impiego delle sequenze T1 con soppressione del grasso di cui alle Fig. 44,45 e 46,57b). Le alterazioni del sistema duttale sono messe in evidenza dallo studio con secretina. I reperti patologici ottenibili mediante la wirsungrafia dinamica sono rappresentati da: 1. scarso riempimento del duodeno (insufficienza secretoria) (fig.52) 2. restringimenti e distorsioni del dotto pancreatico (fibrosi periduttale) (Fig.52,53,54,57,58) 3. Aspetti relativi a rallentato deflusso : - effetto parenchimografico (Fig.54, 56) - aumento progressivo del calibro del Wirsung fino a 10‟ con comparsa tardiva di effetto parenchimografico (fIg.55,56) - aumento delle dimensioni delle pseudocisti comunicanti 71 FIG.52 72 FIG.53 FIG.54 73 FIG.55 FIG.56 74 Fig.57 : il restringimento (testa di freccia) è vero in quanto persiste anche dopo somministrazione di secretina, e si accompagna a dilatazione a monte(freccia verde) Notare l‟ipointensità della sezione corpo coda (tra teste di frecce) che denota la presenza di una fibrosi parenchimale. FIG.58. In caso di falso restringimento opo secretina il calibro del lume aumenta. 75 INDICAZIONI DELLA CPRM DINAMICA CON SECRETINA • • • in presenza di dotti non dilatati alla CPRM di base (pancreatiti lievi e moderate) dubbio di stenosi alla CPRM di base al fine di valutare la capacità secretoria Non indicazione e non utilità : •sufficiente nelle forme nettamente ostruttive e/o complicate, per le quali è la CPRM di base (statica) Reperti patologici alla CPRM di base 1. Dilatazione del Wirsung con aspetto a “corona di rosario” 2. Difetti di riempimento da agglomerati proteici o da calcoli 3. Cause di ostruzione ( calcoli e stenosi benigne o maligne ) 4. Cisti e pseudocisti 5. Dilatazione delle vie biliari • QUADRI TARDIVI • FORME OSTRUTTIVE • FORME COMPLICATE Rispetto alla ERCP la CPRM ha il vantaggio di rappresentare il sistema duttale senza il rischio di avere immagini da iperpressione del mdc (Fig.59) di non essere controindicata in presenza di peseudocisti (Fig.64.) 76 Fig.59. La CPRM di base(senza secretina) dimostra il reale calibro del sistema duttale e la presenza di litiasi intraduttale (frecce), a differenza dell’ERCP, nella quale la sovradilatazione da iperpressione (frecce vuote) impedisce la visualizzazione dei calcoli della sezione corpo-coda. Fig.60.CPRM Pancreatite Cronica con calcolo intraduttale. Dilatazione del dotto principale e dei dotti secondari. 77 Fig.61. P.C.con calcolo intraduttale. In A il calcolo è visibile all’esame diretto. In B (ERCP) è confermato come difetto di riempimento,ma non è opacizzato il sistema duttale a monte. In C (CPRM) il calcolo si presenta come area di assenza di segnale (freccia rossa) e, a differenza dell’ERCP, è visibile tutto il sistema duttale dilatato compresi i rami secondari. Fig.62. P.C. con Calcoli intraduttali. In A(esame diretto) concrezioni calcaree sulla proiezione della testa del pancreas. La CPRM dimostra i segni della pancreatine cronica calcifica : aree di assenza di segnale intraduttali (frecce), dilatazione del dotto principale con aspetto tortuoso e dei dotti secondari. 78 Fig.63. P.C. con Calcoli intraduttali. In A(TC) concrezione calcarea nella testa del pancreas. La CPRM preoperatoria (B) dimostra il calcolo intraduttale come area di assenza di segnale(freccia). In C il controllo post-estrazione endoscopica che dimostra il ritorno alla normalità. Fig.64. P.C. complicata da pseudocisti. S=stomaco. La CPRM Haste-Stir (70 mm) dimostra le alterazioni del Wirsung tipiche di pancreatite cronica (teste di freccia) e la presenza di una pseudocisti della coda fistolizzata (freccia), all’interno della quale vi è un’area di ridotto segnale da riferire a residuo necrotico. L’immagine Haste coronale (6 mm) dimostra che la pseudocisti è provvista di una parete ipointensa, fibrosa, aspetto che la differenzia dalle cisti . Questa condizione rappresenta una controindicazione all’ERCP. 79 Fig.65. P.C. complicata da pseudocisti. Ottima visibilità del Wirsung e di 2 pseudocisti che la RM dimostra indipendentemente dalla loro comunicazione con il sistema duttale, a differenza della ERCP, che me dimostra solo una, in quanto la seconda(freccia rossa della CPRM) non è comunicante. In questo caso però la CPRM non mostra i calcoli, visibili invece all’ERCP. Fig.66. P.C. complicata da pseudocisti. L’immagine in T1 con saturazione del grasso dimostra l’ipodensità del parenchima di natura fibrotica e la dilatazione del Wirsung.) La CPRM oltre agli aspetti della P.C. a carico del Wirsung (dilatazione e tortuosità), dimostra l’area di assenza di segnale da calcolo in sede prewateriana. Notare i segni della compressione a carico del duodeno (frecce rosse) e dello stomaco (frecce bleu). 80 Fig.67. P.C. da sbocco del wirsung in cisti da duplicazione duodenale. Immagini Haste-Stir coronale ed obliqua. CO=colecisti; VB=Via biliare; W= Wirsung; C=cisti da duplicazione. La freccia indica lo stomaco. Si tratta di un’anomalia congenita che predispone alla pancreatine cronica. Si nota che il Wirsung sbocca direttamente nella cisti ed ha un decorso tortuoso. Il reperto ha trovato conferma all’intervento. Fig.68. I limiti della RM nella P.C. calcifica : non visibilità delle calcificazioni, ben visibili invece alla TC. In realtà alla RM nel contesto della testa si notano delle piccole aree di vuoto di segnale, che potrebbero essere tanto calcificazioni quanto vasi (freccia). In conclusione nello studio della pancreatine cronica l‟imaging è scarsamente utile nelle forme iniziali, per la diagnosi delle quali ci si affida agli esami di laboratorio. Nelle forme avanzate invece l‟esame è utile. 81 L‟ecografia rappresenta l‟indagine preliminare per l‟approccio • alla malattia, ed è utile nel follow-up La combinazione tra sequenze standard e CPRM di base o, quando • necessario, dopo somministrazione di secretina offre la possibilità di valutare con un solo esame tutti gli aspetti relativi alla pancreatite cronica, ed alle sue complicanze, dando una rappresentazione del sistema duttale sovrapponibile a quella dell‟ERCP, rispetto alla quale presenta il vantaggio del mancato rischio di pancreatite , della possibilità di visualizzare anche il tratto pre-ostruttivo e gli organi addominali adiacenti, consentendo un migliore bilancio anatomico della malattia ai fini della terapia chirurgica o perendoscopica e del follow-up. La ERCP, quanto la PTC, non hanno più motivo di essere utilizzate a • fini esclusivamente diagnostici, ed il loro ruolo residuale è fondamentalmente interventistico, per il quale è ormai richiesto routinariamente l‟impiego preliminare della CPRM, per l‟apporto informativo che può dare ai fini della terapia con ERCP e per il controllo dei risultati. Pancreatite acuta La pancreatite acuta è una flogosi acuta del pancreas a genesi plurifattoriale, causata dall'attivazione enzimatica intrapancreatica, contrassegnata all'esordio da dolore addominale e aumento degli enzimi pancreatici nel sangue e nelle urine, variamente caratterizzata per gravità clinica. Al contrario della pancreatite cronica, la forma acuta, salvo esiti di lesioni necrotiche, consente la piena restitutio ad integrum. I fattori che possono essere implicati sono numerosi. I più frequenti sono rappresentati dalla litiasi biliare (16 – 70%) e dall‟alcolismo (4 – 60%). Queste due condizioni sono da sole responsabili del 60 – 90% di tutte le pancreatiti acute. La malattia comporta stadi di differente gravità di un singolo processo. I reperti possono consistere nel semplice edema pancreatico (pancreatine acuta edematosa), fino a chiazze di steatonecrosi del pancreas e delle strutture adiacenti. 82 Nei casi più gravi può comparire necrosi con maggiore o minore componente emorragica (pancreatine necrotico-emorragica). La radiografia diretta dell'addome, l'esame radiografico del torace o l'esame delle prime vie digestive con pasto baritato risultano di scarsa utilità. L'ecotomografia, la tomografia computerizzata e la risonanza magnetica consentono, con il limite del meteorismo per la prima: Conferma diagnostica della malattia Definizione morfologica del danno Valutazione del grado di diffusione peripancreatica Ricerca di complicanze Controllo evolutivo a distanza TC e RNM in linea di massima consentono di ottenere i medesimi risultati, per cui la RM dovrebbe essere considerata una metodica alternativa alla TC nei casi di controindicazione alle radiazioni ionizzanti ed ai mezzi di contrasto organoiodati. L‟esame RM si basa sulle acquisizioni T2 e T1 senza e dopo mdc, e sulla CPRM. Fig.69.Pancreatite acuta edematosa . Alla TC(a) area di ipodensità anteriormente al pancreas da raccolta liquida (frecce) . Alla RM(T2) la raccolta si presenta come area d’iperintensità. 83 Fig.70. Pancreatite acuta necrotica . Il pancreas è aumentato di volume. In T2(a) ed in CPRM (b) area d’iperintensità ,in T1md(c) area di mancato CE da riferire a necrosi. Da notare che il reperto di iperdensità parenchimale è più eclatante in CPRM, in quanto si riferisce ad una fetta dello spessore di 50 mm, piuttosto che ad una fetta di 6 mm (immagine a). Fig.71. Pancreatite acuta necrotica. Pancreas aumentato di volume con ampia area d’iperintensità (immagine assiale). Alla CPRM (sotto) si evidenza un’area d’iperintensità più marcata ed omogenea da riferire alla componente necrotica(freccia). 84 Neoplasie. Distinguiamo : a) Adenocarcinomi b) Neoplasie endocrine c) Neoplasie cistiche. Nel caso degli adenocarcinomi l‟impiego della RM è alternativo a quello della TC con le stesse finalità (riconoscimento e stadiazione) , problematiche metodologiche ed intepretative (lesioni avascolari non differenziabili dalle pancreatiti focali). Rispetto alla TC la RM ha però il vantaggio di fornire una mappa rappresentativa dei sistemi duttali (Fig.72.75) Fig.72. Neoplasia della testa del pancreas. A(TC) e B (FSET2) espanso a livello della testa del pancreas (freccia). In C (T2 Haste) visione assiale del coledoco e del Wirsumd dilatat(frecce)i. In D (T2 Haste-Stir) visione panoramica coronale che dimostra che l’espanso della testa del pancreas (bifreccia) determina stop del coledoco e del Wirsung con aspetto a canne di fucile e dilatazione spiccata, ed impronta sul duodeno (D). I tumori endocrini possono essere funzionanti o non funzionanti. Sostanzialmente la diagnostica di questi tumori si affida, come per la TC, alla dimostrazione della ipervascolarizzazione negli studi con mdc. Per quanto riguarda la DD: con gli adenocarcinomi si terrà conto delle classiche differenze dal punto di vista morfologico ( margini, dimensioni, clivaggi, crescita non infiltrante, etc.) ma anche del fatto che questi tumori nelle 85 sequenze T2 sono discretamente iperintensi, mentre l‟adenocarcinoma in questa sequenza presenta una sostanziale isointensità con il parenchima pancreatico. Fig.73. Neoplasia della testa del pancreas. Sono evidenti i segni di dilatazione del coledoco e del Wirsung e la distorsione del tratto terminale di quest’ultimo, ma non si ha alcuna evidenza diretta del processo espansivo. Fig.74. Neoplasie della testa del pancreas(tre casi diversi). Nel caso in alto a dx.(CPRM assiale) la freccia indica una formazione iperintensa corrispondente alla visibilità diretta della formazione neoplastica. 86 Fig.75. Neoplasie della testa del pancreas (2 casi A e B). Nel Caso A vi è solo dilatazione del Wirsung. Nel Caso B vi è dilatazione del wirsung e del coledoco. L’esame con mdc può dimostrare la presenza del processo espansivo (freccia) ma non vi è alcuna differenza tra una neoplasia ed una pancreatine focale. Fig.76. Neoplasia della testa del pancreas. Sequenza FSET2. l processo espansivo, a livello della testa del pancreas infiltra l’arteria mesenterica superiore. 87 Fig.77. Neoplasie della testa del pancreas. A sn. sequenza RFFAST T1mdc coronale, che individua la presenza di un processo espansivo ipointenso (avascolare) a livello della testa del pancreas (tra frecce); si notano anche due aree ipointense a livello del fegato (frecce) da riferire a MTS. L’angioRM (a dx.) dimostra l’infiltraxzione ostruente della vena mesenterica superiore(freccia), e l’attivazione dell’arcata dir Riolano (freccia vuota). Le neoplasie cistiche comprende i cistoadenomi sierosi, mucinosi ed i tumori intraduttale. Il cistoadenoma sieroso è una neoplasia invariabilmente benigna caratterizzata da piccole formazioni cistiche, che a livello macroscopico possono anche simulare una massa solida. Il cistoadenoma mucinoso ha invece un aspetto macrocistico, uniloculato o poliloculato, che, nel caso uniloculato, va differenziato da una pseudocisti esito di pancreatite acuta, fondamentalmente in base ai dati anamnestici di un pregresso processo flogistico. Le neoplasie mucinose possono essere potenzialmente maligne o originariamente maligne (cistoadenocarcinoma mucinoso). E’ importante quindi la differenziazione tra le forme sierose,benigne, e quelle mucinose, potenzialmente o originariamente maligne. Tale differenziazione comporta l’individuazione di elementi solidi a livello delle componenti liquide, facilmente acquisibile nell’immagine in T2, ed eventualmente nelle sequenze T1 con mdc in base al rilevamento di in CE patologico. Purtroppo la differenziazione tra la forma sierosa e quella mucinosa, già difficile alla TC, è altrettanto difficile alla RM. Né può 88 essere di ausilio l’intensità del segnale del liquido cistico, che nelle forme mucinose tende a risultare meno intenso. Il tumore mucinoso intraduttale è una neoplasia rara che si sviluppa all’interno dei dotti pancreatici, spesso a livello del processo uncinato. Si evidenzia come ujna dilatazione settoriale o diffusa del Wirsung, che deve essere differenziata dalle dilatazioni riscontrabili nella pancreatite cronica, il che non sempre è possibile. La diagnosi si basa sulla dimostrazione di una dilatazione circoscritta non imputabile ad una causa ostruttiva e trova conferma tramite il cateterismo del wirsung ed il prelievo del muco dalla porzione dilatata. Fig.79. CISTODENOMA MUCINOSO . Sopra un’immagine T2 assiale, sotto la CPRM coronale, dimostrano la formazione cistica tipicamente iperintensa in T2, localizzata a livello della sezione corpo-coda, senza segni di ispessimento parietali, vegetazioni endocistiche o setti. Coesiste la dilatazione dei dotti della coda del pancreas(Freccia), Anamnesi negativa per precedenti pancreatiti acute. All’intervento: cistoadenoma mucinoso. Fig.80. CISTODENOMA MUCINOSO . La presenza di vegetazioni endocistiche all’ETG indirizza verso la diagnosi di cistoadenoma mucinoso. 89 Fig.80. CISTODENOMA MUCINOSO . Le frecce indicano una formazione neoplastica, con aspetto cistico, ma con intensità di segnale inferiore a quello delle vie biliari . Tale aspetto è determinato dall’’importante componente mucinosa all’interno della cisti.All’intervento: cistoadenoma mucinoso, nonostante l’aspetto irregolare del Wirsung possa indirizzare verso una pancreatite cronica. Fig.81. CISTODENOMA MUCINOSO . CPRM. L’immagine di sn, acquisita secondo un piano OAS dimostra la formazione cistica, e la dilatazione del Wirsung, che presenta un aspetto tortuoso come da P.C. complicata da pseudocisti. L’immagine destra (piano OAD) fa valutare la porzione terminale del coledoco(freccia) e da una visione panoramica della colecisti, del cistico e delle vie biliari dilatate. La cisti è allocata nel processo uncinato,e presenta un contorno poco netto ad ore 4-6.All’intervento: cistoadenoma mucinoso 90