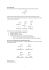Corso di Laurea in Farmacia CHIMICA BIOLOGICA Insegnamento di
Transcript
Corso di Laurea in Farmacia CHIMICA BIOLOGICA Insegnamento di
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 4 Scoperta degli amminoacidi: gli amminoacidi essenziali Gli amminoacidi essenziali sono quegli amminoacidi che un organismo vertebrato non è in grado di sintetizzare da sé in quantità sufficiente, ma che deve assumere con l'alimentazione. Nell'alimentazione umana si considerano essenziali i seguenti aminoacidi: fenilalanina, isoleucina, istidina, leucina, lisina, metionina, treonina, triptofano, valina. Arginina, cisteina, e tirosina sono essenziali durante l'infanzia e lo sviluppo. Amminoacido mg per kg peso corporeo* mg per 70 kg mg per 100 kg H Istidina 10 700 1000 I Isoleucina 20 1400 2000 L Leucina 39 2730 3900 K Lisina 30 2100 3000 M Metionina + C Cisteina 15 (totale) 1050 1500 F Fenilalanina + Y Tirosina 25 (totale) 1750 2500 T Treonina 15 1050 1500 W Triptofano 4 280 400 V Valina 26 1820 2600 *Fabbisogni raccomandati dall'Organizzazione mondiale della sanità (OMS) La struttura degli amminoacidi Concetti chiave: • I 20 amminoacidi standard condividono una struttura comune ma differiscono a livello della loro catena laterale. • Alcune catene laterali degli amminoacidi contengono gruppi ionizzabili i cui valori di pK possono variare. Gli amminoacidi proteici Le proteine (próteios, “che occupa la prima posizione”) sono la classe di macromolecole più abbondante in una cellula, rappresentando più del 50% del suo peso totale (acqua esclusa). Non c’è fenomeno biologicamente rilevante dove una o più proteine non abbiano un ruolo essenziale. Le proteine sono POLIMERI costituite da catene di α- amminoacidi Struttura degli amminoacidi La struttura di un α-amminoacido è definita da un atomo di carbonio (carbonio α) che lega: i due gruppi funzionali carbossilico ed amminico un atomo di idrogeno una catena laterale R, diversa per ciascun amminoacido. Struttura degli amminoacidi Ad eccezione della prolina e dei suoi derivati, tutti gli amminoacidi che si trovano comunemente nelle proteine possiedono una struttura di questo tipo. Gli amminoacidi proteici sono 20 La prolina ha una struttura ciclica con la catena laterale legata al gruppo amminico. E’ dunque un imminoacido, e non propriamente un α-amminoacido. La nomenclatura degli amminoacidi Struttura degli amminoacidi I 20 amminoacidi, i mattoni costitutivi della maggior parte delle proteine, possono essere classificati in base alle proprietà della loro catena laterale come: NON POLARI (IDROFOBICI) POLARI NEUTRI POLARI CARICHI (ACIDI E BASICI) AMMINOACIDI CON CATENA NON POLARE GLICINA E ALANINA GLICINA ALANINA VALINA, LEUCINA E ISOLEUCINA VALINA LEUCINA ISOLEUCINA PROLINA E METIONINA PROLINA METIONINA AMMINOACIDI CON CATENA LATERALE POLARE NEUTRA SERINA, TREONINA E CISTEINA SERINA TREONINA CISTEINA La cisteina può formare ponti disolfuro ASPARAGINA E GLUTAMMINA ASPARAGINA GLUTAMMINA AMMINOACIDI AROMATICI FENILALANINA, TIROSINA E TRIPTOFANO FENILALANINA TIROSINA TRIPTOFANO AMMINOACIDI CON CATENA LATERALE IONIZZABILE LISINA, ARGININA E ISTIDINA LISINA ARGININA ISTIDINA AMMINOACIDI CON CATENA LATERALE IONIZZABILE AMMINOACIDI CON CATENA LATERALE IONIZZABILE ASPARTATO E GLUTAMMATO ACIDO ASPARTICO GLUTAMMATO POTENZIALITA’ DI LEGAME DELLE CATENE LATERALI DEGLI α-AMMINOACIDI Le proprietà chimiche, e cioè la natura dei gruppi funzionali e le dimensioni molecolari di ciascun amminoacido, sono alla base del loro ruolo nelle proteine. Oltre ai legami covalenti che formano tra i gruppi α-carbossilici e α -amminici, gli amminoacidi hanno la capacità di interagire chimicamente tra loro, con il solvente acquoso e con altre molecole, grazie alle loro catene laterali. Tali interazioni sono in genere di tipo non-covalente e, come già detto, vengono comunemente denominate legami deboli. Legami ionici o elettrostatici Legami a idrogeno Le catene laterali degli amminoacidi possono interagire mediante: Forze di Van der Waals Interazioni idrofobiche AMMINOACIDI CON CATENA NON POLARE AMMINOACIDI CON CATENA NON POLARE AMMINOACIDI CON CATENA LATERALE POLARE NEUTRA AMMINOACIDI CON CATENA LATERALE POLARE NEUTRA AMMINOACIDI CON CATENA LATERALE IONIZZABILE ACIDI BASICI GLI AMMINOACIDI SONO IONI DIPOLARI In ciascun α-amminoacido sono presenti almeno due gruppi ionizzabili: quello α- carbossilico ed α- amminico. In condizioni fisiologiche, gli amminoacidi esistono come zwitterioni, nei quali il gruppo carbossilico ha ceduto un protone mentre il gruppo amminico ne ha acquistato uno, formando, così, un “sale interno”. La carica negativa sul carbossile è delocalizzata tra i due atomi di ossigeno. IONIZZAZIONE DEGLI AMMINOACIDI La forma cationica è presente a bassi valori di pH, quella anionica ad alti valori di pH. GLI AMMINOACIDI SONO IONI DIPOLARI Punto isoelettrico Il valore di pH al quale un amminoacido si trova nella forma con carica netta zero è detta Punto isoelettrico (pI). Per un α- amminoacido con catena laterale non ionizzabile il punto isoelettrico è la media aritmetica dei valori di pK del gruppo carbossilico e del gruppo amminico: pI=pK1+pK2 2 Valori di pH superiori al punto isoelettrico: Carica netta dell’amminoacido negativa Valori di pH inferiori al punto isoelettrico: Carica netta dell’amminoacido positiva Punto isoelettrico Per gli amminoacidi con catena laterale ionizzabile per il calcolo del pI si considerano le costanti di dissociazione delle reazioni di dissociazione a carico delle specie neutre ovvero i due pK più alti per gli aa basici e i due più bassi per gli aa acidi. CURVA DI TITOLAZIONE DELLA GLICINA CURVA DI TITOLAZIONE DELL’ISTIDINA CURVA DI TITOLAZIONE DEL GLUTAMMATO Punto isoelettrico Proprietà degli amminoacidi standard Proprietà degli amminoacidi standard Proprietà degli amminoacidi standard Proprietà degli amminoacidi standard Proprietà degli amminoacidi standard Stereochimica Concetti chiave: • Gli amminoacidi, come molti altri composti biologici, sono molecole chirali la cui configurazione può essere rappresentata con le proiezioni di Fischer. • Gli amminoacidi, nelle proteine, hanno tutti la configurazione stereochimica L. STEREOCHIMICA DEGLI AMMINOACIDI Gli atomi di carbonio α degli amminoacidi (eccetto la glicina) sono centri chirali STEREOCHIMICA DEGLI AMMINOACIDI Le molecole otticamente attive sono asimmetriche cioè non sono sovrapponibili alla loro immagine speculare. STEREOCHIMICA DEGLI AMMINOACIDI Ad eccezione della glicina, tutti gli amminoacidi sono otticamente attivi ovvero ruotano il piano della luce polarizzata. La direzione e l’angolo di rotazione possono essere misurati con un polarimetro. Proprietà ottiche degli α-amminoacidi Il senso della rotazione non ha alcuna relazione con l’appartenenza dell’amminoacido a una delle serie steriche D e L. Si possono infatti ritrovare Lamminoacidi destrogiri (+) o levogiri (-). La determinazione del potere ottico rotatorio degli amminoacidi è effettuata mediante POLARIMETRI. Il potere ottico specifico di qualunque molecola è definito da: [α]lλ = Rotazione osservata (gradi · 100) l·c l = lunghezza del cammino ottico espressa in dm; c = concentrazione del campione espressa in grammi per 100 ml di soluzione; λ = lunghezza d’onda della luce utilizzata. La misura va effettuata ad una temperatura di 20°C. La convenzione di Fischer Con la convenzione di Fisher descrive la configurazione dei centri asimmetrici. La configurazione dei gruppi intorno al centro asimmetrico è confrontata con quella della gliceraldeide che contiene un centro chirale. La L-Gliceraldeide (levo, sinistra) ruota il piano della luce polarizzata verso sinistra mentre la DGliceraldeide (dextro, destro) ruota il piano della luce polarizzata verso destra. Configurazione relativa La configurazione degli L-amminoacidi può essere correlata alla configurazione della L-gliceraldeide. CO-R-N: letta in senso orario (con H verso di noi) -NH2 = -COOH = -H = -CH2OH= - OH - CHO -H -R Configurazione relativa Nelle proteine si trovano esclusivamente gli enantiomeri L Enantiomeri della L-Alanina e D-Alanina Configurazione relativa Il sistema RS Notazione R-S di Cahn, Ingold e Prelog “Il numero atomico superiore precede quello inferiore” SH > OR > OH > NH-COCH3 > NH2 > COOR > COOH > CHO > CH2OH > C6H5 > CH3 > 3H > 2H > H 1: - NH2 2: - COOH 3: - R Configurazione S (sinister) Configurazione R (rectus) 3 3 2 1 2 1 Enantiomero con azione anti-infiammatoria L'ibuprofene è un principio attivo che rientra nella famiglia dei farmaci antinfiammatori non steroidei (FANS). Il farmaco è dotato di proprietà analgesica, antinfiammatoria e antipiretica. Solo l’enantiomero illustrato possiede azione antinfiammatoria. L'enantiomero del talidomide con effetto sedativo L’enantiomero inattivo del talidomide determina gravi malformazioni alla nascita. La sintesi organica chirale è divenuta un’area di della chimica medica oggetto di intense ricerche nell’industria farmaceutica. Proprietà degli α-amminoacidi: Assorbimento della luce La radiazione elettromagnetica è, dal punto di vista dell'elettromagnetismo classico, un fenomeno ondulatorio dovuto alla contemporanea propagazione di perturbazioni periodiche di un campo elettrico e di un campo magnetico, oscillanti in piani tra di loro ortogonali. E = h ν = h c/ λ h= costante di Plank E= Energia λ= Lunghezza d’onda 1/λ= λ -1 = Numero d’onda c = velocità di propagazione (3 x 1010 cm /sec2) ν = Frequenza = numero di onde che passano in punto per unità di tempo Proprietà degli α-amminoacidi: Assorbimento della luce SPETTRO ELETTROMAGNETICO 700 nm 340 nm Proprietà degli α-amminoacidi: Assorbimento della luce • Gli amminoacidi proteici non sono colorati, cioè non assorbono la luce nello spettro del visibile (380-780 nm), ma assorbono tutti la luce violetta (UV) a lunghezza d’onda sotto i 220 nm. • La capacità di assorbire luce UV in un campo spettrale compreso tra i 320 e i 240 nm è è una caratteristica degli amminoacidi aromatici: FENILALANINA TIROSINA TRIPTOFANO Proprietà degli α-amminoacidi: Assorbimento della luce Proprietà degli α-amminoacidi: Assorbimento della luce • La proprietà di assorbimento della luce UV da parte di Triptofano, Tirosina e Fenilalanina è particolarmente utile per il riconoscimento e la determinazione quantitativa delle proteine. • L’assorbimento di luce ad una qualunque lunghezza d’onda può essere messo in relazione con la concentrazione della sostanza assorbente mediante la LEGGE DI LAMBERT E BEER A=εcl A = assorbimento ad una determinata lunghezza d’onda; c = concentrazione della sostanza espressa in moli per litro di soluzione; l = lunghezza del cammino ottico espressa in cm; ε = coefficiente di estinzione molare (assorbimento di una soluzione 1M del composto in esame, quando questa è attraversata per 1cm dalla luce incidente). Proprietà degli α-amminoacidi: Assorbimento della luce La luce della lampada passa attraverso un monocromatore per la selezione della lunghezza d’onda. Il raggio attraversa la cella al quarzo (UV) o in vetro o policarbonato (visibile) in cui è contenuto il campione e viene registrato da un detector collegato con un registratore. Monocromatore Lenti Detector Reticoli o prismi Lampada a H o D⇒ ⇒UV Lampada ad incandescenza o filamento di tungsteno ⇒Visibile Cuvetta Campione Amplificatore Registratore La concentrazione bisogna sceglierla in modo tale che l’assorbanza non superi il valore di 2-3.