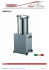Titolo: Trasformazione isobara
Transcript
Titolo: Trasformazione isobara
Titolo: La dipendenza volume – temperatura in una trasformazione isobara (legge di Volta-Gay Lussac) Strumenti e materiali • 1 pistone a basso attrito (Heat engine/Gas Law Apparatus); • 1 cilindro di alluminio con anello di supporto e tubo di collegamento lungo con 1 connettore a baionetta; • 1 piastra riscaldante con asta verticale; • 1 elemento di collegamento ortogonale (scatola Stativi-ST); • 1 becher (capacità 1000 ml); • 1 sensore di pressione assoluta e temperatura (Absolute Pressure/Temperature Sensor, per le caratteristiche vedi scheda allegata allo strumento); • 1 cavo di collegamento; • acqua; • nastro adesivo. Montaggio Disponi il cilindro a basso attrito reclinato in posizione orizzontale e chiudi, con la pinza serra-tubo, una delle due valvole. Collega l’altra al cilindro di alluminio usando il connettore a baionetta. Connetti la sonda di temperatura al sensore mediante l’attacco-jack, connetti il sensore di pressione e temperatura al Power Link. Colloca sopra la piastra riscaldante il becher riempito fino a circa 800 ml di acqua; immergi il cilindro di alluminio nell’acqua il più possibile senza tuttavia toccare il fondo del becher, bloccalo in posizione verticale servendoti dell’anello, dell’elemento di collegamento ortogonale e dell’asta fissata alla piastra riscaldante. Immergi nel becher l’ancoretta, accendi la piastra riscaldante posizionando la manopola della temperatura a 150°C, avvia anche l’agitatore magnetico con la frequenza “1”. Immergi nell’acqua nel becher il sensore di temperatura, che provvederai a fissare con un po’ di nastro adesivo evitando che tocchi le pareti sia del becher che del cilindro. (vedi foto) Procedimento Assumeremo che la temperatura dell’aria all’interno del cilindro di alluminio sia uguale a quella dell’acqua. Raccogliendo i dati in forma grafica, osserveremo la temperatura aumentare linearmente nel tempo. Per valutare il volume occorre servirsi della scala stampata sul pistone a basso attrito, in questo modo la proporzionalità tra volume e temperatura diventa una proporzionalità tra posizione (s) e temperatura (t). Per leggere la temperatura e contemporaneamente la posizione, si possono stabilire anticipatamente le letture di quest’ultima e misurare i valori di temperatura in un intervallo di ± 0,5 mm attorno al valore stabilito selezionando il tratto di grafico interessato e utilizzando le funzioni media, min, max per ricavare la migliore stima e l’incertezza assoluta come semidispersione. Risultati possono essere riportati in una tabella mediante cui verificare per via algebrica o grafica (su carta millimetrata o utilizzando il foglio elettronico o lo stesso software Data Studio) la proporzionalità tra posizione (volume) e temperatura. Risultati I risultati contenuti nella tabella seguente sono un esempio di quelli che tipicamente si ottengono; si è calcolato il volume utilizzando il diametro del cilindro (indicato sul fronte dello strumento) e come altezza la posizione letta sulla scala. Calcolati ΔV e Δt si è verificata per via algebrica la relazione di proporzionalità diretta con il metodo delle cifre significative. 2 S=π 2 d 32 ,5 mm =π =829 , 58 mm 3 ≃0, 830 cm3 2 2 S= 0, 830±0, 001 cm 3 s (mm) t (°C) V (cm3) Δt (°C) ΔV (cm3) ΔV Δt 15,0±0,5 17,0±0,5 19,0±0,5 22,0±0,5 24,0±0,5 26,0±0,5 47±1 51±1 55±1 61±1 66±1 70±1 1,2±0,1 1,4±0,1 1,6±0,1 1,8±0,1 2,0±0,1 2,2±0,1 4±1 8±1 14±1 19±1 23±1 0,2±0,1 0,3±0,1 0,6±0,1 0,7±0,1 0,9±0,1 0,04±0,01 0,04±0,01 0,04±0,01 0,04±0,01 0,04±0,01 3 cm °C isobara e temperatura. Di seguito una verifica per via grafica con Excel dellaTrasformazione relazione tra volume 2,5 f(x) = 0,0394704890387858x - 0,600945193929174 R² = 0,998916596795011 2,0 V (cm3) 1,5 1,0 0,5 0,0 45 50 55 60 t (°C) 65 70 Osservazioni Si è presentata una elaborazione algebrica dei dati di volume e temperatura (più precisamente tra ΔV e Δt, dove con ΔV si esclude il volume di aria contenuto nei tubi di collegamento). L’elaborazione grafica è stata realizzata tra V e t, dove però il volume V è sottostimato per i motivi poc’anzi ricordati; nonostante questo il valore di r= 0,999 indica un ottimo accordo con l’ipotesi di proporzionalità diretta. Per migliorare la tenuta del cilindro di alluminio e quella tra i connettori e i tubi è stato consigliato di utilizzare vaselina bianca (comeTrasformazione una sorta di grasso di tenuta economico), questa operazione non isobara è stata però compiuta. 2,5 f(x) = 0,0394704890387858x - 0,600945193929174 R² = 0,998916596795011 2,0 1,5 1,0 0,5 0,0 45 50 55 60 t (°C) 65 70 75 Titolo: La dipendenza di pressione – volume in una trasformazione isoterma (legge di Boyle) Strumenti e materiali • 1 sensore di pressione assoluta e temperatura (Absolute Pressure/Temperature Sensor, per le caratteristiche vedi scheda allegata allo strumento); • 1 siringa (portata 60 ml, sensibilità 1 ml) con tubo di collegamento corto e connettore a baionetta; • 1 cavo di collegamento. Montaggio Collega il sensore con il Power Link e la siringa con il sensore usando il connettore a baionetta. (vedi foto) Andamento della pressione in un esperimento di compressione (a sinistra) e di espansione (a destra) Procedimento In questo esperimento si suppone che la temperatura del gas si mantenga costante durante la compressione/espansione. In realtà se le trasformazioni avvengono rapidamente questo non è vero; occorre dunque procedere con una certa lentezza in modo che la temperatura rimanga costante all’interno della siringa (il comportamento della temperatura in relazione alla rapidità delle trasformazioni può essere mostrato dall’insegnante dalla cattedra con l’ausilio della “siringa della legge dei gas perfetti” – Ideal Gas Law Stringe, vedi scheda “La legge dei gas perfetti”). Prepara una tabella dove raccogliere i dati di volume (in cm3)e di pressione (in kPa). È bene stabilire preventivamente i valori del volume; una volta raggiunti mantieni il pistone fermo per alcuni secondi in modo da identificare un valore di pressione. È preferibile raccogliere i dati in forma grafica, selezionare il “pianerottolo” che il grafico forma quando la pressione è stabile e utilizzare le funzioni media, max e min per trovare la migliore stima e calcolare la semidispersione (un esempio è riportato in figura). Generalmente la semidispersione risulta minore dell’accuratezza del sensore (±2 kPa) quindi quest’ultima viene utilizzata come incertezza assoluta; per il volume si assume come incertezza la sensibilità della siringa. Preleva i dati sia in compressione sia in espansione. Risultati Le tabelle seguenti contengono esempi di dati che tipicamente si ottengono; l’incertezza del prodotto pV è calcolato con il metodo delle cifre significative. V (cm ) 60±1 55±1 50±1 45±1 40±1 35±1 30±1 3 V (cm ) 30±1 35±1 40±1 45±1 50±1 55±1 60±1 3 Compressione p (kPa) pV (cm3·kPa) 101±2 6100±100 111±2 6100±100 122±2 6100±100 135±2 6100±100 150±2 6000±100 170±2 6000±100 196±2 5900±100 Espansione p (kPa) 101±2 88±2 78±2 70±2 63±2 57±2 53±2 pV (cm3·kPa) 3000±100 3100±100 3100±100 3200±100 3200±100 3100±100 3200±100 Osservazioni Generalmente il prodotto pV tende a diminuire negli esperimenti di compressione e ad aumentare in quelli di espansione; il risultato ha questa possibile interpretazione: in compressione la pressione del gas raggiunge valore più elevati della pressione atmosferica quindi sono possibili perdite di gas, così al termine dell’esperimento si ha meno gas all’interno della siringa, quindi il prodotto PV è minore poiché è proporzionale al numero di moli; viceversa nell’espansione la pressione all’interno del pistone è minore della pressione atmosferica quindi l’aria esterna può entrare all’interno, si ha quindi un incremento di gas e PV aumenta. Resta da verificare se tali discrepanze siano dovute alla deviazione del comportamento del gas dal modello di gas ideale o occorra correggere in eccesso il volume del gas per il contributo di quello contenuto nel tubo di collegamento con il sensore (come mostrato nell’esperimento “La legge dei gas perfetti”). Alcuni risultati fanno ritenere che, se si procede troppo lentamente, aumentano le perdite di gas (o l’ingresso di gas attraverso il pistone), e che quindi occorra trovare un compromesso tra l’esigenza di procedere non troppo velocemente per mantenere costante la temperatura, né troppo lentamente per quanto appena detto. Per migliorare la tenuta del cilindro di alluminio e quella tra i connettori e i tubi è stato consigliato di utilizzare vaselina bianca (come una sorta di grasso di tenuta economico), questa operazione non è stata però compiuta. Titolo: La dipendenza pressione – temperatura in una trasformazione isocora (legge di Charles) Strumenti e materiali • 1 cilindro di alluminio con anello di supporto e tubo di collegamento lungo con connettore a baionetta; • 1 piastra riscaldante con asta verticale; • 1 elemento di collegamento ortogonale (scatola Stativi, ST); • 1 becher (capacità 1000 ml); • 1 sensore di pressione assoluta e temperatura (Absolute Pressure/Temperature Sensor, per le caratteristiche vedi scheda allegata allo strumento); • 1 cavo di collegamento; • acqua; • nastro adesivo. Montaggio Collega il cilindro di alluminio con il sensore di pressione e temperatura mediante il connettore a baionetta e la sonda di temperatura al sensore mediante l’attacco-jack, infine il sensore di pressione e temperatura al Power Link. Colloca sopra la piastra riscaldante il becher riempito di acqua fino a circa 800 ml; immergi il cilindro di alluminio nell’acqua il più possibile senza tuttavia toccare il fondo del becher, bloccalo in posizione verticale servendoti dell’anello, dell’elemento di collegamento ortogonale e dell’asta fissata alla piastra riscaldante. Metti nel becher l’ancoretta e immergi nell’acqua il sensore di temperatura che provvederai a fissare con un po’ di nastro adesivo evitando che tocchi le pareti sia del becher che del cilindro. (vedi foto) Procedimento Apri il software Data Studio e crea un grafico con la temperatura sull’asse delle ascisse e la pressione su quello delle ordinate: nel menu “Dati” clicca su “Pressione assoluta (kPa)” e trascina fino a “Grafico” nel menu “Visualizzazioni”, rilasciando comparirà una finestra con la pressione in funzione del tempo (schermo 1); clicca quindi “Temperatura (°C)” e trascina fin sull’etichetta “Tempo (s)” dell’asse delle ascisse (schermo 2), ottenendo il grafico voluto (schermo 3). schermo 1 schermo 2 schermo 3 Accendi la piastra riscaldante ruotando in senso orario la manopola di sinistra e regolandola su 150°C, avvia l’agitatore magnetico ruotando la manopola di destra nello stesso modo e posizionala su “1”. Procedi alla raccolta dei dati ciccando su “Avvia”. Quando il grafico pressione-temperatura è sufficientemente regolare (per verificarlo clicca sul tasto “Ridimensiona per adattare” in alto a sinistra nella finestra del grafico), fai ripartire la raccolta dei dati per circa 20-25 minuti. Non superare mai i 70°C che sono la portata del sensore di temperatura. Risultati Il grafico seguente rappresenta la trasformazione oggetto di studio. I dati sono stati elaborati con Data Studio per ottenere la retta di regressione: dopo averli selezionati, clicca su “Interpola” e scegli “Interpolazione lineare”. Come si vede l’accordo dei dati con una retta è ottimo e il coefficiente di correlazione r= 1. Osservazioni È possibile estrapolare i dati per ottenere l’intercetta con l’asse delle temperature, che dovrebbe avvenire allo zero assoluto. Con i dati sopra riportati: 0= mt 0 b , b 93 ,0 kPa t 0= − = − ≃ −306 ° C m kPa 0, 304 °C Per ottenere una stima migliore occorrerebbe svolgere l’esperimento su un intervallo di temperature più ampio, ad esempio da 0°C a 70°C (portata del sensore), anche se ciò è reso difficile dalla lentezza del riscaldamento (peraltro necessaria) e dal limitato tempo a disposizione. Per migliorare la tenuta del cilindro di alluminio e quella tra i connettori e i tubi è stato consigliato di utilizzare vaselina bianca (come una sorta di grasso di tenuta economico), questa operazione non è stata finora compiuta. Titolo: La legge dei gas perfetti Strumenti e materiali • 1 siringa della legge dei gas perfetti (Ideal Gas Law Syringe); • 1 sensore di pressione assoluta/temperatura (Absolute Pressure/Temperature Sensor, per le caratteristiche vedi la scheda allegata allo strumento); • 1 cavo di collegamento. Montaggio Collega la siringa con il sensore di pressione assoluta e temperatura utilizzando sia l’attacco jack (temperatura) che quello a baionetta (pressione); durante l’esperimento per variare il volume d’aria all’interno della siringa dovrai da disconnettere e riconnettere quest’ultimo. Procedimento Regola il volume iniziale del gas nella siringa a 40 cm 3 circa. Avvia la raccolta dei dati. Comprimi velocemente il gas fino a fine corsa; il volume finale dovrebbe aggirarsi intorno a 20 cm 3 . Rimani in questa posizione finché la pressione e la temperatura non hanno raggiunto un valore stabile. Occorrono circa 30 secondi affinché la temperatura ritorni pari a quella ambiente. Rilascia il pistone e attendi nuovamente che temperatura e pressione raggiungano un valore costante, il volume finale potrebbe non raggiungere i 40 cm3. Interrompi l’acquisizione dei dati. Risultati ed elaborazione Temperatura costante Seleziona un’area del grafico della pressione prima della compressione, utilizzando le funzioni media, min e max calcola la migliore stima e la semidispersione (P1); il più della volte l’accuratezza sarà maggiore di quest’ultima, pertanto assumeremo ±2 kPa come incertezza per la pressione. Annota in una tabella P1 e il volume iniziale V1. Seleziona una parte del grafico della pressione prima del rilascio del pistone (P2); annota questo valore assieme al volume finale (V2) in tabella. 1 2 V (cm3) 40±1 18±1 PV 4000±100 3500±100 P (kPa) 101±2 193±2 Come si vede il prodotto PV non è costante come vorrebbe la legge di Boyle: P1 V 1 =P2 V 2 Uno dei motivi è che con il procedimento illustrato, viene sottostimato il volume, infatti il volume di aria contenuto nei tubi di collegamento e nel sensore non è considerato nella taratura della siringa. Chiamiamo questo volume incognito V0 e calcoliamolo imponendo valida la legge di Boyle considerando anche questo volume aggiuntivo: P1 V 1 V 0 =P 2 V 2 V 0 , V 0= P1 V 1 −P 2 V 2 ≃ 6 cm3 P2 −P1 Temperatura variabile Seleziona un tratto del grafico della temperatura prima della compressione (T 1); annota il valore (in gradi Kelvin) in una tabella in cui inserisci anche P1 e V1, quest’ultimo aumentato della quantità precedentemente calcolata. Individua poi il valore di picco della temperatura (T2, che segue di circa 0,5 s quello della pressione) e il corrispondente valore della pressione (P 2). Per ottenere T2 e P2 allo stesso istante usa il cursore come mostrato in figura. Anche V2 sarà aumentato della quantità V0. V(cm3) P (kPa) T (K) PV T kPa⋅cm 3 K 1 2 46±1 24±1 101±2 204±2 305,7±0,5 320,0±0,5 15±1 15±1 Nell’ultima colonna della tabella è stato calcolato (con il metodo delle cifre significative) il rapporto PV che per la legge dei gas perfetti è costante, dipendendo solo dal numero di moli. Come si vede T i due valori coincidono. Osservazioni È possibile notare come la temperatura non rimanga costante in compressioni e decompressioni rapide come quelle descritte in questo esperimento che sono essenzialmente adiabatiche; la temperatura ritorna poi lentamente al valore ambiente perché c’è in effetti un flusso di calore attraverso le pareti della siringa. Il metodo di correggere il volume del gas per il contributo dei tubi di connessione potrebbe essere applicato anche nell’esperimento della legge di Boyle (vedi l’apposita scheda intitolata “Trasformazione isoterma”) utilizzando due coppie di dati per determinarlo e poi utilizzandolo nella elaborazione degli altri. Titolo: Macchina termica ciclica Strumenti e materiali • 1 pistone a basso attrito (Heat engine/Gas Law Apparatus); • 1 cilindro di alluminio con anello di supporto e tubo di collegamento lungo con connettore a baionetta; • 1 sensore di pressione relativa (Relative Pressure Sensor, per le caratteristiche vedi la scheda allegata allo strumento); • 1 tubo di collegamento corto con 2 connettori a baionetta; • 2 becher (capacità 1000 ml), uno contenente acqua calda, uno contenente acqua fredda; • 1 piastra riscaldante; • 1 eventuale massa tarata (100 – 200 g) o altro oggetto di massa non superiore; • 1 cavo di collegamento. Montaggio Disponi il cilindro con basso attrito in posizione verticale, collega ad esso il cilindro di alluminio mediante il connettore a baionetta e alla seconda valvola il sensore di pressione relativa usando il tubo corto con due connettori a baionetta. Collega il sensore al Power Link. Riempi uno dei due becher con acqua calda (70°-80°C, utilizza la piastra riscladante) e l’altro con acqua fredda (è sufficiente l’acqua prelevata dal rubinetto del laboratorio, la cui temperatura si aggira sui 17-18°C). Procedimento L’esperimento consiste nel realizzare una trasformazione ciclica che consenta di sollevare un oggetto (collocato al di sopra del pistone) e di ripristinare le condizioni iniziali per il sollevamento di un altro oggetto. a. La situazione di partenza prevede di avere il cilindro di alluminio immerso nel contenitore di acqua fredda e il pistone scarico; preleva Pa (in kPa) e Va (in cm3); a. → b. il passo successivo è quello di collocare l’oggetto sopra al piatto del pistone, la pressione aumenterà e il volume diminuirà; per la rapidità con cui avviene questa compressione può essere ritenuta una adiabatica; b. preleva Pb (in kPa) e Vb (in cm3); b. → c. immergi il cilindro di alluminio nel contenitore di acqua calda, l’aria contenuta all’interno compirà una espansione isobara sollevando sia il pistone che l’oggetto aggiuntivo; c. preleva Pc (in kPa) e Vc (in cm3); c. → d. quando il pistone raggiunge la massima quota grazie alla espansione isobara, togli l’oggetto aggiuntivo e il pistone si solleverà ancora mentre la pressione diminuirà bruscamente; anche in questo caso la rapidità con cui avviene la trasformazione rende trascurabili gli scambi di calore con l’esterno e la trasformazione può essere considerata adiabatica; d. preleva Pd (in kPa) e Vd (in cm3); d. → a’. infine immergi il cilindro di alluminio nell’acqua fredda realizzando una compressione isobara che dovrebbe permetterti di ritornare nello stato iniziale; in realtà molto spesso ciò non accade, in particolare il volume finale è inferiore a quello iniziale e questo può essere facilmente attribuito alle perdite del pistone a basso attrito. Per misurare il volume devi prelevare la quote a cui arriva il pistone leggendo la scala (in mm) impressa sul cilindro in cui esso scorre e moltiplicarlo per la superficie di base del pistone che si ottiene utilizzando il diametro fornito dal costruttore. 2 2 d 32 ,5 mm S=π =π =829 , 58 mm 3 ≃0, 830 cm3 2 2 S= 0, 830±0, 001 cm 3 Prelevare in forma grafica i dati di pressione relativa ed elaborali selezionando i tratti opportuni. Risultati Di seguito sono riportati il grafico della pressione relativa e la tabella con tutte le misure. Stato a b c d a’ h (mm) 12,0±0,5 9,0±0,5 27,0±0,5 28,0±0,5 7,0±0,5 V (cm3) 1,00±0,01 0,75±0,01 2,24±0,01 2,32±0,01 0,58±0,01 Prel (kPa) 0,4±0,1 1,4±0,1 1,4±0,1 0,4±0,1 0,4±0,1 Le misure e le trasformazioni effettuate possono essere rappresentate nel piano pressione-volume su carta millimetrata, ottenendo un grafico simile a quello rappresentato in figura, in cui al solito le isobare sono rappresentate da segmenti paralleli all’asse x, mentre le adiabatiche sono approssimate da segmenti con pendenza negativa. Risultati Questo esperimento mostra come sia necessario scambiare calore con due sorgenti per realizzare una trasformazione ciclica. Dal punto di vista quantitativo è possibile calcolare il lavoro termodinamico come area racchiusa dal ciclo nel piano P-V; è possibile farlo calcolando l’area del parallelogramma abcd o mediante l’utilizzo di carta millimetrata. Seguiremo il primo metodo, applicando la formula dell’area del trapezio poiché i lati opposti obliqui non sono congruenti: L= V c −V b V d−V a ⋅ P −P =2, 24 cm3 −0, 75 cm3 2, 32 cm3 −1, 00 cm 3 ⋅ 1,4 kPa−0,4 kPa = b a 2 2 ¿ 1, 405⋅10−6 m3 1,0 103 Pa≃1,4⋅10−3 J =0, 014 J In definitiva: Lter = 0, 014±0, 001 J È possibile confrontare questo risultato con il lavoro meccanico di sollevamento dell’oggetto dato da L= m⋅g⋅h dove m è la massa dell’oggetto e h lo spostamento verticale che possiamo leggere sulla scala. Nel caso in esame la massa dell’oggetto da sollevare (un telefonino) è m= (0,081±0,001) kg . L’oggetto viene sollevato dalla situazione b a quella d in cui viene tolto dal piatto h= h d − h b = 28 ,0−9,0 mm=19 ,0 mm Δh= Δhd Δh b = 0,5 mm0,5 mm=1 mm h= 19±1 mm= 0, 019±0, 001 m Il lavoro meccanico prodotto è N L=m⋅g⋅h=0,081 kg⋅9, 81 ⋅0, 019 m=0, 015 J kg In definitiva: Lmec = 0, 015±0,001 J Le due stime di lavoro sono compatibili entro le incertezze sperimentali valutate con il metodo delle cifre significative. Osservazioni Tanto maggiore è la differenza di temperatura tra i due becher e tanto maggiori sono i sollevamenti che si producono in ogni ciclo di riscaldamento/raffreddamento. Come si vede il ciclo non si “chiude”: il volume finale è inferiore a quello iniziale, è facile imputare questo alle perdite di gas del pistone e dei connettori. Per migliorare la tenuta del cilindro di alluminio e quella tra i connettori e i tubi è stato consigliato di utilizzare vaselina bianca (come una sorta di grasso di tenuta economico), questa operazione non è stata però compiuta. Secondo esperimento Per ulteriore esemplificazione, si riportano i dati di un secondo esperimento realizzato di seguito al precedente dove il sollevamento ottenuto è minore a seguito del raffreddamento della sorgente calda e del riscaldamento di quella fredda. L’esperimento potrebbe essere arricchito dalla misura delle temperature delle sorgenti realizzata con il sensore di pressione assoluta/temperatura con la sola sonda di temperatura collegata. Stato a b c d a’ L= h (mm) 6,0±0,5 3,0±0,5 20,0±0,5 21,0±0,5 2,0±0,5 V (cm3) 0,50±0,01 0,25±0,01 1,66±0,01 1,74±0,01 0,17±0,01 P (kPa) 0,4±0,1 1,4±0,1 1,4±0,1 0,4±0,1 0,4±0,1 V c −V b V d−V a ⋅ P −P =1, 66 cm 3 −0, 25 cm3 1, 74 cm 3 −0,50 cm3 ⋅ 1,4 kPa−0,4 kPa = b a 2 2 ¿ 1, 325⋅10−6 m3 1,0 10 3 Pa≃1,3⋅10−3 J =0, 013 J Quindi: Lter = 0, 013±0, 001 J Confrontiamo ancora questo risultato con il lavoro meccanico di sollevamento dell’oggetto dato da L= m⋅g⋅h dove m è la massa dell’oggetto e h la variazione di altezza che possiamo leggere sulla scala. La massa dell’oggetto da sollevare è ancora m= (0,081±0,001) kg . L’oggetto viene sollevato dalla situazione b a quella d in cui viene tolto dal piatto h= h d − h b = 21 ,0−3,0 mm=18 ,0 mm Δh= Δhd Δh b = 0,5 mm0,5 mm=1 mm h= 18±1 mm= 0, 018±0, 001 m Il lavoro meccanico prodotto è N L=m⋅g⋅h=0,081 kg⋅9, 81 ⋅0, 018 m=0, 014 J kg In definitiva: Lmec = 0, 014±0, 001 J Anche in questo caso c’è accordo tra le due misure di lavoro. Titolo: Macchina termica unidirezionale Strumenti e materiali • 1 pistone a basso attrito (Heat Engine/Gas Law Apparatus); • 1 cilindro di alluminio con anello di supporto e tubo di collegamento lungo con connettore a baionetta; • 1 tubo di collegamento “a y” (con valvole ad una via e connettore a baionetta); • 2 becher (capacità 1000 ml), uno contenente acqua calda, uno contenente acqua fredda; • 1 piastra riscaldante; • 1 eventuale massa tarata (100 – 200 g) o altro oggetto di massa non superiore. Montaggio Disponi il cilindro con basso attrito in posizione verticale e chiudi, con la pinza serra-tubo, una delle due valvole. Sostituisci il tubo di collegamento semplice del cilindro di alluminio con quello “a y” e, mediante il connettore a baionetta, collega il cilindro al pistone a basso attrito. Riempi uno dei due becher con acqua calda (70°-80°C, utilizza la piastra riscaldante) e l’altro con acqua fredda (è sufficiente l’acqua prelevata dal rubinetto del laboratorio). Procedimento Immergendo alternativamente il cilindro di alluminio nell’acqua calda e nell’acqua fredda si riesce a sollevare il pistone fino all’altezza desiderata. Infatti quando il cilindro viene immerso nell’acqua calda, l’aria all’interno si espande e fluendo attraverso la valvola ad una via posta lungo il ramo più lungo della “y” solleva il pistone; la valvola presente nel ramo più corto è orientata in modo opposto alla prima e impedisce al gas in espansione di uscire all’esterno. Quando il cilindro viene immerso nell’acqua fredda il gas si contrae diminuendo la propria pressione; poiché non può fluire indietro attraverso la prima valvola, il pistone resta alla medesima quota, mentre dall’esterno entra gas nel cilindro attraverso la seconda valvola (poiché la pressione esterna è maggiore di quella interna). In altre parole, durante l’immersione in acqua calda il gas del cilindro di alluminio si espande sollevando il pistone, mentre durante l’immersione in acqua fredda il cilindro viene “alimentato” da aria a pressione atmosferica proveniente dall’ambiente esterno ripristinando la situazione iniziale e permettendo alla successiva immersione in acqua calda di sollevare ulteriormente il pistone. Risultati L’esperienza è di tipo qualitativo e ha lo scopo di mostrare come anche in una macchina non ciclica sia necessario scambiare calore con due sorgenti, una più fredda e una più calda, per ottenere lavoro in modo continuativo. Si può tentare di verificare sperimentalmente la relazione L=P⋅ΔV dove è possibile calcolare L come L= m⋅g⋅Δh dove m è la massa del pistone fornita dal costruttore (a cui va sommata la massa dell’eventuale oggetto aggiuntivo) e h lo spostamento verticale che possiamo leggere sulla scala impressa sul cilindro; P può essere misurato collegando il sensore di pressione assoluta alla seconda valvola del pistone a basso attrito (con il tubo corto con due connettori a baionetta) e ΔV può essere calcolato come prodotto della superficie S del pistone (che trovi utilizzando il diametro fornito dal costruttore) e h. Una verifica simile viene proposta nella scheda intitolata “Macchina termica ciclica”. Osservazioni Tanto maggiore è la differenza di temperatura tra i due becher, tanto maggiori sono i sollevamenti che si producono in ogni ciclo di riscaldamento/raffreddamento. Per migliorare la tenuta del cilindro di alluminio e quella tra i connettori e i tubi è stato consigliato di utilizzare vaselina bianca (come una sorta di grasso di tenuta economico), questa operazione non è stata finora compiuta.